5-Methoxy-1H-indol ist eine chemische Verbindung und ein Derivat des 1H-Indols.
| Strukturformel | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
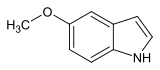
| |||||||||||||||||||
| Allgemeines | |||||||||||||||||||
| Name | 5-Methoxy-1H-indol | ||||||||||||||||||
| Andere Namen |
5-Methoxyindol | ||||||||||||||||||
| Summenformel | C9H9NO | ||||||||||||||||||
| Kurzbeschreibung |
beige Kristalle[1] | ||||||||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||||||||
| |||||||||||||||||||
| Eigenschaften | |||||||||||||||||||
| Molare Masse | 147,17 g·mol−1 | ||||||||||||||||||
| Aggregatzustand |
fest[1] | ||||||||||||||||||
| Schmelzpunkt |
52–55 °C[1] | ||||||||||||||||||
| Siedepunkt |
176–178 °C[1] | ||||||||||||||||||
| Sicherheitshinweise | |||||||||||||||||||
| |||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). | |||||||||||||||||||
Darstellung
BearbeitenEine Synthese ist ausgehend von para-Aminoanisol möglich. Dieses muss zunächst durch Diazotierung und Reduktion der Azoverbindung zum Hydrazin umgesetzt werden[2] und dann mit Acetaldehyd im Sinne einer Fischer-Indol-Synthese reagieren.[3][4]
Einzelnachweise
Bearbeiten- ↑ a b c d e f Datenblatt 5-Methoxy-1H-indol bei Sigma-Aldrich, abgerufen am 17. Oktober 2021 (PDF).
- ↑ S. Zhao, Y. Zhang, H. Zhou, S. Xi, B. Zou, G. Bao, L. Wang, J. Wang, T. Zeng, P. Gong, X. Zhai: Synthesis and biological evaluation of 4-(2-fluorophenoxy)-3,3′-bipyridine derivatives as potential c-met inhibitors. In: Eur. J. Med. Chem. Band 120, 2016, S. 3, doi:10.1016/j.ejmech.2016.04.062.
- ↑ A. R. Maguire, S. J. Plunkett, S. Papot, M. Clynes, R. O’Connor, S. Touhey: Synthesis of Indomethacin Analogues for Evaluation as Modulators of MRP Activity. In: Bioorg. Med. Chem. Band 9, Nr. 3, 2000, S. 745–762, doi:10.1016/s0968-0896(00)00292-3, PMID 11310610.
- ↑ N. N. Suvorov, V. N. Shkil'kova, N. Y. Podkhalyuzina: CATALYTIC SYNTHESIS OF 4-, 5-, 6-, AND 7-METHOXYINDOLES. In: Chem. Heterocycl. Compd. Band 18, 1983, S. 802–803, doi:10.1007/BF00506582.
