Benzolsulfonylchlorid
Benzolsulfonylchlorid ist eine chemische Verbindung aus der Gruppe der Organoschwefelverbindungen.
| Strukturformel | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
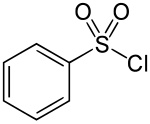
| |||||||||||||||||||
| Allgemeines | |||||||||||||||||||
| Name | Benzolsulfonylchlorid | ||||||||||||||||||
| Andere Namen |
| ||||||||||||||||||
| Summenformel | C6H5ClO2S | ||||||||||||||||||
| Kurzbeschreibung |
farblose bis grünliche Flüssigkeit mit unangenehmem stechendem Geruch[1] | ||||||||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||||||||
| |||||||||||||||||||
| Eigenschaften | |||||||||||||||||||
| Molare Masse | 176,62 g·mol−1 | ||||||||||||||||||
| Aggregatzustand |
flüssig[1] | ||||||||||||||||||
| Dichte |
1,38 g·cm−3[1] | ||||||||||||||||||
| Schmelzpunkt | |||||||||||||||||||
| Siedepunkt |
251 °C (Zersetzung)[1] | ||||||||||||||||||
| Dampfdruck | |||||||||||||||||||
| Löslichkeit |
Zersetzung in Wasser[1] | ||||||||||||||||||
| Brechungsindex |
1,553 (20 °C, 589 nm)[2] | ||||||||||||||||||
| Sicherheitshinweise | |||||||||||||||||||
| |||||||||||||||||||
| Toxikologische Daten | |||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). Brechungsindex: Na-D-Linie, 20 °C | |||||||||||||||||||
Gewinnung und Darstellung
BearbeitenBenzolsulfonylchlorid kann durch Reaktion von Natriumbenzolsulfonat mit Phosphorpentachlorid oder Phosphoroxychlorid sowie durch Reaktion von Benzol mit Chlorsulfonsäure gewonnen werden.[3]
Eigenschaften
BearbeitenBenzolsulfonylchlorid ist eine brennbare, wenig flüchtige, farblose bis grünliche Flüssigkeit mit unangenehmem stechendem Geruch, die praktisch unlöslich in Wasser ist. Sie zersetzt sich bei Erhitzung über 251 °C.[1] Sie reagiert mit Wasser, Ammoniak, Ethanol oder Phenol zum zugehörigen Benzolsulfonsäurederivat. Mit Benzol bildet sie durch eine Friedel-Crafts-Reaktion Diphenylsulfon.[4]
Verwendung
BearbeitenBenzolsulfonylchlorid wird für die Hinsberg-Trennung von primären von sekundären Aminen verwendet, wobei diese durch Reaktion mit der Verbindung in Benzolsulfonsäureamide überführt werden deren unterschiedliche Löslichkeit dann ausgenutzt wird.[5] Es wird als Zwischenprodukt bei der Herstellung von Benzolsulfonamiden, Thiophenolen, Glybazol und Benzonitrilen verwendet.[6]
Einzelnachweise
Bearbeiten- ↑ a b c d e f g h i j k Eintrag zu Benzolsulfonylchlorid in der GESTIS-Stoffdatenbank des IFA, abgerufen am 3. Januar 2023. (JavaScript erforderlich)
- ↑ Datenblatt Benzolsulfonylchlorid bei Merck, abgerufen am 31. Dezember 2012.
- ↑ Roger Adams and C. S. Marvel: Benzolsulfonyl Chloride In: Organic Syntheses. 1, 1921, S. 21, doi:10.15227/orgsyn.001.0021; Coll. Vol. 1, 1941, S. 84 (PDF).
- ↑ Raj K. Bansal: A Textbook Of Organic Chemistry. New Age International, 2003, ISBN 81-224-1459-1, S. 632 (eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ Richard Göttlich, Siegfried Schindler: Chemisches Grundpraktikum im Nebenfach. Pearson Deutschland GmbH, 2011, ISBN 3-86894-030-8, S. 225 (eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ Sittig's Handbook of Toxic and Hazardous Chemicals and Carcinogens, 5th Edition. 2000, ISBN 0-8155-1553-7, S. 334 (eingeschränkte Vorschau in der Google-Buchsuche).

