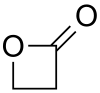
Propiolacton (nach IUPAC Oxetan-2-on) ist eine organische chemische Verbindung und zählt zur Stoffgruppe der β-Lactone, intramolekularer, cyclischer Ester.
| Strukturformel | ||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| ||||||||||||||||||||||
| Allgemeines | ||||||||||||||||||||||
| Name | Propiolacton | |||||||||||||||||||||
| Andere Namen |
| |||||||||||||||||||||
| Summenformel | C3H4O2 | |||||||||||||||||||||
| Kurzbeschreibung |
farblose Flüssigkeit mit stechendem Geruch[1] | |||||||||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Eigenschaften | ||||||||||||||||||||||
| Molare Masse | 72,06 g·mol−1 | |||||||||||||||||||||
| Aggregatzustand |
flüssig | |||||||||||||||||||||
| Dichte |
1,15 g·cm−3 (20 °C)[1] | |||||||||||||||||||||
| Schmelzpunkt | ||||||||||||||||||||||
| Siedepunkt |
155 °C (Zersetzung)[1] | |||||||||||||||||||||
| Dampfdruck | ||||||||||||||||||||||
| Löslichkeit |
löslich in Wasser, Ethanol, Aceton und Chloroform[2] | |||||||||||||||||||||
| Brechungsindex |
1,4105 (20 °C)[3] | |||||||||||||||||||||
| Sicherheitshinweise | ||||||||||||||||||||||
| ||||||||||||||||||||||
| MAK | ||||||||||||||||||||||
| Thermodynamische Eigenschaften | ||||||||||||||||||||||
| ΔHf0 |
−329,9 kJ/mol[6] | |||||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). Brechungsindex: Na-D-Linie, 20 °C | ||||||||||||||||||||||
Gewinnung und Darstellung
BearbeitenPropiolacton wird industriell durch Umsetzung von Formaldehyd mit Keten in Gegenwart von Aluminiumchlorid, Zinkchlorid oder Bortrifluorid als Katalysator hergestellt.[7]
Die Selektivität zu Propiolacton beträgt hierbei 90 %. Die Reaktion kann in einem Lösungsmittel oder in der Gasphase durchgeführt werden.[7]
2010 wurde die Synthese von Propiolacton durch Umsetzung von Ethylenoxid mit Kohlenmonoxid in Gegenwart eines komplexstabilisierten Carbonylcobaltats in einem höhersiedenden dipolar aprotischen Lösemittel mit Umsatz und Selektivität von bis zu 99 % beschrieben.[8]
Eigenschaften
BearbeitenPhysikalische Eigenschaften
BearbeitenPropiolacton ist gut wasserlöslich und mischbar mit polaren organischen Lösungsmitteln wie Ethanol, Aceton, Diethylether und Chloroform. Bei Raumtemperatur liegt Propiolacton als brennbare, farblose Flüssigkeit mit schwach süßlichem Geruch vor. Gekühlt ist es länger stabil, bei Raumtemperatur jedoch nicht.[9]
Chemische Eigenschaften
BearbeitenDie hochreaktive Verbindung ist in Wasser gelöst einige Stunden stabil; erst bei starker Verdünnung oder Stehenlassen über mehrere Stunden hydrolysiert das Lacton zur β-Hydroxypropionsäure:[10]
- Propiolacton hydrolysiert zur β-Hydroxypropionsäure
Die Verbindung kann analog mit Aminen, Thiolen und anderen Nucleophilen unter Ringöffnung reagieren, wobei dann die entsprechenden Amide, Thiolcarbonsäuren oder andere Carbonsäurederivate der 3-Hydroxypropionsäure entstehen.[11]
Propiolacton reagiert bei 140–180 °C und 25–250 bar mit Orthophosphorsäure und Kupferpulver als Katalysator quantitativ zu Acrylsäure und bei Anwesenheit eines Alkohols zu den entsprechenden Acrylsäureestern.[7]
Toxikologische Eigenschaften
BearbeitenDer LD50 (oral, Ratte) wurde auf 50–100 mg/kg Körpergewicht bestimmt.[12] Die toxische Wirkung ist gekennzeichnet durch einen raschen Wirkungseintritt.[12] Zu den Vergiftungssymptomen zählen Zittern, Keuchen, blutige Durchfälle, Tremor und Krämpfe.[12] In Tierversuchen trat der Tod innerhalb von Stunden bis Tagen durch Lungenödeme, Darmblutungen oder Hirnödeme ein.[12]
In verschiedenen Versuchen erwies es sich als mutagen und kanzerogen (sowohl lokale als auch systemische Tumoren konnten induziert werden).[12]
Verwendung
BearbeitenPropiolacton wird unter anderem zur Virusinaktivierung und zur Sterilisation von Impfstoffen eingesetzt. Dabei sind 0,2 bis 0,4%ige wässrige Lösungen über einen weiten pH-Bereich viruzid wirksam. Da der Stoff im wässrigen Medium innerhalb weniger Stunden zerfällt, verbleibt kein Rückstand des toxischen Lactons.[10]
Literatur
Bearbeiten- W. Stephan: Inactivation of hepatitis viruses and HIV in plasma and plasma derivatives by treatment with beta-propiolactone/UV irradiation. In: Current studies in hematology and blood transfusion. Nummer 56, 1989, S. 122–127, PMID 2642784 (Review).
Einzelnachweise
Bearbeiten- ↑ a b c d e f g h i j Eintrag zu Propiolacton in der GESTIS-Stoffdatenbank des IFA, abgerufen am 2. Juli 2016. (JavaScript erforderlich)
- ↑ Hans-Dieter Jakubke, Ruth Karcher (Koordinatoren): Lexikon der Chemie in drei Bänden, Spektrum Verlag, Heidelberg, Band 3, 1999, ISBN 3-8274-0381-2, S. 105.
- ↑ David R. Lide (Hrsg.): CRC Handbook of Chemistry and Physics. 90. Auflage. (Internet-Version: 2010), CRC Press / Taylor and Francis, Boca Raton FL, Physical Constants of Organic Compounds, S. 3-408.
- ↑ Eintrag zu Propiolactone im Classification and Labelling Inventory der Europäischen Chemikalienagentur (ECHA), abgerufen am 1. August 2016. Hersteller bzw. Inverkehrbringer können die harmonisierte Einstufung und Kennzeichnung erweitern.
- ↑ Schweizerische Unfallversicherungsanstalt (Suva): Grenzwerte – Aktuelle MAK- und BAT-Werte (Suche nach 57-57-8 bzw. β-Propiolacton), abgerufen am 6. November 2020.
- ↑ David R. Lide (Hrsg.): CRC Handbook of Chemistry and Physics. 90. Auflage. (Internet-Version: 2010), CRC Press / Taylor and Francis, Boca Raton FL, Standard Thermodynamic Properties of Chemical Substances, S. 5-23.
- ↑ a b c Hans-Jürgen Arpe: Industrielle Organische Chemie - Bedeutende Vor- und Zwischenprodukte. 6. Auflage. WILEY-VCH Verlag GmbH & Co. KGaA, Weinheim 2007, ISBN 978-3-527-31540-6, S. 322.
- ↑ Patentanmeldung WO 2010/118128: Process for beta-lactone production. Scott D. Allen et al., Novomer Inc., published 14 October 2010.
- ↑ Tse‐Lok Ho, Mary Fieser, Louis Fieser: β‐Propiolactone. In: Fieser and Fieser's Reagents for Organic Synthesis. 15. Dezember 2006, doi:10.1002/9780471264194.fos08613.
- ↑ a b F. v. Rheinbaben, M. H. Wolff: Handbuch der viruswirksamen Desinfektion. Springer, 2002, ISBN 978-3-540-67532-7.
- ↑ H. P. Latscha, U. Kazmaier, H. A. Klein: Organische Chemie: Chemie-Basiswissen II, 6. Auflage, Springer, 2008, ISBN 978-3-540-77106-7, S. 281.
- ↑ a b c d e Manfred Metzler, Frank J. Hennecke: Toxikologie für Naturwissenschaftler und Mediziner Stoffe, Mechanismen, Prüfverfahren. 3., überarb. und aktualisierte Auflage. Weinheim 2005, ISBN 978-3-527-30989-4, S. 26–267.

