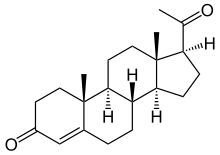
Corticosteroide oder Kortikosteroide (von lateinisch cortex = ‚Rinde‘; gr. stereos, στερεός = ‚fest‘), kurz auch Corticoide, Kortikoide oder Cortine geschrieben, sind eine Gruppe von ca. 50 in der Nebennierenrinde (dem Kortex der Nebenniere) gebildeten Steroidhormonen sowie chemisch vergleichbaren synthetischen Stoffen. Alle Corticoide entstehen dabei aus dem Ausgangsstoff Cholesterin. Gemeinsames Grundgerüst der Hormone ist das Progesteron (Δ4-Pregnen-3,20-dion).
Die Corticosteroide lassen sich nach ihrer biologischen Wirkung bzw. ihrem Bildungsort in drei Gruppen einteilen:
- Mineralocorticoide (Hauptvertreter Aldosteron) werden in der Zona glomerulosa der Nebennierenrinde gebildet und beeinflussen vorwiegend den Kalium-Natrium-Haushalt und damit den Wassergehalt des Körpers.
- Glucocorticoide (Hauptvertreter Cortisol) werden in der Zona fasciculata der Nebennierenrinde gebildet. Sie vermitteln wichtige Wirkungen im Glucose-, Lipid- und Proteinstoffwechsel.
- Androgene (Hauptvertreter Dehydroepiandrosteron (DHEA)) und Estrogene werden in der Zona reticularis der Nebennierenrinde gebildet.
Zu den natürlichen Glucocorticoiden gehören Cortison, Corticosteron und Cortisol; zu den Mineralocorticoiden das Aldosteron und das bereits 1935 von Reichstein isolierte Desoxycorticosteron. Synthetische Corticoide sind z. B. Prednison und Prednisolon, Methylprednisolon, Triamcinolon, Dexamethason, Betamethason und Paramethason.
Synthese
BearbeitenDie unterschiedlichen Hormone werden aus Progesteron durch Hydroxylierung (Einbau von OH-Gruppen) und Oxidation dieser Gruppen zu Keto- oder Aldehydgruppen an verschiedenen Positionen gebildet. Die Synthese und Sekretion der Androgene und Glucocorticoide wird durch ACTH (Kortikotropin) aus der Adenohypophyse (Hypophysenvorderlappen der Hirnanhangdrüse) stimuliert. Die Synthese und Sekretion der Mineralocorticoide wird über Angiotensin II und Kalium stimuliert.
Wirkung
BearbeitenAls lipophile Hormone wirken Corticosteroide auf Rezeptoren im Zytosol und Zellkern, zu denen sie frei durch die Zellmembran diffundieren können. Inzwischen wird aber auch die Existenz von membranständigen Rezeptoren für Kortikoide angenommen und erforscht.[1] Die Rezeptoren im Zellinneren kann man in zwei Typen aufteilen. Typ I ist spezifisch für Mineralcorticoide und Typ II für Glucocorticoide.[1] Die Spezifität der Rezeptoren scheint von der Aktivität der 11β-Hydroxysteroid-Dehydrogenase 1 abhängig zu sein, die durch eine Dehydrierung der β-OH-Gruppe am C11Atom erfolgt. Dadurch werden die Corticoide bzw. 11-Oxykortikosteroide[2] (mit Ausnahme des Aldosterons) unwirksam. Exzessiver Genuss von Lakritze kann die 11-Hydroxysteroid-Dehydrogenase hemmen und so zu stärkeren Wirkungen der Mineralcorticoide führen.[1]
Überproduktion, Mangel
BearbeitenKrankhafte Überproduktion, etwa bei Stress, oder langdauernde Einnahme von Glucocorticoiden erzeugen ein charakteristisches Krankheitsbild (Cushing-Syndrom) mit Osteoporose, Diabetes mellitus, Fettsucht (v. a. Stammfettsucht) und Muskelschwund. Zu hohe Mineralocorticoid-Konzentrationen stören den Wasser-Elektrolythaushalt und schädigen die Nieren (Conn-Syndrom).
Ein Mangel an Nebennierenrindenhormonen erzeugt den Morbus Addison, eine lebensbedrohliche Erkrankung mit Kreislaufschwäche, Austrocknung und Kachexie. Ein bestimmter Gendefekt, bei dem zu viel Androgene und zu wenig Aldosteron produziert werden, verursacht Virilismus und Wassereinlagerung; das Vollbild der Krankheit wird als adrenogenitales Syndrom bezeichnet.
Abbau
BearbeitenCorticoide werden in der Leber durch Reduktion zu inaktiven Derivaten (17-Hydroxysteroide, 17-Ketosteroide) umgewandelt und über Urin und Gallenflüssigkeit ausgeschieden.
Therapie
BearbeitenAußer bei den o. g. Mangelzuständen werden vor allem Glucocorticoide in zahlreichen Immunerkrankungen und Notfallsituationen als Medikament eingesetzt. Die natürlichen Corticoide sind gegenüber den künstlichen Corticoiden schwächer wirksam. Medikamente mit einer höheren Affinität binden sich leichter an die Rezeptoren und haben bei gleicher Arzneimittelkonzentration eine größere Wirkung.
Für die orale und intravenöse Therapie werden Äquivalenzdosen (die gleichwirksame Dosis Cortison) angegeben. Prednison (17α,21-Dihydroxy-1,4-pregnadien-3,20-dion) ist ein künstliches Corticoid, welches einer dehydrierten Variante des Cortisons entspricht. Seine Wirkung liegt etwa bei der vier- bis fünffachen des Cortisons.
Corticoide werden zur Behandlung von u. a. Autoimmunerkrankungen wie Asthma, Cluster-Kopfschmerz, Ekzemen, Epilepsie, Hörsturz sowie akutem Tinnitus,[3] Nephritis, Neurodermitis und bei bestimmten Chemotherapien (Morbus Hodgkin, NHL) eingesetzt.
Unerwünschte Wirkungen
BearbeitenDa Corticosteroide eine Magensäureüberproduktion induzieren, sollte bei dauerhafter Gabe zusätzlich ein Protonenpumpenhemmer genommen werden, um die Entstehung eines Magenulkus zu verhindern. Allgemein kann, insbesondere bei langfristiger und/oder hochdosierter Anwendung, eine große Zahl von Nebenwirkungen auftreten, insbesondere Störungen in der Hypothalamus-Hypophysen-Nebennieren-Achse mit der Folge einer sekundären Nebennierenrinden-Insuffizienz[4] (z. B. Cushing-Syndrom, siehe auch Absatz Überproduktion), die eine sorgfältige Abwägung bei der Anwendung erforderlich machen. Bei einer Stoßtherapie im Bereich der Behandlung von Epilepsie oder eines Multiple-Sklerose-Schubes muss etwa eine Stunde nach der Einnahme einer Dosis ein Magenschutzmittel verabreicht werden.
Durch die immunsuppressive Wirkung von Glucocorticoiden treten bei Patienten aufgrund der geschwächten Immunabwehr gehäuft Infektionen mit Viren, Bakterien oder Pilzen auf.[5]
Literatur
Bearbeiten- Jeremy M. Berg, John L. Tymoczko, Lubert Stryer: Biochemie. 6. Auflage, Spektrum Akademischer Verlag, Heidelberg 2007. ISBN 978-3-8274-1800-5.
- Donald Voet, Judith G. Voet: Biochemistry. 3. Auflage, John Wiley & Sons, New York 2004. ISBN 0-471-19350-X.
- Bruce Alberts, Alexander Johnson, Peter Walter, Julian Lewis, Martin Raff, Keith Roberts: Molecular Biology of the Cell, 5. Auflage, Taylor & Francis 2007, ISBN 978-0-8153-4106-2.
Anmerkungen
Bearbeiten- ↑ a b c Hans-Christian Pape, Armin Kurtz, Stefan Silbernagl: Physiologie. 7. Auflage. Georg Thieme Verlag, Stuttgart 2014, ISBN 978-3-13-796007-2, S. 613.
- ↑ Vgl. etwa Wilhelm Stepp: Was leistet die Diät in der modernen Krankenbehandlung. In: Münchener Medizinische Wochenschrift. Band 95, Nr. 1, 2. Januar 1953, S. 25–31 (Vortrag vor den Ärzten Vorarlbergs in Dornbirn am 20. Mai 1952), hier: S. 28–29.
- ↑ Eine Wirksamkeit ist hier jedoch nicht zuverlässig und stichhaltig belegt.
- ↑ M. M. Liu, A. B. Reidy, S. Saatee, C. D. Collard: Perioperative Steroid Management – Approaches Based on Current Evidence. In: Anesthesiology. Band 127, 2017, S. 166–172.
- ↑ Michael Brendler: Fatale Spritzen. Frankfurter Allgemeine Sonntagszeitung, 23. Oktober 2017.