Endogenes Retrovirus
Endogene Retroviren (ERV) sind Retroviren, die keinen vollständigen Replikationszyklus durchlaufen, sondern als Provirus von Generation zu Generation im Genom des Wirts weitervererbt werden. Man nimmt an, dass sie vor vielen Generationen durch Infektion der Keimbahnzellen von Menschen und anderen Wirbeltieren entstanden sind.
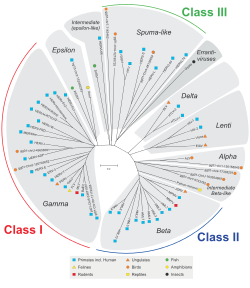
Eigenschaften
BearbeitenRetroviren sind Viren, die mit Hilfe des viralen Enzyms Reverse Transkriptase ihr RNA-Genom in DNA umschreiben, um sie in das Genom ihrer Wirtszelle integrieren zu können. Die meisten Retroviren können nur einige somatische Zelltypen infizieren. Wenn es einigen gelingt, Keimzellen zu infizieren und damit auf die nachfolgenden Generationen weitervererbt zu werden, werden sie zu endogenen Retroviren, die über lange Zeiträume im Genom ihrer Wirtsspezies verbleiben können.
Zum Teil bleiben endogene Retroviren nur über kurze Zeit (einige hundert Generationen) infektiös, weil sich bei der Replikation durch den Wirt Mutationen ansammeln, die zur schleichenden Virus-Inaktivierung führen. Grundsätzlich neigen die endogenen Retroviren zu Mutationen, weil sie keine Proteine codieren, die für die Zellen notwendig sind.
Andere bleiben aktiv und können weiterhin exogene Viruspartikel produzieren. Vollständige und damit prinzipiell replikationsfähige Proviren sind jedoch die Ausnahme und machen nur etwa 0,5 Prozent des menschlichen Genoms aus.[1]
Unter bestimmten Bedingungen kann eine Remobilisierung der endogenen Retroviren stattfinden, die dann eine Transposition durchführen. Diese mobilen Elemente, bei denen zum Teil nur die LTR-Regionen noch vorhanden (konserviert) sind, werden dann auch als LTR-Retrotransposons bezeichnet.
Geschichte
BearbeitenEndogene Retroviren wurden Ende der 1960er Jahre entdeckt. Drei verschiedene Typen endogener Retroviren wurden etwa gleichzeitig beschrieben: Das Aviäre Leukosevirus (ALV) aus dem Haushuhn (Gallus gallus) und das Murine Leukämievirus (MLV) sowie das Maus-Mammatumorvirus (MMTV) aus der Hausmaus (Mus musculus).
Bis 2007 ging man davon aus, dass nur die einfachen, nicht jedoch die komplexen Retroviren zu endogenen Retroviren werden können (eine Ausnahme bilden die Spumaviren).[2] 2007 wurde dann das erste endogene Retrovirus, das von einem Lentivirus und damit von einem komplexen Retrovirus stammt, beschrieben: Das rabbit endogenous lentivirus type K (RELIK).[3] Die einzige Retrovirus-Gattung, von der bisher keine endogenen Retroviren beschrieben wurden, sind somit die Deltaretroviren.
Humane endogene Retroviren
BearbeitenHumane endogene Retroviren (HERV) kommen in großer Zahl im menschlichen Genom vor. Da sie bereits vor sehr langer Zeit Bestandteil des Genoms wurden, haben sich in ihrer Sequenz zahlreiche Mutationen aller Art angesammelt, darunter Punktmutationen, Deletionen, Insertionen anderer Retroelemente, Rekombinationen und Mini- und Mikrosatelliten-Expansion. Die retroviralen Sequenzen sind daher bereits stark verändert und oft schwer zu finden.[4] Manche HERV stehen im Verdacht, an der Entwicklung mancher Autoimmunerkrankungen beteiligt zu sein, insbesondere mit Multipler Sklerose. Andere sorgen für die Entwicklung und Regulation wichtiger Organe, z. B. der Plazenta bei Säugetieren (siehe Syncytin).[5]
Im Rahmen des Humangenomprojekts wurden im menschlichen Genom mehrere tausend ERV gefunden, die zunächst in 24 verschiedene „Familien“ eingeteilt werden und etwa 8 % des menschlichen Genoms ausmachen.[6] Neueren Erkenntnissen zufolge sind es bereits 31 verschiedene Gruppen,[7] die jeweils durch ein einzelnes Integrationsereignis entstanden sind.[8]
Endogene Retroviren bei Schweinen
BearbeitenPorcine endogene Retroviren (PERV) sind die endogenen Retroviren der Schweine. Je nach Schweinerasse liegen 3 – 140 Kopien von PERV im Genom eines Schweines vor. Die Retroviren PERV-A und PERV-B finden sich bei allen Schweinerassen, PERV-C bei den meisten. Die ersten beiden Formen können im Laborversuch auch menschliche Zellen infizieren, PERV-C nur Schweinezellen. Jedoch können sich Rekombinationen der PERV bilden, die dann ebenfalls infektiös sein können.
Der einzige Weg, sie zu inaktivieren, ist die Genomentfernung mittels Genome editing. Ein früherer Versuch mit Zinkfinger-Nukleasen ist gescheitert, da die multiplen Genveränderungen sich am Ende als cytotoxisch erwiesen haben. Nun ist es aber gelungen, zunächst in immortalen Schweine-Zelllinien mittels CRISPR-Cas 62 PERV-Sequenzen zu eliminieren, und 2017 konnten lebende Schweine gezüchtet werden, nachdem 25 PERV-Sequenzen aus dem Genom entfernt wurden.
Die PERV und ihre Inaktivierung stehen im Fokus der Forschung, weil Schweine als Organspender für Xenotransplantationen in Betracht kommen und die PERV dabei ein Sicherheitsrisiko darstellen.[9][10]
Literatur
Bearbeiten- Retrotransposons, Endogenous Retroviruses, and the Evolution of Retroelements. In: John M. Coffin, Stephen H. Hughes, Harold Varmus: Retroviruses. Cold Spring Harbor Laboratory Press, Plainview NY 1997, ISBN 0-87969-497-1.
- Roswitha Löwer, Johannes Löwer, Reinhard Kurth: The viruses in all of us: Characteristics and biological significance of human endogenous retrovirus sequences. In: Proceedings of the National Academy of Sciences. (PNAS) 28. Mai 1996, Bd. 93, Nr. 11, S. 5177–5184, Volltext (PDF).
- Luis P Villarreal: Viruses and the Evolution of Life. ASM Press, Washington 2005.
Weblinks
Bearbeiten- kereng: Evolutionsbeweis durch endogene Retroviren, AG EvoBio vom 13. September 2010, abgerufen am 16. Februar 2020.
- HERVd – Human Endogenous Retrovirus Database, Institute of Molecular Genetics of the ASCR, abgerufen am 16. Februar 2020.
- Nadja Podbregar: Geheime Helfer - Welche Funktion haben endogene Retroviren in uns?, auf: scinexx.de vom 5. November 2010, abgerufen am 16. Februar 2020
- Reinhard Kurth: Entdeckung von Viren im menschlichen Erbgut, Spektrum der Wissenschaft 9 / 1993
Einzelnachweise
Bearbeiten- ↑ Christiane Hohmann: Parasiten im Genom. In: Pharmazeutische Zeitung. Juli 2010, abgerufen am 11. August 2017.
- ↑ Robin A. Weiss: The discovery of endogenous retroviruses In: Retrovirology. 3. Oktober 2006, Band 3, S. 67 → Review. PMID 17018135, doi:10.1186/1742-4690-3-67.
- ↑ Aris Katzourakis, Michael Tristem, Oliver G. Pybus, Robert J. Gifford: Discovery and analysis of the first endogenous lentivirus. In: Proceedings of the National Academy of Sciences. (PNAS) 10. April 2007, Band 104, Nr. 15, S. 6261–6265, PMID 17384150, Volltext
- ↑ Jan Paces, Adam Pavlícek, Václav Paces: HERVd: database of human endogenous retroviruses. In: Nucleic Acids Research. 2002, Bd. 30, Nr. 1, S. 205–206, Volltext.
- ↑ P. Perot, P. A. Bolze, F. Mallet: From Viruses to Genes: Syncytins. In: Günther Witzany (Hrsg.): Viruses: Essential Agents of Life. Springer, Dordrecht / New York 2012, ISBN 978-94-007-4898-9, S. 325–361.
- ↑ E. Lander u. a.: Initial sequencing and analysis of the human genome. In: Nature. 2001, Bd. 409, S. 860–921.
- ↑ E. C. Holmes: Ancient lentiviruses leave their mark. In: Proceedings of the National Academy of Sciences. (PNAS) 10. April 2007, Bd. 104, Nr. 15, S. 6095–6096, PMID 17404211.
- ↑ R. J. Gifford: Evolution at the host-retrovirus interface. In: Bioessays. Dez. 2006, Bd. 28, Nr. 12, S. 1153–1156, PMID 17117481.
- ↑ Joachim Denner: Paving the path toward procine Organs for transplantation New England Journal of Medicine 2017, Band 377, Ausgabe 19 vom 9. November 2017, Seiten 1891–1893, doi:10.1056/NEJMcibr1710853
- ↑ Sven Stockrahm: Schwein ist mein ganzes Herz. In: Zeit Online. 11. Juli 2017, abgerufen am 14. August 2017.