3-Hexanol ist eine chemische Verbindung aus der Gruppe der sekundären Alkohole. Sie ist eines der 17 Strukturisomere der Hexanole.
| Strukturformel | ||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
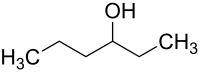
| ||||||||||||||||
| Strukturformel ohne definierte Angabe zur Stereochemie | ||||||||||||||||
| Allgemeines | ||||||||||||||||
| Name | 3-Hexanol | |||||||||||||||
| Andere Namen |
| |||||||||||||||
| Summenformel | C6H14O | |||||||||||||||
| Kurzbeschreibung |
entzündliche, wenig flüchtige Flüssigkeit[1] | |||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||
| ||||||||||||||||
| Eigenschaften | ||||||||||||||||
| Molare Masse | 102,18 g·mol−1 | |||||||||||||||
| Aggregatzustand |
flüssig | |||||||||||||||
| Dichte |
0,82 g·cm−3 (20 °C)[1] | |||||||||||||||
| Schmelzpunkt | ||||||||||||||||
| Siedepunkt |
135 °C[1] | |||||||||||||||
| Dampfdruck | ||||||||||||||||
| Löslichkeit |
| |||||||||||||||
| Brechungsindex |
1,415 (20 °C)[3] | |||||||||||||||
| Sicherheitshinweise | ||||||||||||||||
| ||||||||||||||||
| Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). Brechungsindex: Na-D-Linie, 20 °C | ||||||||||||||||
Isomere
BearbeitenDie Verbindung kommt in zwei stereoisomeren Formen vor. Wenn in der wissenschaftlichen Literatur oder in diesem Artikel von „3-Hexanol“ ohne jeden weiteren Zusatz die Rede ist, meint man in der Regel das Racemat, also (RS)-(±)-3-Hexanol, ein 1:1-Gemisch von (R)- und (S)-3-Hexanol.
| Isomere von 3-Hexanol | ||
| Name | (S)-3-Hexanol | (R)-3-Hexanol |
| Strukturformel | ||
| CAS-Nummer | 6210-51-1 | 13471-42-6 |
| 623-37-0 (unspez.) | ||
| EG-Nummer | – | – |
| 210-790-0 (unspez.) | ||
| ECHA-Infocard | – | – |
| 100.009.810 (unspez.) | ||
| PubChem | 638098 | 6994293 |
| 12178 (unspez.) | ||
| Wikidata | Q82123451 | |
| Q83763 (unspez.) | ||
Vorkommen
Bearbeiten3-Hexanol kommt natürlich in verschiedenen Pflanzen, wie Spanischem Pfeffer (Capsicum annuum),[4][5] der Färberdistel (Carthamus tinctorius),[4][5] Safran, Lavendel,[2] Papaya,[2] Preiselbeeren,[2] Bananen,[2] Melonen,[2] Süßgras,[2] Zitronenmelisse,[2] Ananas,[2] Moosbeeren (Vaccinium macrocarpon),[2] Parmesan,[2] gekochtem Hühnerfleisch,[2] Schwarzen Johannisbeeren,[2] Kakao[2] und Sojabohnen[2] vor.
-
Färberdistel
-
Bananen
-
Zitronenmelisse
-
Parmesan
Gewinnung und Darstellung
BearbeitenRacemisches 3-Hexanol kann durch Hydroborierung von 3-Hexen oder 3-Hexin gewonnen werden.[2]
Sicherheitshinweise
BearbeitenDie Verbindung bildet leicht entzündliche Dampf-Luft-Gemische. Sie hat einen Flammpunkt von 41 °C. Der Explosionsbereich liegt zwischen 1,1 Vol.‑% (45 g/m3) als untere Explosionsgrenze (UEG) und 7 Vol.‑% (298 g/m3) als obere Explosionsgrenze (OEG). Die Zündtemperatur beträgt 305 °C. Sie fällt somit in die Temperaturklasse T2.[6][1]
Weblinks
BearbeitenEinzelnachweise
Bearbeiten- ↑ a b c d e f g h i Eintrag zu 3-Hexanol in der GESTIS-Stoffdatenbank des IFA, abgerufen am 20. Januar 2022. (JavaScript erforderlich)
- ↑ a b c d e f g h i j k l m n o p George A. Burdock: Fenaroli’s Handbook of Flavor Ingredients. CRC Press, 2004, ISBN 1-4200-3787-0, S. 786 (englisch, eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ Datenblatt 3-Hexanol bei Sigma-Aldrich, abgerufen am 21. Februar 2011 (PDF).
- ↑ a b 3-HEXANOL (englisch). In: Dr. Duke's Phytochemical and Ethnobotanical Database, Hrsg. U.S. Department of Agriculture, abgerufen am 11. September 2021.
- ↑ a b 3-Hexanol. In: Liber Herbarum Minor (Deutsch). 9. April 2018, abgerufen am 12. September 2021.
- ↑ E. Brandes, W. Möller: Sicherheitstechnische Kenngrößen – Band 1: Brennbare Flüssigkeiten und Gase. Wirtschaftsverlag NW – Verlag für neue Wissenschaft GmbH, Bremerhaven 2003, ISBN 3-89701-745-8.

