Kaliumhydroxid (auch Ätzkali, kaustisches Kali), chemische Formel KOH, ist ein weißer hygroskopischer Feststoff. In Wasser löst es sich unter großer Wärmeentwicklung zu der starken Base Kalilauge. Mit Kohlenstoffdioxid der Luft reagiert es zu Kaliumcarbonat und wird deshalb in luftdichten Behältern aufbewahrt. Um zu verhindern, dass Kaliumhydroxid Wasser aus der Luft bindet, kann man es mit einem Trockenmittel lagern. Das Hydroxid-Ion verdrängt als starke Base schwächere und flüchtige Basen aus ihren Salzen.
| Kristallstruktur | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
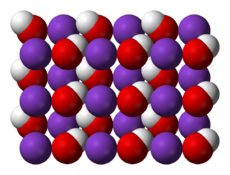
| |||||||||||||||||||
| _ K+ __ OH− | |||||||||||||||||||
| Allgemeines | |||||||||||||||||||
| Name | Kaliumhydroxid | ||||||||||||||||||
| Andere Namen | |||||||||||||||||||
| Verhältnisformel | KOH | ||||||||||||||||||
| Kurzbeschreibung |
weißer, hygroskopischer, geruchloser Feststoff[3] | ||||||||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||||||||
| |||||||||||||||||||
| Eigenschaften | |||||||||||||||||||
| Molare Masse | 56,11 g·mol−1 | ||||||||||||||||||
| Aggregatzustand |
fest[3] | ||||||||||||||||||
| Dichte |
2,04 g·cm−3[3] | ||||||||||||||||||
| Schmelzpunkt | |||||||||||||||||||
| Siedepunkt |
1327 °C[3] | ||||||||||||||||||
| Löslichkeit | |||||||||||||||||||
| Sicherheitshinweise | |||||||||||||||||||
| |||||||||||||||||||
| MAK |
Schweiz: 2 mg·m−3 (gemessen als einatembarer Staub)[5] | ||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). | |||||||||||||||||||
Eigenschaften
BearbeitenKaliumhydroxid ist ein weißer, stark hygroskopischer Stoff, der meist als Plätzchen oder Stangen, seltener als Pulver verkauft wird. In Wasser löst es sich unter großer Wärmeentwicklung durch die negative Lösungsenthalpie von −57,1 kJ/mol und bildet Kalilauge, im festen Zustand bildet es Mono-, Di- und Tetrahydrate. Mit dem in der Luft enthaltenen Kohlenstoffdioxid reagiert es unter Bildung von Kaliumcarbonat. Auch in Alkoholen wie Methanol und Ethanol ist Kaliumhydroxid löslich, „Alkoholisches Kali“ genannt.
Synthese
BearbeitenFrüher wurde Kaliumhydroxid durch Kaustifizierung von Kaliumcarbonat hergestellt. Dies verläuft nach der Gleichung
Heute wird Kaliumhydroxid meist durch wässrige Elektrolyse von Kaliumchlorid und anschließendes Eindampfen der Lösung gewonnen.
Verwendung
BearbeitenNach der zuvor beschriebenen Chloralkali-Elektrolyse, bei der Chlorgas produziert wird, kann die resultierende stabile Kalilauge (Kaliumhydroxid-Lösung) bei einer Konzentration von 20–40 % großtechnisch als Elektrolyt für die Wasserstofferzeugung im alkalischen Elektrolyseur zum Einsatz kommen.
In der Mikrosystemtechnik wird Kaliumhydroxid zum selektiven anisotropen Nassätzen von einkristallinem Silicium eingesetzt.
In der Mikrobiologie wird es zur Unterscheidung von grampositiven und gramnegativen Bakterien im Schnelltestverfahren verwendet.
In galvanischen Sauerstoffsensoren wird es als Elektrolyt verwendet. Denselben Zweck erfüllt es auch in den weit verbreiteten Alkali-Mangan-Zellen und den historisch wichtigen Nickel-Cadmium-Akkumulatoren.
In der Lebensmittelindustrie wird es als Säureregulator eingesetzt. Es ist in der EU als Lebensmittelzusatzstoff der Bezeichnung E 525 ohne Höchstmengenbeschränkung (quantum satis) für Lebensmittel allgemein zugelassen.
Es wird zur Herstellung von Kaliumverbindungen, Glas, Farbstoffen, Batterien sowie als Trocknungs- und Absorptionsmittel von Kohlenstoffdioxid verwendet.
Es kann unter starker Erwärmung bestimmte Metalle alkalisch-oxidativ aufschließen.
Bei der Herstellung durch Umesterung von Rapsöl und Methanol zu Biodiesel wird Kalilauge als Katalysator eingesetzt.
Haushalt und Handwerk
BearbeitenKaliumhydroxid wird zur Herstellung weicher Seifen (Schmierseifen) aus verschiedenen pflanzlichen und tierischen Fetten und Ölen sowie in der Waschmittelfabrikation zur Produktion wasserenthärtenden Kaliumphosphats für flüssige Waschmittel benutzt.
Da sich mit Natriumhydroxid hergestellte Seife aufgrund des Natriumchloridgehalts des Salzwassers nicht in Meerwasser löst, werden auch spezielle Salzwasser-Seifen für Seeleute mit Kaliumhydroxid hergestellt.
Kaliumhydroxid verseift auch eingebrannte und verharzte Fette und Öle zu wasserlöslichen Salzen der Fettsäuren und wird darum als Backofenreiniger sowie zum Ablaugen von Lack- und Ölfarben verwendet.
Rohrreinigungsmitteln wird Kaliumhydroxid beigesetzt, da dieses sowohl Haare auflöst, als auch die im Abfluss haftenden Fette verseift, wodurch sie vom Wasser fortgespült werden können. Da Ätzkali jedoch sowohl Acrylglas, als auch emaillierte und glasierte Oberflächen von Wannen und Sanitärkeramik angreift, die aus silikatischem glasartigen Material bestehen (Glaskorrosion), sollte es mit Bedacht eingesetzt werden.[6]
Weblinks
BearbeitenEinzelnachweise
Bearbeiten- ↑ Eintrag zu E 525: Potassium hydroxide in der Europäischen Datenbank für Lebensmittelzusatzstoffe, abgerufen am 27. Juni 2020.
- ↑ Eintrag zu POTASSIUM HYDROXIDE in der CosIng-Datenbank der EU-Kommission, abgerufen am 17. Februar 2020.
- ↑ a b c d e f g h Eintrag zu Kaliumhydroxid in der GESTIS-Stoffdatenbank des IFA, abgerufen am 3. Januar 2023. (JavaScript erforderlich)
- ↑ Eintrag zu Potassium hydroxide im Classification and Labelling Inventory der Europäischen Chemikalienagentur (ECHA), abgerufen am 1. Februar 2016. Hersteller bzw. Inverkehrbringer können die harmonisierte Einstufung und Kennzeichnung erweitern.
- ↑ Schweizerische Unfallversicherungsanstalt (Suva): Grenzwerte – Aktuelle MAK- und BAT-Werte (Suche nach 1310-58-3 bzw. Kaliumhydroxid), abgerufen am 2. November 2015.
- ↑ Prof. Blumes Tipp des Monats August 2004 (Tipp-Nr. 86): Abflussreiniger sind gefährlich, In: Chemieunterricht.de

