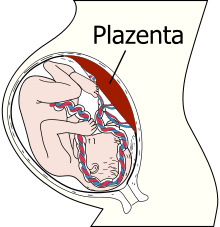
Plazenta
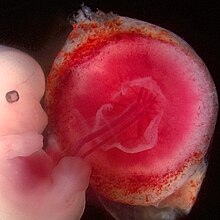
Die Plazenta (lat. placenta ,Kuchen‘, dt. auch Mutterkuchen oder „Fruchtkuchen“) ist ein bei allen weiblichen Höheren Säugetieren (Eutheria) einschließlich des Menschen und mancher Beutelsäuger (Metatheria) während der Trächtigkeit (bzw. Schwangerschaft) sich entwickelndes Gewebe an der Gebärmutterwand, das zum embryonalen Organismus gehört, von diesem gebildet wird und von Blutgefäßen der Mutter und des Embryos durchwoben ist. Darüber steht der Embryo (später der Fötus) mittelbar mit dem Blutkreislauf der Mutter in Verbindung, erhält Nährstoffe und Sauerstoff und gibt Abfallprodukte ab. Nach der Entbindung wird die Plazenta gemeinsam mit der Eihaut als Nachgeburt ausgestoßen. Eine analoge Struktur stellt die Dottersack-Plazenta der Grundhaie dar, die ebenso wie die Plazenta der Säugetiere der Versorgung der Embryonen dient.[1]

Funktionen
BearbeitenDie Plazenta besteht sowohl aus embryonalem bzw. fetalen (Placenta fetalis) als auch aus mütterlichem (Placenta materna) Gewebe. Die Plazenta entsteht, indem embryonales Gewebe in die Gebärmutterschleimhaut (Endometrium bzw. Dezidua) einwächst. Sie stellt die Versorgung mit Nährstoffen, die Entsorgung von Exkretionsprodukten und den Gasaustausch des Embryos bzw. Fötus sicher. Die Verbindung zwischen Embryo und Plazenta erfolgt über die Nabelschnur.
Anders als alle anderen Säugetier-Organe, die erst nach einer ausreichenden Entwicklungs- und Reifungsperiode ihre Funktion aufnehmen, muss die Plazenta ihr eigenes Wachstum steuern und parallel dazu volle Funktionstüchtigkeit entwickeln. Dabei müssen in jedem Stadium der Schwangerschaft die jeweils spezifischen Bedürfnisse des Kindes befriedigt werden. Neben der Versorgung des Kindes erfüllt die Plazenta hormonelle Aufgaben. Noch kaum erforscht ist die Fähigkeit der Plazenta, das Immunsystem der Mutter so zu beeinflussen, dass es zwar funktionstüchtig bleibt und die Mutter damit vor Infektionen schützt, gleichzeitig aber daran gehindert wird, die Plazenta selbst und das Kind als Fremdgewebe abzustoßen.
Aufbau
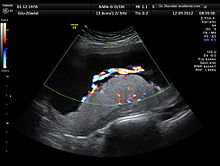
BearbeitenDie menschliche Plazenta ist im ausgereiften Zustand ein circa 500 bis 600 Gramm schweres und im Durchmesser 15 bis 20 Zentimeter großes Organ, das sich nach der Einnistung (Nidation) der Blastozyste in der Gebärmutter bildet. Sie entsteht aus dem fetalen Trophoblasten und aus der mütterlichen Gebärmutterschleimhaut (Endometrium). Die fetale Seite der Plazenta – also Chorionplatte und Nabelschnur – ist mit weißlich trübem Amnionepithel bedeckt (siehe letztes Bild). Zwischen der Chorionplatte und der mütterlichen Basalplatte (Dezidua) befindet sich der mit mütterlichem Blut gefüllte intervillöse Raum. Dieser wird durch bindegewebige Plazentasepten von der Basalplatte aus in 15 bis 20 Felder, die so genannten Kotyledonen, unterteilt. Aus dem Chorion wachsen Primärzotten, die die Sekundärzotten tragen, in diese blutgefüllten Kotyledonen. Durch das Einsprossen von Kapillaren wird die Sekundärzotte zur Tertiärzotte und ist somit zum Stoffaustausch bereit. (In der Abbildung ist der gesamte Zottenbaum als Villus bezeichnet.) Zwischen den Kapillaren der Tertiärzotten und dem intervillösen Raum findet auf Grund der Plazentaschranke (siehe unten) kein Blutaustausch statt. Der Stoffaustausch erfolgt über Diffusion, erleichterte Diffusion, Pinozytose oder wird über Rezeptoren vermittelt. Ab der vierten Schwangerschaftswoche, wenn das Herz des Kindes zu schlagen beginnt, wird die Frucht über die Plazenta versorgt.
Als Organ dient die Plazenta nur eine begrenzte Zeit. Sie zeichnet sich durch den geringsten Gehalt an straffem Bindegewebe aller Organe aus. Außerdem ist die Plazenta nicht mit Nerven durchzogen.
Plazentaschranke
BearbeitenEine der Funktionen der Plazenta ist die Plazentaschranke mit dem vom Trophoblasten abstammenden Synzytiotrophoblast, einer vielkernigen Lage ohne Zellgrenzen (Synzytium).[2] Dies stellt eine passive Filtermembran dar, die mütterliches und kindliches Blut trennt und den Übertritt von verschiedenen im Blut gelösten Substanzen ermöglicht oder verhindert. Die dafür verwendeten Mechanismen sind Diffusion und erleichterte Diffusion, aktiver Transport, Diapedese und Pinozytose. Durch Diffusion gelangen Sauerstoff, Wasser, einige Vitamine, aber auch Alkohol, Gifte, Drogen und Medikamente in den Fötus. Glukose, Aminosäuren und Elektrolyte gelangen über erleichterte Diffusion und aktive Transportprozesse in das Kind. Proteine, Antikörper vom Typ IgG und Fette werden über Pinozytose transportiert. Viren und Bakterien können sich per Diapedese Zugang zum Kind verschaffen. Die Übertragung mütterlicher IgG-Antikörper ist besonders wichtig, da das Kind bis einige Monate nach der Geburt nicht ausreichend eigene Antikörper bilden kann (Nestschutz).
Durch Mikrotraumen in der Plazenta kann es zum Übertritt kindlichen Blutes in den mütterlichen Kreislauf kommen. Dies ist normalerweise ungefährlich, es sei denn, das Kind ist Rhesus-positiv, die Mutter jedoch negativ. In einem solchen Fall kann es zur Sensibilisierung der Mutter gegen kindliche Antigene kommen. Die Mutter bildet Antikörper vom plazentagängigen IgG-Typ gegen das rhesuspositive Blut, welche bei einer Folgeschwangerschaft in den fötalen Kreislauf gelangen und dort das Krankheitsbild des Morbus haemolyticus neonatorum auslösen.
Plazenta als endokrines Organ
BearbeitenDie Plazenta produziert das Hormon Chorion-Gonadotropin und etwa ab dem vierten Monat auch das Gelbkörperhormon Progesteron, nachdem der Gelbkörper im Eierstock die Produktion eingestellt hat. Das Gelbkörperhormon unterdrückt die Regelblutung und ermöglicht somit das Weiterbestehen der Schwangerschaft.
Zudem bildet die Plazenta das humane Plazentalaktogen (HPL). HPL kann ab der 8. Schwangerschaftswoche im Serum der Mutter nachgewiesen werden und nimmt dann bis zur Geburt kontinuierlich um bis zu 2 g täglich zu. Aufgabe von HPL ist es die Brüste zu entwickeln und für die Laktation vorzubereiten. Zudem reguliert es den Metabolismus und hat anabole Effekte.[3]
Plazentaveränderungen
BearbeitenDie Plazenta kann individuell sehr unterschiedlich sein. Form und Größe des Organs variieren ebenso, wie der Ansatz (Insertionsstelle) der Nabelschnur.
Zu den Formvarianten zählen die Placenta succenturiata (Nebenplazenta), die Placenta bilobata/multilobata (zweifach/mehrfach gelappte Plazenta), die Placenta anularis (Ring- oder gürtelförmige Plazenta), die Placenta fenestrata, sowie die Placenta membranacea. Eine Nebenplazenta oder gelappte Plazenta beeinträchtigt die fetale Entwicklung nicht.
Als Folgen einer Plazentationsstörung entstehen Formen, wie die Placenta accreta, die Placenta increta, sowie die Placenta percreta. Dabei wachsen die Zotten durch teilweise oder völlig fehlende Dezidua in das Myometrium ein. Die Folge sind Plazentalösungsstörungen nach der Geburt des Kindes.
Auch Lageveränderungen, wie die unterschiedlichen Formen der Placenta praevia, kommen vor.
Tumoren der Plazenta sind insgesamt sehr selten. Der häufigste ist das Chorangiom.[4][5] Weitere Tumoren können sein: Chorangiomatose, Teratom und Plazentabett-Tumor (Placental site trophoblastic tumor).[6]
Nachgeburt
BearbeitenDie Plazenta mit der Eihaut wird kurz nach der Geburt des Kindes als Nachgeburt geboren.
Oft ist es möglich, die Plazenta ausgehändigt zu bekommen. Kommerzielle Anbieter stellen daraus sog. Globuli (ursprünglich homöopathische Medikamente) her. Manche Menschen vergraben sie in der Erde, meist unter einem Baum. Dieser Brauch war und ist in unterschiedlichsten Regionen der Welt verbreitet.
In China wurde die Plazenta im 16. Jahrhundert gegen Unfruchtbarkeit und Impotenz bei Männern empfohlen.[7] In der zweiten Hälfte des 20. Jahrhunderts wurden Plazenten auch an die Kosmetikindustrie verkauft. Daraus hergestellte Cremes sollten der Hautverjüngung dienen, wissenschaftliche Studien hierzu gibt es keine. Diese Praxis ist unter anderem wegen der Angst vor HIV/AIDS und anderen Infektionen überholt.[8]
Die aus den Plazenten gewonnenen Inhaltsstoffe werden heute aus anderen Quellen oder synthetisch hergestellt bzw. durch alternative Stoffe ersetzt.
Plazentophagie
BearbeitenWährend fast alle sogenannten Plazentatiere ihre Nachgeburt verzehren, ist lediglich von Menschen und Kamelen dokumentiert, dass diese Verhaltensweise bei ihnen nicht die Norm ist.[9]
Doch auch in einigen menschlichen Gesellschaften hat der Verzehr der Plazenta eine lange Geschichte, da diese oft als individuelles Heilmittel im Wochenbett gilt. Sowohl in Nordamerika, als auch in Ozeanien, Europa, Teilen Südamerikas und Asien verzehrt ein Teil der Mütter ihre Plazentas, wobei Forscher feststellen, dass die Zahlen offenbar steigen. In den USA verzehrte 2018 jede dritte Frau, die ihr Kind nicht im Krankenhaus zur Welt brachte ihre eigene Plazenta. Die traditionelle chinesische Medizin verwendet getrocknetes Plazentapulver sowohl zum Anregen der Laktation als auch zur Behandlung von Fruchtbarkeitsstörungen.[10] Während ein Teil der möglichen Risiken noch nicht erforscht ist, konnte nachgewiesen werden, dass die in getrockneter Plazenta enthaltenen Hormone bei 86 Prozent der untersuchten Frauen zu vermehrter Milchbildung führten.[9]
Plazenta kann roh verzehrt, als Brühe oder Sud, zubereitet werden, oder auch als Pulver oder Kapsel eingenommen werden. Im Handel erhältliche Produkte müssen unter bestimmten Hygienemaßnahmen und unter Einhaltung vorgegebener Verarbeitungsschritte erzeugt werden, wobei frische Plazenta innerhalb weniger Stunden nach der Geburt verarbeitet werden muss.[9]
Die Literaturstudie von Cynthia W. Coyle u. a. (Northwestern University Feinberg) von Juni 2015 über Plazentophagie in den Jahren 1950 bis 2014 kommt zum Schluss, dass Nutzen und Risiken erst noch erforscht werden müssen, um fundierte Aussagen treffen zu können.[11][12]
In einer Einzelfallstudie berichten Forscher der US Centers for Disease Control and Prevention (CDC) von einem Kind, das sich mit Streptokokken infizierte, nachdem seine Mutter ihre eigene Plazenta in Form von Kapseln zu sich genommen hatte.[13] Die nachgewiesenen Streptokokken der Gruppe B wurden zwar sowohl im getrockneten Plazentagewebe als auch im Blut des Neugeborenen nachgewiesen, nicht aber in der Muttermilch.[9]
Stammzellgewinnung
BearbeitenInzwischen ist bekannt, dass sowohl aus der Plazenta selbst, der Nabelschnur als auch dem darin befindlichen Nabelschnurblut Nabelschnurblutstammzellen extrahiert werden können. In der Plazenta und Nabelschnur wurden vor allem mesenchymale,[14] im Nabelschnurblut vorrangig blutbildende, also hämatopoetische Stammzellen nachgewiesen. Während die Stammzellen der Nabelschnur derzeit nur zu experimentellen und Forschungszwecken gewonnen werden, können Nabelschnurblutstammzellen routinemäßig gewonnen, konserviert und medizinisch verwendet werden. Häufigstes Verwendungsgebiet war 2001 die Stammzelltransplantation zur Behandlung von Leukämie[15]. Allerdings befindet sich die Forschung zur Anwendung von Nabelschnurblut noch in den Anfängen, speziell in der Regenerativen Medizin und beim Heranzüchten von Gewebe, Knorpeln- und Knochenteile wurden 2013 viele Studien durchgeführt.[16] Fälle, in denen Nabelschnurblut für eine Stammzelltherapie benötigt wird, sind selten. Als Beleg dafür können die Angaben der größten Stammzellenbank Vita 34 herangezogen werden: 30 medizinische Verwendungen bei über 200 000 Einlagerungen. Außerdem ist die Verwendung eigener blutbildender Stammzellen aus Blut oder Knochenmark meist möglich.[17] Ein weiterer Kritikpunkt sind die kurzen Abnabelungszeiten, die im Falle einer Stammzellengewinnung auftreten, und deutlich geringer als die von Seiten der WHO empfohlenen Abnabelungsdauer sind. In diesem Zusammenhang wird oft vom „Auspulsieren“ des Nabelschnurblutes gesprochen, die positiven Effekte dieser Methode sind teilweise bewiesen z. B. eine höhere Eisenmenge im Blut des Säuglings.[18]
Bei Tieren
BearbeitenBei Säugetieren gibt verschiedene Plazentatypen. Kommt es zu einem umfangreichen Abbau der Gebärmutterschleimhaut, spricht man von einer Vollplazenta (Placenta vera). Dies ist bei Primaten, Nagetieren und Raubtieren der Fall. Nach Verteilung der Kontaktstellen unterteilt man diese in die Gürtelplazenta (Placenta zonaria, histologisch: endotheliochorial, das Chorion hat mit den mütterlichen Endothelzellen Kontakt) bei Raubtieren und die Scheibenplazenta (Placenta discoidalis, histologisch: hämochorial, direkter Kontakt mit dem Blut der Mutter) bei Nagetieren und Primaten.[19]
Unterbleibt dieser umfangreiche Abbau der Gebärmutterschleimhaut, spricht man von einer Halbplazenta (Semiplacenta). Bei Unpaarhufern und Walen sind die Kontaktstellen gleichmäßig verteilt (Placenta diffusa, histologisch: epitheliochorial, also das Chorion steht mit dem Epithel der Gebärmutterschleimhaut in Kontakt), bei Schweinen nicht über die gesamte Kontaktfläche (Placenta diffusa incompleta, histologisch ebenfalls epitheliochorial) und bei Wiederkäuern an lokal erhabenen drüsenlosen Kontaktflächen, den Karunkeln (Placenta multiplex s. cotyledonaria).[19]
Beuteltiere besitzen eine unvollkommene Dottersackplazenta, da sie nur eine geringe Tragezeit von 8 bis 40 Tagen haben.
Von über 4.000 Säugetierarten ist bekannt, dass sie ihre eigene Plazenta verzehren.[9] Darunter sind auch zahlreiche Tiere, die sonst selbst rein vegetarisch oder vegan leben. Für den Verzehr der Nachgeburt werden unterschiedliche Gründe angegeben, zu denen der Schutz des Jungtieres vor Raubtieren zählt, da diese die Duftspur wahrnehmen könnten oder auch Versorgung mit Mineralstoffen, Vitaminen und anderen wichtigen Nährstoffen, deren Verfügbarkeit in der freien Natur begrenzt ist.
Evolution der Plazenta
BearbeitenDie Plazenta ist eine Schlüsselinnovation der Säugetiere (Evolution der Säugetiere), von ihren Anfängen bis heute. Sie stellt ein neues Organ dar, das es bei den eierlegenden Tieren davor nicht gab. Neben der Innovation der Muttermilch, der Milchdrüse und der Mutterbindung musste eine Ernährungsverbindung vom Ei des Embryos im Mutterleib zur Mutter evolvieren, um das Wachstum des Embryos im Mutterleib zu ermöglichen. Dieses Wachstum war ein entscheidender selektiver Vorteil. Die Plazenta steigerte die Überlebenschancen des Ungeborenen in der Zeit der Dinosaurier vor etwa 160 Millionen Jahren.
Als wichtiges Gen für die Ausbildung der Plazenta wurde das Gen Paternally expressed gene Peg10 identifiziert. Dieses Gen wurde wahrscheinlich durch ein Retrovirus in die DNA der Keimzellen früher Säuger kodiert,[20] eine virale Invasion und ein Prozess vergleichbar dem, der beim rezenten Koala mit dem krankheitserregenden KoRV-Gen beobachtet wurde. Ein Gen-Knockout von Peg10 bei der Maus im Labor führt zum Stillstand des Wachstums der Plazenta und zum frühen Tod des Embryos.[21]
Peg10 ist also dafür verantwortlich, die Plazenta zu bilden. Das Gen unterbindet die Immunabwehr der Mutter und verhindert damit, dass der Embryo beim Aufbau der physischen Mutter-Kind-Verbindung wieder abgestoßen wird. Erst für den weiteren Verlauf der Evolution wird angenommen, dass die Nahrungsversorgung des Embryos mittels der Plazenta zum Immunabwehrschutz hinzukam. Im Verlauf der Evolution wurde die Plazenta größer, die Tragezeit des Embryos konnte verlängert werden. Eine längere Schwangerschaft war hilfreich für die Unabhängigkeit der Mutter vor Fressfeinden, und Tiere begannen, lebende Säuger auszutragen.
Für die Bildung des Synzytiotrophoblasten ist das env-Gen des endogenen Retrovirus HERV-W verantwortlich. Dieses und weitere beteiligte ERVs müssen die gemeinsamen Vorfahren der Höheren Säugetiere erworben haben, da sie Beuteltieren und Kloakentieren (eierlegenden Säugetieren) fehlen.[22] Insbesondere ist das Protein Syncytin (Syncytin 1 und 2) viralen Ursprungs.[23][24][25][26][27]
Literatur
Bearbeiten- Lois Jovanovic, Genell J. Subak-Sharpe: Hormone. Das medizinische Handbuch für Frauen. (Originalausgabe: Hormones. The Woman’s Answerbook. Atheneum, New York 1987) Aus dem Amerikanischen von Margaret Auer, Kabel, Hamburg 1989, ISBN 3-8225-0100-X, S. 177 f., 383 f. und öfter.
- Andrea Stiefel, Karin Brendel, Nicole H. Bauer et al.: Hebammenkunde, Lehrbuch für Schwangerschaft, Geburt, Wochenbett und Beruf. Hrsg.: Andrea Stiefel, Karin Brendel, Nicole H. Bauer et al. 6. Auflage. Georg Thieme Verlag, Stuttgart 2020, ISBN 978-3-13-240450-2, S. 1141.
- Fritz Strauss: Kurzgeschichte der Placentarforschung. In: Gesnerus 45 (1988) 381-410.
Weblinks
BearbeitenEinzelnachweise
Bearbeiten- ↑ Leonard Compagno, Marc Dando, Sarah Fowler: Sharks of the World. Princeton Field Guides, Princeton University Press, Princeton/ Oxford 2005, ISBN 0-691-12072-2, S. 335.
- ↑ Synzytiotrophoblast, auf: DocCheck Flexikon
- ↑ Klaus Diedrich u. a. (Hrsg.): Gynäkologie und Geburtshilfe. 2., völlig neu bearb. Auflage. Springer, Heidelberg 2007, ISBN 978-3-540-32867-4.
- ↑ Kurt Benirschke, Shirley G. Driscoll: Tumors of the Placenta. In: Springer eBooks. 1967, S. 477–526 doi:10.1007/978-1-4612-9809-0_14.
- ↑ A. Kirkpatrick, Daniel J. Podberesky, Anne E. Gray, Joseph H. Mcdermott: Placental Chorioangioma. In: Radiographics. 2007, Band 27, Nummer 4, S. 1187–1190 doi:10.1148/rg.274065207.
- ↑ Radiopaedia
- ↑ Studienüberblick: Nein, Sie müssen Ihre Plazenta nicht essen. Auf: Spiegel Online, 8. Juni 2015.
- ↑ Franziska Zoidl: Umstritten: Lasagne mit Mutterkuchen. In: Der Standard. 19. Juni 2015.
- ↑ a b c d e Sophia K. Johnson, Jana Pastuschek, Jürgen Rödel, Udo R. Markert, Tanja Groten: Mutterkuchen – mal versuchen? Humane maternale Plazentophagie: möglicher Nutzen und potenzielle Risiken doi:10.1055/a-0674-6275 Thieme Verlag, abgerufen am 12. Dezember 2023
- ↑ R. Botelle & C. Willott (2020): Birth, attitudes and placentophagy: a thematic discourse analysis of discussions on UK parenting forums. BMC Pregnancy & Childbirth, 14712393, 3/6/2020, Bd./Jhrg. 20, Ausgabe 1 doi:10.1186/s12884-020-2824-3
- ↑ Christina Hucklenbroich: Geburtsmedizin: Der Verzehr der Plazenta – ein neuer Trend? faz.net vom 15. Juli 2015, abgerufen am 2. September 2015.
- ↑ Cynthia W. Coyle u. a.: Placentophagy: therapeutic miracle or myth? In: Archives of Women's Mental Health. 4. Juni 2015, abgerufen am 2. September 2015.
- ↑ Genevieve L. Buser, Sayonara Mató, Alexia Y. Zhang, Ben J. Metcalf, Bernard Beall: Notes from the Field: Late-Onset Infant Group B Streptococcus Infection Associated with Maternal Consumption of Capsules Containing Dehydrated Placenta — Oregon, 2016. In: MMWR. Morbidity and Mortality Weekly Report. Band 66, Nr. 25, 2017, ISSN 0149-2195, S. 677–678, doi:10.15585/mmwr.mm6625a4 (cdc.gov [abgerufen am 29. Juli 2017]).
- ↑ V. Lechner u. a.: Isolierung mesenchymaler Stammzellen aus der humanen Nabelschnur als Grundlage für eine autologe Stammzelltherapie in der Kinderchirurgie. German Medical Science GMS Publishing House, 2007. Doc 07dgch6655 (egms.de)
- ↑ H.-D. Peters, R. Kath: Neue therapeutisch aktive monoklonale Antikörper gegen Leukämien und Lymphome. In: Der Onkologe. Band 7, Nr. 2, 19. Februar 2001, ISSN 0947-8965, S. 196–199, doi:10.1007/s007610170158 (springer.com [abgerufen am 19. September 2018]).
- ↑ Werner Müller: Therapie mit Stammzellen. In: Biologie in unserer Zeit. Band 43, Nr. 1, Februar 2013, ISSN 0045-205X, S. 40–45, doi:10.1002/biuz.201310499 (wiley.com [abgerufen am 19. September 2018]).
- ↑ Veronika Szentpetery : Geschäft mit der Angst. auf: heise.de
- ↑ Susan J. McDonald, Philippa Middleton, Therese Dowswell, Peter S. Morris: Effect of timing of umbilical cord clamping of term infants on maternal and neonatal outcomes. In: Cochrane Database of Systematic Reviews. Nr. 7, 2013, ISSN 1465-1858, doi:10.1002/14651858.CD004074.pub3 (cochranelibrary.com [abgerufen am 19. September 2018]).
- ↑ a b Monika Kressin, Bertram Schnorr: Embryologie der Haustiere. 5. Auflage. Enke-Verlag, Stuttgart 2006, ISBN 3-8304-1061-1.
- ↑ Ryuichi Onoa, Shin Kobayashi, Hirotaka Wagatsuma, Kohzo Aisaka, Takashi Kohda, Tomoko Kaneko-Ishino, Fumitoshi Ishino: A Retrotransposon-Derived Gene, Peg10, Is a Novel Imprinted Gene Located on Human Chromosome 7q21. In: Genomics. Band. 73, Nr. 2, 15. April 2001, S. 232–237.
- ↑ Ryuichi Ono, Kenji Nakamura, Kimiko Inoue, Mie Naruse, Takako Usami, Noriko Wakisaka-Saito, Toshiaki Hino, Rika Suzuki-Migishima, Narumi Ogonuki, Hiromi Miki, Takashi Kohda, Atsuo Ogura, Minesuke Yokoyama, Tomoko Kaneko-Ishino, Fumitoshi Ishino: Deletion of Peg10, an imprinted gene acquired from a retrotransposon, causes early embryonic lethality. In: Nature Genetics. Band 38, 2006, S. 101–106.
- ↑ Nadja Podbregar: Geheime Helfer – Welche Funktion haben endogene Retroviren in uns? auf: scinexx.de vom 5. November 2010.
- ↑ Henning Engeln: Die gute Seite der Viren. auf: Spektrum.de, 16. April 2020.
- ↑ A. Dupressoir, C. Lavialle, T. Heidmann: From ancestral infectious retroviruses to bona fide cellular genes: role of the captured syncytins in placentation. In: Placenta. Band 33, Nr. 9, September 2012, S. 663–671, doi:10.1016/j.placenta.2012.05.005, PMID 22695103.
- ↑ B. Soygur, L. Sati: The role of syncytins in human reproduction and reproductive organ cancers. In: Reproduction (Cambridge, England). Band 152, Nr. 5, 2016, S. R167–R178, doi:10.1530/REP-16-0031, PMID 27486264.
- ↑ E. V. Koonin: Viruses and mobile elements as drivers of evolutionary transitions. In: Philosophical transactions of the Royal Society of London. Series B, Biological sciences. Band 371, Nummer 1701, 08 2016, S. , doi:10.1098/rstb.2015.0442. PMID 27431520, PMC 4958936 (freier Volltext) (Review).
- ↑ S. Mi, X. Lee, X. Li, G. M. Veldman, H. Finnerty, L. Racie, E. LaVallie, X. Y. Tang, P. Edouard, S. Howes, J. C. Keith Jr, J. M. McCoy: Syncytin is a captive retroviral envelope protein involved in human placental morphogenesis. In: Nature. Band 403, Nr. 6771, 17. Februar 2000, S. 785–789, doi:10.1038/35001608. PMID 10693809.