α-Galactosidase A
α-Galactosidase A (auch Melibidase) ist ein Enzym, das die Hydrolyse der glycosidischen Bindung von α-Galactopyranosiden katalysiert. Es kommt in allen Eukaryoten vor und ist je nach Aufgabe und Organismus unterschiedlich spezifisch. So können einige α-Galactosidasen auch α-D-Fucopyranoside hydrolysieren. Das Enzym kommt in Zellen in den Lysosomen vor.
| Α-Galactosidase A | ||
|---|---|---|
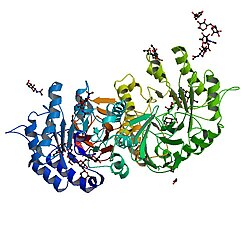
| ||
|
Vorhandene Strukturdaten: 1R46, 1R47, 3GXN, 3GXP, 3GXT, 3HG2, 3HG3, 3HG4, 3HG5, 3LX9, 3LXA, 3LXB, 3LXC, 3S5Y, 3S5Z, 3TV8, 4NXS | ||
| Eigenschaften des menschlichen Proteins | ||
| Masse/Länge Primärstruktur | 48,7 Kilodalton / 429 Aminosäuren | |
| Sekundär- bis Quartärstruktur | Homodimer | |
| Bezeichner | ||
| Gen-Namen | GLA ; GALA | |
| Externe IDs | ||
| Arzneistoffangaben | ||
| ATC-Code | A16AB03 | |
| DrugBank | DB00103 | |
| Wirkstoffklasse | Enzym | |
| Enzymklassifikation | ||
| EC, Kategorie | 3.2.1.22, Glycosidase | |
| Reaktionsart | Hydrolytische Abspaltung von endständigen α-D-Galactoseresten | |
| Substrat | Galactosehaltige Oligo- und Polysaccharide | |
| Vorkommen | ||
| Homologie-Familie | alpha-Galactosidase Precursor | |
| Übergeordnetes Taxon | Eukaryoten | |
| Orthologe | ||
| Mensch | Hausmaus | |
| Entrez | 2717 | 11605 |
| Ensembl | ENSG00000102393 | ENSMUSG00000031266 |
| UniProt | P06280 | |
| Refseq (mRNA) | NM_000169 | NM_013463 |
| Refseq (Protein) | NP_000160 | NP_038491 |
| Genlocus | Chr X: 101.4 – 101.41 Mb | Chr X: 134.59 – 134.6 Mb |
| PubMed-Suche | 2717 | 11605
|
Krankheiten
BearbeitenIst das Enzym nicht ausreichend vorhanden, kommt es zu einer Anreicherung der Glycosphingolipide, was schließlich zum Tod der Zelle führt. Ist der Mangel an α-Galactosidase durch einen Genfehler bedingt, spricht man vom Krankheitsbild des Morbus Fabry. Dies ist eine X-chromosomal vererbte Stoffwechselkrankheit, bei der ein organismusweiter Mangel des Enzyms auftritt.
Expression
BearbeitenDas GLA-Gen besteht aus insgesamt etwa 12.000 Basenpaaren.[1] Sieben Exons mit 1290 Basenpaaren kodieren für das Genprodukt α-Galactosidase A.[2] Deren Präkursor-Protein besteht aus 429 Aminosäuren. Durch posttranslationale Modifikation entsteht das Glycoprotein α-Galactosidase A mit 370 Aminosäuren und einer molaren Masse von 41,4 kDa.[3] Das Homodimer wird wie alle lysosomalen Enzyme cotranslational, das heißt während der Übersetzung der mRNA in die Aminosäuresequenz, mit einem Mannose-6-phosphat-Rest versehen. Ein Teil der phosphorylierten α-Galactosidase-A-Moleküle wird von den Zellen sezerniert und von anderen Zellen über den membranständigen Mannose-6-phosphat-Rezeptor per Endozytose aufgenommen. Die Wiederaufnahme der phosphorylierten α-Galactosidase A über den Mannose-6-phosphat-Rezeptor ist die Grundlage für die Enzymersatztherapie.[4]
Geschichte
BearbeitenIn den frühen 1980er Jahren forschte Goldstein am New York Blood Center als erster an der Technik die Blutgruppe durch Glycosidasen zu ändern.[5] Aus Kaffeebohnen (Coffea canephora) gewonnene α-Galactosidase wurde benutzt, um rote Blutkörperchen der Blutgruppe B zu roten Blutkörperchen der Blutgruppe 0 zu ändern. Im Jahr 2008 wird jedoch von noch erheblichem Forschungsbedarf gesprochen, um diesen Prozess klinisch nutzbar zu machen.[6]
Einzelnachweise
Bearbeiten- ↑ D. F. Bishop, R. Kornreich, R. J. Desnick: Structural organization of the human alpha-galactosidase A gene: further evidence for the absence of a 3' untranslated region. In: PNAS. Band 85, Nummer 11, Juni 1988, S. 3903–3907, PMID 2836863. PMC 280328 (freier Volltext).
- ↑ A. Gal, E. Schäfer, I. Rohard: The genetic basis of Fabry disease. In: A. Mehta, M. Beck, G. Sunder-Plassmann (Hrsg.): Fabry Disease: Perspectives from 5 Years of FOS. Kapitel 33, Oxford PharmaGenesis, 2006, ISBN 1-903539-03-X, PMID 21290673
- ↑ D. H. Calhoun, D. F. Bishop u. a.: Fabry disease: isolation of a cDNA clone encoding human alpha-galactosidase A. In: PNAS. Band 82, Nummer 21, November 1985, S. 7364–7368, PMID 2997789. PMC 391345 (freier Volltext).
- ↑ M. W. King: Introduction to Fabry Disease. Stand: 13. Februar 2011, abgerufen am 1. September 2011
- ↑ Martin L Olsson, Cheryl A Hill, Humberto de la Vega, Qiyong P Liu, Mark R Stroud, Jean Valdinocci, Steven Moon, Henrik Clausen, Margot S Kruskall: Universal red blood cells—enzymatic conversion of blood group A and B antigens. In: Transfusion Clinique et Biologique. Band 11, Nr. 1, Februar 2004, S. 33, doi:10.1016/j.tracli.2003.12.002, PMID 14980547.
- ↑ Martin L. Olsson, Henrik Clausen: Modifying the red cell surface: towards an ABO-universal blood supply. In: British Journal of Haematology. Band 140, Nr. 1, 26. Oktober 2007, S. 3–12, doi:10.1111/j.1365-2141.2007.06839.x, PMID 17970801.