2,4,6-Trichlorbenzoylchlorid
2,4,6-Trichlorbenzoylchlorid (auch bekannt als das Yamaguchi-Reagenz oder kurz TCBC) ist eine dreifach chlorierte aromatische Verbindung aus der Gruppe der Carbonsäurechloride.
| Strukturformel | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
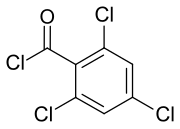
| |||||||||||||||||||
| Allgemeines | |||||||||||||||||||
| Name | 2,4,6-Trichlorbenzoylchlorid | ||||||||||||||||||
| Andere Namen |
| ||||||||||||||||||
| Summenformel | C7H2Cl4O | ||||||||||||||||||
| Kurzbeschreibung |
Gelbe Flüssigkeit[1] | ||||||||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||||||||
| |||||||||||||||||||
| Eigenschaften | |||||||||||||||||||
| Molare Masse | 243,90 g·mol−1 | ||||||||||||||||||
| Aggregatzustand |
flüssig[1] | ||||||||||||||||||
| Dichte |
1,560 g·cm−3 [1] | ||||||||||||||||||
| Schmelzpunkt | |||||||||||||||||||
| Sicherheitshinweise | |||||||||||||||||||
| |||||||||||||||||||
| Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). | |||||||||||||||||||
Darstellung
BearbeitenDie Darstellung von 2,4,6-Trichlorbenzoylchlorid wurde von Masaru Yamaguchi 1979 beschrieben. Dabei wird 2,4,6-Trichloranilin in einer Sandmeyer-Reaktion zu 2,4,6-Trichlorbenzonitril umgesetzt. Durch Hydrolyse des Nitrils erhält man die 2,4,6-Trichlorbenzoesäure, die mit Thionylchlorid zu 2,4,6-Trichlorbenzoylchlorid umgesetzt wird.[2][3]
Alternativ kann 2,4,6-Trichlorbenzoylchlorid durch Reaktion von 1,3,5-Trichlorbenzol mit Butyllithium unter Kohlenstoffdioxid-Atmosphäre und anschließender Umsetzung mit Thionylchlorid dargestellt werden.[4]
Verwendung
Bearbeiten2,4,6-Trichlorbenzoylchlorid findet im Yamaguchi-Verfahren zur Herstellung von Makroliden Anwendung.[5]
Einzelnachweise
Bearbeiten- ↑ a b c d e f 2,4,6-Trichlorobenzoyl chloride. Thermo Fisher, abgerufen am 21. Juni 2023.
- ↑ Reynold C. Fuson, John W. Bertetti, Wm. E. Ross: the Haloform Reaction. Vii. the Effect of Ortho Chlorine Atoms. In: Journal of the American Chemical Society. Band 54, Nr. 11, 1932, S. 4380–4383, doi:10.1021/ja01350a036.
- ↑ Junji Inanaga, Kuniko Hirata, Hiroko Saeki, Tsutomu Katsuki, Masaru Yamaguchi: A Rapid Esterification by Means of Mixed Anhydride and Its Application to Large-ring Lactonization. In: Bulletin of the Chemical Society of Japan. Band 52, Nr. 7, 1979, S. 1989–1993, doi:10.1246/bcsj.52.1989.
- ↑ Tharun Kumar Kotammagari: 2,4,6-Trichlorobenzoyl Chloride (Yamaguchi Reagent). In: Synlett. Band 25, Nr. 09, Juni 2014, S. 1335–1336, doi:10.1055/s-0033-1341245.
- ↑ Masataka Hikota, Youji Sakurai, Kiyoshi Horita, Osamu Yonemitsu: Synthesis of erythronolide a via a very efficient macrolactonization under usual acylation conditions with the Yamaguchi reagent. In: Tetrahedron Letters. Band 31, Nr. 44, Januar 1990, S. 6367–6370, doi:10.1016/S0040-4039(00)97066-7.
