6′-Sialyllactose
6′-Sialyllactose ist ein humanes Milch-Oligosaccharid (HMO). Es ist ein Trisaccharid bestehend aus den Monosacchariden Glucose, Galaktose und Sialinsäure. Ein prominentes Isomer, welches ebenfalls ein HMO ist, ist 3'-Sialyllactose.[2] Nach der EU-Verordnung 2015/2283 zählt das Natriumsalz der 6′-Sialyllactose als neuartiges Lebensmittel.[3][4] Die Zulassung gilt seit dem 17. Februar 2021 und wurde von der dänischen Firma Glycom A/S beantragt. Die EU-Verordnung sieht die Verwendung in milchartigen Getränken für Kleinkinder und als Nahrungsergänzungsmittel vor.
| Strukturformel | |||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
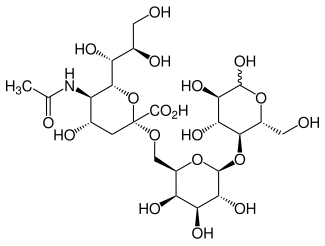
| |||||||||||||
| Allgemeines | |||||||||||||
| Name | 6′-Sialyllactose | ||||||||||||
| Andere Namen |
| ||||||||||||
| Summenformel | C23H39NO19 | ||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||
| |||||||||||||
| Eigenschaften | |||||||||||||
| Molare Masse | |||||||||||||
| Aggregatzustand |
fest[1] | ||||||||||||
| Sicherheitshinweise | |||||||||||||
| |||||||||||||
| Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). | |||||||||||||
Geschichte
BearbeitenDie Entdeckung von 6′-Sialyllactose geht auf die Arbeiten von Richard Kuhn, Reinhard Brossmer, R. E. Trucco und R. Caputto in den 1950er Jahren zurück. Diese isolierten Trisaccharide aus Brustdrüsen von Ratten und aus Kuh-Kolostrum.[5] Aufgrund der damals zur Verfügung stehenden Analysemethoden kann heute nicht mehr eindeutig festgestellt werden, ob die gefundenen Isolate genau die Struktur der 6′-Sialyllactose hatten oder ob etwa die Acetylgruppe an anderer Stelle saß. Die Grundstruktur des Gerüstes war aber zu dieser Zeit schon klar festzustellen. Die erste chemische Synthese von 6′-Sialyllactose wurde 1986 von einer japanischen Arbeitsgruppe veröffentlicht und bedurfte einem großen Aufwand an Schutzgruppen-Chemie. Es wurden vor allem Acetyl-, Benzyl- und Tritylgruppen verwendet.[6] Mittlerweile sind chemoenzymatische Synthesen zur Gewinnung von 6′-Sialyllactose in der Literatur bekannt und von einem chinesischen Institut patentiert.[7][8]
Vorkommen
BearbeitenAuch in Kuhmilch kommt 6′-Sialyllactose vor, allerdings in geringerem Maße als in humaner Milch.[9]
Gewinnung und Darstellung
BearbeitenZu analytischen Zwecken wird 6′-Sialyllactose meist aus Kuhmilch isoliert.[9][1] Zu kommerziellen Zwecken wird es auch fermentativ mittels Escherichia coli K-12 DH1 gewonnen.[10]
Eigenschaften
Bearbeiten6′-Sialyllactose wird unter sauren Bedingungen schnell zu den Bestandteilen Sialinsäure und Lactose hydrolysiert. In neutraler Lösung ist sie Monate stabil. In schwach alkalischer Lösung tritt eine Isomerisierung zu 6′-Sialyllactulose ein. Eine wässrige 6′-Sialyllactose-Lösung ist am längsten stabil, wenn die eingesetzte Substanz aus einer auf pH 5 eingestellten Lösung durch Gefriertrocknung gewonnen wurde.[10]
Einzelnachweise
Bearbeiten- ↑ a b c d Datenblatt 6′-Sialyllactose sodium salt bei Sigma-Aldrich, abgerufen am 4. September 2023 (PDF).
- ↑ Externe Identifikatoren von bzw. Datenbank-Links zu 3'-Sialyllactose: CAS-Nr.: 35890-38-1, PubChem: 123914, ChemSpider: 110445, Wikidata: Q3482888.
- ↑ Verordnung (EU) 2017/2470
- ↑ Verordnung (EU) 2015/2283
- ↑ R. Kuhn, R. Brossmer: Über O-Acetyl-lactaminsäure-lactose aus Kuh-Colostrum und ihre Spaltbarkeit durch Influenza-Virus. In: Chemische Berichte. Band 89, Nr. 9, 1956, S. 2013–2025, doi:10.1002/cber.19560890902.
- ↑ K. Furuhata, K. Anazawa, M. Itoh, Y. Shitori, H. Ogura: Studies on Sialic Acids. V. Synthesis of α-and β-D-Neu5Acp-(2→6)-lactose. In: Chemical and Pharmaceutical Bulletin. Band 34, Nr. 7, 1986, S. 2725–2731, doi:10.1248/cpb.34.2725.
- ↑ Patent EP4052712: ZUCKERKETTE UND ZUSAMMENSETZUNGEN DAVON UND IHRE VERWENDUNG ZUR PRÄVENTION UND/ODER BEHANDLUNG VON CORONAVIRUS-INFEKTIONEN. Angemeldet am 26. Juli 2021, veröffentlicht am 7. September 2022, Anmelder: INST OF PROCESS ENGINEERING CHINESE ACADEMY OF SCIENCES, Erfinder: YUGUANG DU, JIANJUN LI, YUEQIANG XU, ZHUO WANG, DONGDONG LIU, YALU YAN, QI WANG, XIN YOU, XIAOHUI DU.
- ↑ Q. Chao, T. Li, J.-X. Jia, Z. Li, Zijie, P. Peng, X.-D. Gao, N. Wang: Spore-Encapsulating Glycosyltransferase Catalysis Tandem Reactions: Facile Chemoenzymatic Synthesis of Complex Human Glycans. In: ACS Catalysis. Band 12, Nr. 5, 2022, S. 3181–3188, doi:10.1021/acscatal.1c05630.
- ↑ a b V. Kelly, S. Davis, S. Berry, J. Melis, R. Spelman, R. Snell, K. Lehnert, D. Palmer: Rapid, quantitative analysis of 3′-and 6′-sialyllactose in milk by flow-injection analysis–mass spectrometry: Screening of milks for naturally elevated sialyllactose concentration. In: Journal of Dairy Science. Band 96, Nr. 12, 2013, S. 7684–7691, doi:10.3168/jds.2013-6972.
- ↑ a b D. Turck, J. Castenmiller, S. De Henauw, K. I. Hirsch-Ernst, Karen J. Kearney, A. Maciuk, I. Mangelsdorf, H. J. McArdle, A. Naska: Safety of 6′-Sialyllactose (6′-SL) sodium salt as a novel food pursuant to Regulation (EU) 2015/2283. In: EFSA Journal. Band 18, Nr. 5, 2020, S. e06097, doi:10.2903/j.efsa.2020.6097.