| Sulfonsäuren und Sulfonate |
|---|
 Sulfonsäure |
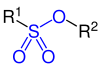 Sulfonsäureester |
 Sulfonsäuresalze |
| R, R1 und R2 sind Organylgruppen. Die funktionellen Gruppen sind blau markiert. |
Sulfonsäuren sind organische Schwefelverbindungen mit der allgemeinen Struktur R–SO2–OH, wobei R ein organischer Rest ist. Ihre Salze und Ester mit der allgemeinen Struktur R–SO2–O− und R1–SO2–O–R2 heißen Sulfonate.
Sulfonsäuren und die ihnen zugehörigen Salze und Ester werden in zwei Gruppen eingeteilt: die aliphatischen Sulfonsäuren bzw. Alkansulfonsäuren oder -sulfonate und die aromatischen Sulfonsäuren bzw. Arensulfonsäuren oder -sulfonate.
Vorkommen
BearbeitenTaurin ist als Aminosulfonsäure eine der wenigen natürlich vorkommenden Sulfonsäuren.
Sekundärmetaboliten
BearbeitenIn den Wurzeln des Stachelbeerbaums (Phyllanthus acidus) wurden sechs Flavonoide mit Sulfonsäurefunktion nachgewiesen.[1] In den Wurzeln des Färberwaids kommen verschiedene Indolalkaloide mit Sulfonsäurefunktionen vor, die teilweise als Glucoside vorliegen. Eine dieser Verbindungen ist Indol-3-methansulfonsäure.[2]
In einem Hornkieselschwamm der Gattung Echinodictyum wurden die Echinosulfonsäure A sowie zwei strukturell verwandte Verbindungen nachgewiesen. Dabei handelt es sich um Verbindungen, die zwei Indol-Einheiten aufweisen.[3] Als Sekundärmetabolit einer Streptomyces-Art aus einer japanischen Boden-Probe ist das Sulfotanon bekannt.[4]
Atmosphärische Vorkommen
BearbeitenMethansulfonsäure kommt in geringen Konzentrationen verbreitet in der Atmosphäre vor. Sie entsteht als Oxidationsprodukt aus flüchtigen Organoschwefelverbindungen marinen Ursprungs, insbesondere Dimethylsulfid.[5] Die atmosphärische Konzentration der Methansulfonsäure liegt in der Größenordnung von 10⁶ bis 10⁷ Molekülen pro Kubikzentimeter und es wird vermutet, dass die Verbindung neben einigen weiteren zur atmosphärischen Aerosolbildung beiträgt.[6]
Gewinnung und Darstellung
BearbeitenRadikalische Reaktionen
BearbeitenEin Gemisch aus Alkansulfonsäuren entsteht durch die Einwirkung von Schwefeldioxid und Sauerstoff auf höhere Alkane in Gegenwart von Radikalbildnern.[7]
Ausgehend von Alkenen können die Natriumsalze von Sulfonsäuren durch radikalische Addition von Natriumhydrogensulfit hergestellt werden.[8]
Oxidationen
BearbeitenAliphatische und aromatische Sulfonsäuren können durch Oxidation von Thiolen (aus Alkylhalogenigen zugänglich) synthetisiert werden, beispielsweise mit Salpetersäure, Kaliumpermanganat oder mit Wasserstoffperoxid in Essigsäure.[7][8]
Eine weitere Methode ausgehend von Alkylhalogeniden ist die Umsetzung zu Thiocyanaten oder Disulfiden und anschließende Oxidation. Weiterhin ist die Addition einer Grignard-Verbindung an Schwefeldioxid und anschließende Oxidation möglich.[8]
Substitution mit Sulfit
BearbeitenDurch nucleophile Substitutionen werden aus Halogenalkanen (insbesondere Bromalkanen) und einem Alkalisulfit (zum Beispiel Natriumsulfit) oder Ammoniumsulfit die entsprechenden Sulfonsäuresalze dargestellt.[7][8]
Aromatische Sulfonsäuren
BearbeitenArensulfonsäuren werden durch die Sulfonierung von Arenen hergestellt. Es findet eine elektrophile aromatische Substitution statt. Das elektrophile Reagens Schwefeltrioxid liegt in konzentrierter Schwefelsäure im Gleichgewicht vor.[7]
Weiter funktionalisierte Sulfonsäuren
BearbeitenPerfluoralkansulfonsäuren werden durch elektrochemische Fluorierung von Alkansulfonsäuren hergestellt. Dabei entsteht zunächst ein Säurefluorid, das durch Hydrolyse die Sulfonsäure ergibt.[8] 1-Hydroxyalkansulfonsäuren entstehen durch Addition von Natriumhydrogensulfit an Aldehyde (Bisulfit-Reaktion). Die Isethionsäure (2-Hydroxyethansulfonsäure) wird durch Reaktion von Ethylenoxid mit Natriumhydrogensulfit gewonnen.[8]
Eigenschaften
BearbeitenAlkansulfonsäuren sind im Allgemeinen viskose Flüssigkeiten, während Arensulfonsäuren hygroskopische Kristalle bilden. Diese lösen sich leicht in Wasser und können durch Natriumchlorid ausgesalzen werden. Einige Sulfonsäuren bilden stabile, kristalline Hydrate.[7] Der Schmelzpunkt von Methansulfonsäure beträgt 20 °C, der von Ethansulfonsäure −17 °C, die Schmelzpunkte der in der homologen Reihe folgenden Vertreter, Propansulfonsäure bis Hexansulfonsäure liegen zwischen diesen beiden Werten.[8]
Sulfonsäuren sind deutlich stärkere Säuren als Carbonsäuren und weisen in der Regel negative pKs-Werte auf. Die starke Säurewirkung beruht auf der Stabilität der korrespondierenden Base, des Sulfonatanions. Durch die gleichmäßige Delokalisierung der negativen Ladung auf die drei äquivalenten Sauerstoffe ist das Anion stark mesomeriestabilisiert. Trifluormethansulfonsäure ist sogar stärker sauer als Perchlorsäure und gehört damit zu der Gruppe der Supersäuren.[9] Die Vertreter der homologen Reihe einfacher Sulfonsäuren von Methansulfonsäure bis einschließlich Heptansulfonsäure sind in Wasser vollständig dissoziiert. Auch Benzolsulfonsäure und para-Toluolsulfonsäure sind starke Säuren. Die einfachste Disulfonsäure, Methandisulfonsäure, weist eine mit Schwefelsäure vergleichbare Säurestärke auf.[8]
Reaktionen
BearbeitenNucleophile Substitution
BearbeitenArensulfonate können bei Temperaturen von 200 bis 300 °C durch eine nucleophile Substitution in Amine, Phenole, Carbonsäuren oder Nitrile umgewandelt werden.[7]
Salzbildung
BearbeitenSulfonsäuren sind wie Schwefelsäure starke Säuren, die mit Metallhydroxiden Salze bilden. Im Gegensatz zu den entsprechenden Sulfaten (Salze der Schwefelsäure) lösen sich aber Calcium-, Barium- und Blei(II)-sulfonate gut in Wasser.[7]
Desulfonierung von Arensulfonsäuren
BearbeitenDie Sulfonierung von Arenen zur Herstellung von Arensulfonsäuren ist eine reversible Reaktion. Die bei der Herstellung angegebene Benzolsulfonsäure wird beispielsweise durch verdünnte Salzsäure bei Temperaturen von 150 bis 200 °C zu Benzol hydrolysiert:[7]
Verwendung
BearbeitenFarbstoffe
BearbeitenAuch viele Farbstoffe tragen Sulfonatgruppen, um eine hohe Wasserlöslichkeit zu erreichen.
Tenside
BearbeitenNatriumsalze der Sulfonsäurederivate werden oft als anionische Tenside in Reinigungsmitteln eingesetzt.[10] Von den Alkylbenzolsulfonaten (ABS) mit der allgemeinen Formel CnH2n+1–C6H4–SO3− Na+ war der wichtigste Vertreter bis in die 1960er-Jahre das Tetrapropylenbenzolsulfonat (TBS). Es hatte in den 1950er-Jahren die Seife als Tensid weitgehend verdrängt. TBS wird allerdings (wie viele Vertreter der stark verzweigten ABS) im Abwasser nur schlecht abgebaut, was u. a. zu Schaumbergen auf Flüssen führte. Deshalb wurde es ab 1964 durch sogenannte lineare Alkylbenzolsulfonate (LAS) abgelöst, die seitdem die wichtigsten Tenside in der Waschmittelchemie sind. Praktisch handelt es sich dabei häufig um sekundäre Alkylbenzolsulfonate, eines der am meisten verwendeten ist Natriumdodecylbenzolsulfonat. Weitere sind lineare (sekundäre) Alkylsulfonate (SAS).
-
Tetrapropylenbenzolsulfonat (TBS)
-
Natriumdodecylbenzolsulfonat, Beispiel aus dem Isomerengemisch.
-
p-Toluolsulfonsäure ist ein wichtiges Reagenz in der organischen Synthese.
Chemische Synthese und Analytik
BearbeitenKurzkettige Alkansulfonsäuren weisen eine große Säurestärke auf ohne oxidierend zu wirken. Insbesondere Methansulfonsäure wird daher als saurer Katalysator eingesetzt, beispielsweise für Veresterungen, Polymerisationen und für die Umsetzung von Carbonsäuren mit Wasserstoffperoxid zu Peroxycarbonsäuren.[8]
Ein wichtiges chemisches Intermediat ist die Isethionsäure. Sie dient zur industriellen Synthese von Taurin, N-Methyltaurin und von Tensiden (Isethionate). Weitere industriell wichtige Vertreter sind das Natriumhydroxymethansulfonat, das sich von der Hydroxymethansulfonsäure ableitet, sowie die Vinylsulfonsäure, die als Alkylierungsmittel eingesetzt und polymerisiert werden kann.[8]
Medizin
BearbeitenDes Weiteren sind Sulfonsäuren und ihre Derivate in Gerbstoffen und Arzneimitteln enthalten.[7]
Weitere Verwendungen
BearbeitenEine spezielle Anwendung finden Polymere mit Sulfonatgruppen bei der Wasseraufbereitung, wo sie in Ionenaustauschern für Kationen eingesetzt werden.
Weblinks
BearbeitenEinzelnachweise
Bearbeiten- ↑ Thuc-Huy Duong, Mehdi A. Beniddir, Van-Kieu Nguyen, Thammarat Aree, Jean-François Gallard, Dinh-Hung Mac, Huu-Hung Nguyen, Xuan-Hao Bui, Joël Boustie, Kim-Phi-Phung Nguyen, Warinthorn Chavasiri, Pierre Le Pogam: Sulfonic Acid-Containing Flavonoids from the Roots of Phyllanthus acidus. In: Journal of Natural Products. Band 81, Nr. 9, 28. September 2018, S. 2026–2031, doi:10.1021/acs.jnatprod.8b00322.
- ↑ Lingjie Meng, Qinglan Guo, Yufeng Liu, Minghua Chen, Yuhuan Li, Jiandong Jiang, Jiangong Shi: Indole alkaloid sulfonic acids from an aqueous extract of Isatis indigotica roots and their antiviral activity. In: Acta Pharmaceutica Sinica B. Band 7, Nr. 3, Mai 2017, S. 334–341, doi:10.1016/j.apsb.2017.04.003, PMID 28540170, PMC 5430897 (freier Volltext).
- ↑ Simon P. B. Ovenden, Robert J. Capon: Echinosulfonic Acids A−C and Echinosulfone A: Novel Bromoindole Sulfonic Acids and a Sulfone from a Southern Australian Marine Sponge, Echinodictyum. In: Journal of Natural Products. Band 62, Nr. 9, 1. September 1999, S. 1246–1249, doi:10.1021/np9901027.
- ↑ Mohamed S. Abdelfattah, Naoki Ishikawa, Utpal K. Karmakar, Masami Ishibashi: Sulfotanone, a new alkyl sulfonic acid derivative from Streptomyces sp. IFM 11694 with TRAIL resistance-overcoming activity. In: Journal of Natural Medicines. Band 70, Nr. 2, April 2016, S. 266–270, doi:10.1007/s11418-015-0951-3.
- ↑ E. S. Saltzman, D. L. Savoie, R. G. Zika, J. M. Prospero: Methane sulfonic acid in the marine atmosphere. In: Journal of Geophysical Research: Oceans. Band 88, C15, 20. Dezember 1983, S. 10897–10902, doi:10.1029/JC088iC15p10897.
- ↑ Hailiang Zhao, Xiaotong Jiang, Lin Du: Contribution of methane sulfonic acid to new particle formation in the atmosphere. In: Chemosphere. Band 174, Mai 2017, S. 689–699, doi:10.1016/j.chemosphere.2017.02.040.
- ↑ a b c d e f g h i Siegfried Hauptmann: Organische Chemie. Deutscher Verlag für Grundstoffindustrie, 1985, ISBN 3-87144-902-4, S. 480–482.
- ↑ a b c d e f g h i j Kurt Kosswig: Sulfonic Acids, Aliphatic. In: Ullmann's Encyclopedia of Industrial Chemistry. Wiley-VCH Verlag GmbH & Co. KGaA, Weinheim, Germany 2000, ISBN 978-3-527-30673-2, doi:10.1002/14356007.a25_503.
- ↑ Hans Beyer: Lehrbuch der Organische Chemie. S. Hirzel Verlag, Stuttgart/ Leipzig 1998, ISBN 3-7776-0808-4, S. 158–160.
- ↑ Joachim Buddrus: Grundlagen der Organischen Chemie. 4. Auflage. de Gruyter Verlag, Berlin 2011, ISBN 978-3-11-024894-4, S. 97.