Aluminiumcarbid
Aluminiumcarbid ist eine anorganische chemische Verbindung aus der Gruppe der Carbide; hier zählt es zu den Methaniden (C4−), da es formal vom Methan abgeleitet ist. Es besteht aus den Elementen Aluminium und Kohlenstoff.
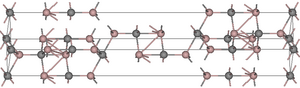
| Kristallstruktur | ||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| ||||||||||||||||
| _ Al3+ _ C4− | ||||||||||||||||
| Allgemeines | ||||||||||||||||
| Name | Aluminiumcarbid | |||||||||||||||
| Verhältnisformel | Al4C3 | |||||||||||||||
| Kurzbeschreibung |
farblose Kristalle[1] | |||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||
| ||||||||||||||||
| Eigenschaften | ||||||||||||||||
| Molare Masse | 143,96 g·mol−1 | |||||||||||||||
| Aggregatzustand |
fest | |||||||||||||||
| Dichte |
2,36 g·cm−3[2] | |||||||||||||||
| Schmelzpunkt | ||||||||||||||||
| Siedepunkt |
Zersetzung >2200 °C[2] | |||||||||||||||
| Löslichkeit |
in Wasser heftige Zersetzung[2] | |||||||||||||||
| Sicherheitshinweise | ||||||||||||||||
| ||||||||||||||||
| Thermodynamische Eigenschaften | ||||||||||||||||
| ΔHf0 |
−209 kJ·mol−1[3] | |||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). | ||||||||||||||||
Geschichte
BearbeitenDie Verbindung wurde erstmals im Jahr 1855 vom französischen Chemiker Henri Étienne Sainte-Claire Deville beschrieben.[4][5] Der französische Chemiker Henri Moissan stellte es 1897 durch das Zusammenschmelzen von Tonerde und Calciumcarbid im elektrischen Ofen her.[6]
Synthese
BearbeitenDie Herstellung von Aluminiumcarbid erfolgt im elektrischen Ofen in Wasserstoffatmosphäre bei 2000 °C aus den Elementen. Durch Verunreinigung mit verbleibendem Aluminium ist das Reaktionsprodukt gelblich bis orange gefärbt. Außerdem kann es bei 1100 °C aus den Elementen in Anwesenheit von Terpentin erzeugt werden.[7]
Eigenschaften
BearbeitenEs bildet farblose bis hellgelbe, hexagonale Kristalle (a = 3,325, c = 24,94 Å) und schmilzt bei einer Temperatur von 2100 °C. Oberhalb von 2200 °C ist es nicht mehr stabil und zersetzt sich.[7]
Aufgrund seines Charakters als salzartiges Carbid reagiert Aluminiumcarbid mit Säuren zu Methan und Aluminiumsalzlösungen.
Aluminiumcarbid ist neben Berylliumcarbid das einzige Carbid, das mit Wasser unter Bildung von Methan reagiert.[1]
Weblinks
Bearbeiten- Eintrag im Omikron Chemie-Lexikon ( vom 7. Mai 2012 im Internet Archive)
Einzelnachweise
Bearbeiten- ↑ a b Eintrag zu Aluminiumcarbid. In: Römpp Online. Georg Thieme Verlag, abgerufen am 6. März 2014.
- ↑ a b c d e f Eintrag zu Aluminiumcarbid in der GESTIS-Stoffdatenbank des IFA, abgerufen am 8. Januar 2021. (JavaScript erforderlich)
- ↑ PAETEC Formelsammlung Ausgabe 2003, Seite 116.
- ↑ Rolf Werner Soukup: Chemiegeschichtliche Daten anorganischer Substanzen, Version 2020, S. 6 pdf.
- ↑ H. É. Sainte-Claire Deville: Recherches sur les métaux, et en particulier sur l'aluminium. et sur une nouvelle forme du silicium in Ann. Chim. Phys. 43 (1855) 15.
- ↑ H. Moissan: Nouvelle méthode de préparation des carbures par l'action du carbure de calcium sur les oxydes in Compt. Rend. 125 (1897) 840.
- ↑ a b Georg Brauer (Hrsg.), unter Mitarbeit von Marianne Baudler u. a.: Handbuch der Präparativen Anorganischen Chemie. 3., umgearbeitete Auflage. Band II, Ferdinand Enke, Stuttgart 1978, ISBN 3-432-87813-3, S. 841.

