Berkelium(III)-fluorid
Berkelium(III)-fluorid ist eine chemische Verbindung bestehend aus den Elementen Berkelium und Fluor. Es besitzt die Formel BkF3 und gehört zur Stoffklasse der Fluoride.
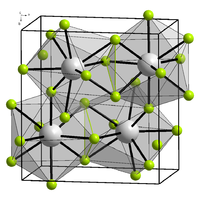
| Kristallstruktur | |||||||
|---|---|---|---|---|---|---|---|
| |||||||
| _ Bk3+ _ F− | |||||||
| Kristallsystem | |||||||
| Gitterparameter |
a = 670 pm | ||||||
| Koordinationszahlen |
Bk[9], F[3] | ||||||
| Allgemeines | |||||||
| Name | Berkelium(III)-fluorid | ||||||
| Andere Namen |
Berkeliumtrifluorid | ||||||
| Verhältnisformel | BkF3 | ||||||
| Kurzbeschreibung |
gelbgrüner Feststoff[1] | ||||||
| Externe Identifikatoren/Datenbanken | |||||||
| |||||||
| Eigenschaften | |||||||
| Molare Masse | 304,07 g·mol−1 | ||||||
| Aggregatzustand |
fest | ||||||
| Dichte |
9,70 g·cm−3[2] | ||||||
| Gefahren- und Sicherheitshinweise | |||||||
 Radioaktiv | |||||||
| |||||||
| Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). | |||||||
Eigenschaften
BearbeitenBerkelium(III)-fluorid ist ein gelbgrüner Feststoff und besitzt zwei kristalline Strukturen, die temperaturabhängig sind. Bei niedrigen Temperaturen ist die orthorhombische Struktur (YF3-Typ) zu finden mit a = 670 pm, b = 709 pm und c = 441 pm sowie einer Dichte von 9,70 g·cm−3. Bei höheren Temperaturen bildet es ein trigonales System (LaF3-Typ) mit a = 697 pm und c = 714 pm sowie einer Dichte von 10,15 g·cm−3. Hierbei ist jeder Berkeliumkern von neun Fluorkernen in einer verzerrten dreifach-überkappten trigonal-prismatischen Struktur umgeben. Die Umwandlungstemperatur des BkF3 liegt im Bereich von 350 bis 600 °C.[2][4][5]
Verwendung
BearbeitenDie ersten Proben von Berkeliummetall wurden 1969 durch Reduktion von BkF3 bei 1000 °C mit Lithium in Reaktionsapparaturen aus Tantal hergestellt.[6]
Sicherheitshinweise
BearbeitenEinstufungen nach der CLP-Verordnung liegen nicht vor, weil diese nur die chemische Gefährlichkeit umfassen und eine völlig untergeordnete Rolle gegenüber den auf der Radioaktivität beruhenden Gefahren spielen. Auch Letzteres gilt nur, wenn es sich um eine dafür relevante Stoffmenge handelt.
Einzelnachweise
Bearbeiten- ↑ Berkelium(III)-fluorid bei www.webelements.com.
- ↑ a b J. R. Peterson, B. B. Cunningham: Crystal Structures and Lattice Parameters of the Compounds of Berkelium IV. Berkelium Trifluoride, in: J. Inorg. Nucl. Chem., 1968, 30 (7), S. 1775–1784 (doi:10.1016/0022-1902(68)80353-7).
- ↑ Die von der Radioaktivität ausgehenden Gefahren gehören nicht zu den einzustufenden Eigenschaften nach der GHS-Kennzeichnung. In Bezug auf weitere Gefahren wurde dieser Stoff entweder noch nicht eingestuft oder eine verlässliche und zitierfähige Quelle hierzu wurde noch nicht gefunden.
- ↑ D. D. Ensor, J. R. Peterson, R. G. Haire, J. P. Young: Absorption Spectrophotometric Study of Berkelium(III) and (IV) Fluorides in the Solid State, in: J. Inorg. Nucl. Chem., 1981, 43 (5), S. 1001–1003 (doi:10.1016/0022-1902(81)80164-9).
- ↑ Joseph Richard Peterson: The Solution Absorption Spectrum of Bk3+ and the Crystallography of Berkelium Dioxide, Sesquioxide, Trichloride, Oxychloride, and Trifluoride, Ph.D. Thesis, October 1967, U. S. Atomic Energy Commission Document Number UCRL-17875 (1967).
- ↑ J. R. Peterson, J. A. Fahey, R. D. Baybarz: The Crystal Structures and Lattice Parameters of Berkelium Metal, in: J. Inorg. Nucl. Chem., 1971, 33 (10), S. 3345–3351 (doi:10.1016/0022-1902(71)80656-5).
Literatur
Bearbeiten- David E. Hobart, Joseph R. Peterson: Berkelium, in: Lester R. Morss, Norman M. Edelstein, Jean Fuger (Hrsg.): The Chemistry of the Actinide and Transactinide Elements, Springer, Dordrecht 2006; ISBN 1-4020-3555-1, S. 1444–1498 (doi:10.1007/1-4020-3598-5_10).