Bortribromid
Bortribromid ist eine chemische Verbindung bestehend aus den Elementen Bor und Brom mit der Summenformel BBr3.
| Strukturformel | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
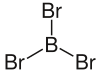
| |||||||||||||||||||
| Allgemeines | |||||||||||||||||||
| Name | Bortribromid | ||||||||||||||||||
| Andere Namen |
Tribromboran | ||||||||||||||||||
| Summenformel | BBr3 | ||||||||||||||||||
| Kurzbeschreibung |
farblose Flüssigkeit mit stechendem Geruch[1] | ||||||||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||||||||
| |||||||||||||||||||
| Eigenschaften | |||||||||||||||||||
| Molare Masse | 250,54 g·mol−1 | ||||||||||||||||||
| Aggregatzustand |
flüssig | ||||||||||||||||||
| Dichte |
2,64 g·cm−3[1] | ||||||||||||||||||
| Schmelzpunkt | |||||||||||||||||||
| Siedepunkt |
91 °C[1] | ||||||||||||||||||
| Dampfdruck | |||||||||||||||||||
| Löslichkeit |
heftige Zersetzung in Wasser[1] | ||||||||||||||||||
| Brechungsindex |
1,5312 (16 °C)[2] | ||||||||||||||||||
| Sicherheitshinweise | |||||||||||||||||||
| |||||||||||||||||||
| MAK |
Schweiz: 1 ml·m−3 bzw. 10 mg·m−3[5] | ||||||||||||||||||
| Thermodynamische Eigenschaften | |||||||||||||||||||
| ΔHf0 |
−239,7 kJ/mol[6] | ||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). Brechungsindex: Na-D-Linie, 20 °C | |||||||||||||||||||
Darstellung
BearbeitenBortribromid lässt sich darstellen durch Umsetzung von:
1. Bortrifluorid mit Aluminiumbromid[7]
2. Borcarbid mit elementarem Brom im Quarzrohr bei erhöhter Temperatur
3. (Amorphes) Bor mit elementarem Brom im Quarzrohr bei etwa 700 °C[7][8][9]
4. Kaliumtetrafluoroborat mit wasserfreiem Aluminiumbromid[10]
Eigenschaften
BearbeitenBortribromid ist eine sehr giftige, an feuchter Luft rauchende Verbindung, die bei Raumtemperatur als Flüssigkeit vorliegt.[11] Sie ist kommerziell verfügbar und eine starke Lewis-Säure.
Bei Kontakt mit Wasser erfolgt eine heftige Zersetzungsreaktion durch die Hydrolyse zu Borsäure und Bromwasserstoffsäure:[12]
Verwendung
BearbeitenBortribromid kann zur Spaltung von Ethern unter milden Bedingungen, insbesondere zur schonenden Spaltung von Alkylarylethern benutzt werden. Zusätzlich wird es auch bei der Olefin-Polymerisation und bei Friedel-Crafts-Reaktionen eingesetzt. In der Elektronikindustrie dient es als Borlieferant bei der Dotierung von Halbleitern.[13]
Einzelnachweise
Bearbeiten- ↑ a b c d e f Datenblatt Bortribromid bei Merck, abgerufen am 19. Januar 2011.
- ↑ David R. Lide (Hrsg.): CRC Handbook of Chemistry and Physics. 90. Auflage. (Internet-Version: 2010), CRC Press / Taylor and Francis, Boca Raton FL, Index of Refraction of Inorganic Liquids, S. 4-140.
- ↑ a b Eintrag zu Bortribromid in der GESTIS-Stoffdatenbank des IFA, abgerufen am 20. Januar 2022. (JavaScript erforderlich)
- ↑ Eintrag zu Boron tribromide im Classification and Labelling Inventory der Europäischen Chemikalienagentur (ECHA), abgerufen am 1. Februar 2016. Hersteller bzw. Inverkehrbringer können die harmonisierte Einstufung und Kennzeichnung erweitern.
- ↑ Schweizerische Unfallversicherungsanstalt (Suva): Grenzwerte – Aktuelle MAK- und BAT-Werte (Suche nach 10294-33-4 bzw. Bortribromid), abgerufen am 2. November 2015.
- ↑ David R. Lide (Hrsg.): CRC Handbook of Chemistry and Physics. 90. Auflage. (Internet-Version: 2010), CRC Press / Taylor and Francis, Boca Raton FL, Standard Thermodynamic Properties of Chemical Substances, S. 5-5.
- ↑ a b Georg Brauer (Hrsg.), unter Mitarbeit von Marianne Baudler u. a.: Handbuch der Präparativen Anorganischen Chemie. 3., umgearbeitete Auflage. Band II, Ferdinand Enke, Stuttgart 1978, ISBN 3-432-87813-3, S. 800.
- ↑ F. Meyer, R. Zappner: Darstellung von Bor durch Dissoziation von Borbromid. In: Berichte der Deutschen Chemischen Gesellschaft. Nr. 54, 1921, S. 550.
- ↑ Heribert Grubitsch: Anorganisch-präparative Chemie. Springer, Wien 1950, S. 353–354.
- ↑ E. Lee Gamble: Boron chloride and bromide. In: Ludwig F. Audrieth (Hrsg.): Inorganic Syntheses. Band 3. McGraw-Hill, Inc., 1950, S. 27–30 (englisch).
- ↑ Arnold F. Holleman, Egon Wiberg: Lehrbuch der anorganischen Chemie. Walter de Gruyter, 1995, ISBN 978-3-11-012641-9, S. 1890 (eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ J. J. Zuckerman: Inorganic Reactions and Methods, The Formation of Bonds to Hydrogen. John Wiley & Sons, 2009, ISBN 0-470-14536-6, S. 92 (eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ Wiley-VCH: Ullmann’s Fine Chemicals, 3 Volume Set. John Wiley & Sons, 2014, ISBN 978-3-527-68359-8, S. 406 (eingeschränkte Vorschau in der Google-Buchsuche).

