Cobalt(II)-sulfid
Cobalt(II)-sulfid ist eine chemische Verbindung aus der Gruppe der Cobaltverbindungen und Sulfide.
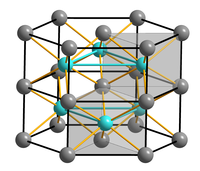
| Kristallstruktur | ||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| ||||||||||||||||
| _ Co2+ _ S2− | ||||||||||||||||
| Kristallsystem |
hexagonal | |||||||||||||||
| Raumgruppe |
P63/mmc (Nr. 194)[1] | |||||||||||||||
| Gitterparameter |
a = 338 pm, c = 520 pm[1] | |||||||||||||||
| Allgemeines | ||||||||||||||||
| Name | Cobalt(II)-sulfid | |||||||||||||||
| Andere Namen |
| |||||||||||||||
| Verhältnisformel | CoS | |||||||||||||||
| Kurzbeschreibung |
schwarzer Feststoff[2] | |||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||
| ||||||||||||||||
| Eigenschaften | ||||||||||||||||
| Molare Masse | 91,00 g·mol−1 | |||||||||||||||
| Aggregatzustand |
fest | |||||||||||||||
| Dichte |
5,45 g·cm−3[3] | |||||||||||||||
| Schmelzpunkt |
> 1116 °C[3] | |||||||||||||||
| Löslichkeit |
praktisch unlöslich in Wasser (3,8 mg·l−1 bei 18 °C)[3] | |||||||||||||||
| Sicherheitshinweise | ||||||||||||||||
| ||||||||||||||||
| Toxikologische Daten | ||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). | ||||||||||||||||
Vorkommen
BearbeitenUnter der Bezeichnung Syepoorit beschrieb James Nicol 1849 ein Cobaltsulfid mit der idealisierten Formel CoS und hexagonaler Symmetrie. Die Bezeichnung wurde 1873 von W. A. Ross in Jeypoorit und 1880 von F. R. Mallet schließlich in Jaipurit abgewandelt.[5] Der Name nimmt Bezug auf die Typlokalität des so bezeichneten Erzes, den Khetri Minen (Ketri Mine) im Bezirk Jhunjhunu in der Division Jaipur im indischen Bundesstaat Rajasthan.[6] Die Beschreibung von Jaipurit war allerdings unvollständig und die Untersuchung einer vom Britischen Museum zur Verfügung gestellten Probe durch Paul Ramdohr erwies sich als ein Gemenge aus vorwiegend Cobaltit und weiteren bereits bekannten Erzen.[7] Der Status als eigenständiges Mineral ist beim Jaipurit damit zurzeit (Stand 2018) fraglich.[8]
Gewinnung und Darstellung
Bearbeitenα-Cobalt(II)-sulfid kann durch Reaktion von Cobalt(II)-nitrat mit Schwefelwasserstoff erzeugt werden.[9]
β-Cobalt(II)-sulfid kann durch direkte Synthese aus den Elementen gewonnen werden.[9]
Es kann auch durch Fällung einer mit Essigsäure versetzten Cobalt(II)-chlorid-Lösung mit Schwefelwasserstoff dargestellt werden.
Eigenschaften
BearbeitenCobalt(II)-sulfid ist ein nicht brennbarer Feststoff, welcher unlöslich in Wasser ist.[3] Er kommt in zwei verschiedenen Kristallformen vor. α-Cobalt(II)-sulfid ist ein schwarzes Pulver, welches in Salzsäure löslich ist und an Luft Co(OH)S bildet. β-Cobalt(II)-sulfid ist ein graues Pulver. Es ist in Säuren löslich und wandelt sich durch anhaltende Temperung bei 200 °C in eine komplizierter gebaute Modifikation um. Es besitzt eine Kristallstruktur des NiAs-Typs (Raumgruppe P63/mmc (Raumgruppen-Nr. 194), a = 336,7, c = 516,0 pm) und ist nicht homogen stöchiometrisch aufgebaut, so dass sich eine Zusammensetzung von CoS1,04 bis CoS1,13 ergibt.[9]
Verwendung
BearbeitenCobalt(II)-sulfid wird als Katalysator für die Druckhydrierung organischer Verbindungen verwendet.[9]
Einzelnachweise
Bearbeiten- ↑ a b Hugo Strunz, Ernest H. Nickel: Strunz Mineralogical Tables. Chemical-structural Mineral Classification System. 9. Auflage. E. Schweizerbart’sche Verlagsbuchhandlung (Nägele u. Obermiller), Stuttgart 2001, ISBN 3-510-65188-X, S. 85.
- ↑ David R. Lide (Hrsg.): CRC Handbook of Chemistry and Physics. 90. Auflage. (Internet-Version: 2010), CRC Press / Taylor and Francis, Boca Raton FL, Properties of the Elements and Inorganic Compounds, S. 4-61.
- ↑ a b c d e f g Eintrag zu Cobalt(II)-sulfid in der GESTIS-Stoffdatenbank des IFA, abgerufen am 23. Juli 2016. (JavaScript erforderlich)
- ↑ Eintrag zu Cobalt sulphide im Classification and Labelling Inventory der Europäischen Chemikalienagentur (ECHA), abgerufen am 1. Februar 2016. Hersteller bzw. Inverkehrbringer können die harmonisierte Einstufung und Kennzeichnung erweitern.
- ↑ Albert Huntington Chester: A dictionary of the names of minerals including their history and etymology. 1. Auflage. John Wiley & Sons, New York 1896, S. 137 (online verfügbar bei archive.org – Internet Archive).
- ↑ Typlokalität Khetri Mine im Mineralienatlas und bei Mindat
- ↑ Paul Ramdohr: Die Erzmineralien und ihre Verwachsungen. 4., bearbeitete und erweiterte Auflage. Akademie-Verlag, Berlin 1975, S. 660 (Jaipurit).
- ↑ Malcolm Back, Cristian Biagioni, William D. Birch, Michel Blondieau, Hans-Peter Boja und andere: The New IMA List of Minerals – A Work in Progress – Updated: July 2024. (PDF; 3,6 MB) In: cnmnc.units.it. IMA/CNMNC, Marco Pasero, Juli 2024, abgerufen am 13. August 2024 (englisch).
- ↑ a b c d Georg Brauer (Hrsg.) u. a.: Handbuch der Präparativen Anorganischen Chemie. 3., umgearbeitete Auflage. Band III, Ferdinand Enke, Stuttgart 1981, ISBN 3-432-87823-0, S. 1667.

