Curium(III)-oxalat
Curium(III)-oxalat ist das Oxalsäuresalz des Elements Curium. Das Decahydrat besitzt die Summenformel Cm2(C2O4)3 · 10 H2O.
| Strukturformel | |||||||
|---|---|---|---|---|---|---|---|
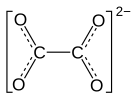
| |||||||
| Allgemeines | |||||||
| Name | Curium(III)-oxalat | ||||||
| Summenformel |
| ||||||
| Kurzbeschreibung |
hellgrüner Feststoff[1] | ||||||
| Externe Identifikatoren/Datenbanken | |||||||
| |||||||
| Eigenschaften | |||||||
| Molare Masse | (für 248Cm): 940,22 g·mol−1 (Decahydrat) | ||||||
| Aggregatzustand |
fest | ||||||
| Löslichkeit |
löslich in wässrigen Alkalimetallcarbonatlösungen[2] | ||||||
| Gefahren- und Sicherheitshinweise | |||||||
 Radioaktiv | |||||||
| |||||||
| Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). | |||||||
Darstellung
BearbeitenCurium(III)-oxalat bildet sich, wenn wässrige Curium(III)-Lösungen mit Oxalsäure versetzt werden.[4]
Eigenschaften
BearbeitenDas Decahydrat dehydratisiert schrittweise im Vakuum, indem es bei 280 °C in die wasserfreie Form übergeht. Wird es auf 360 °C weiter erhitzt, entsteht das Carbonat.[5]
Das hydratisierte Oxalat ist in wässrigen Alkalimetallcarbonatlösungen löslich. Die Löslichkeit nimmt in der Hitze stark zu.
Frisch filtriertes 244Curiumoxalat unterliegt aufgrund der hohen Radioaktivität innerhalb weniger Stunden einer Radiolyse unter Bildung des Carbonats, was durch Gasentwicklung nach Auflösen in Säure nachgewiesen werden konnte.[1]
Verwendung
BearbeitenCuriumoxalat wird routinemäßig zur Darstellung von Curium(IV)-oxid (CmO2) über Curiumhydroxid (Cm(OH)3) herangezogen.[2][5]
Des Weiteren können Curium-Ionen, die durch lange Lagerung Verunreinigungen an Plutonium und Americium aufweisen, durch Oxalatfällung aus ihren Lösungen in sehr hohen Ausbeuten (bis 99,4 %) zurückgewonnen werden.[6]
Sicherheitshinweise
BearbeitenEinstufungen nach der CLP-Verordnung liegen nicht vor, da sich diese nur auf die chemische Gefährlichkeit bezieht. Curium und seine Verbindungen sind hochradioaktiv und müssen daher unter höchster Vorsicht gehandhabt werden.
Literatur
Bearbeiten- Gregg J. Lumetta, Major C. Thompson, Robert A. Penneman, P. Gary Eller: Curium, in: Lester R. Morss, Norman M. Edelstein, Jean Fuger (Hrsg.): The Chemistry of the Actinide and Transactinide Elements, Springer, Dordrecht 2006; ISBN 1-4020-3555-1, S. 1397–1443 (doi:10.1007/1-4020-3598-5_9).
Einzelnachweise
Bearbeiten- ↑ a b G. A. Burney, J. A. Porter: Solubilities of Pu(III), Am(III), and Cm(III) oxalates, in: Inorganic and Nuclear Chemistry Letters, 1967, 3 (3), S. 79–85 (doi:10.1016/0020-1650(67)80128-4).
- ↑ a b N. E. Bibler: Hydroxide metathesis of multigram amounts of curium oxalate, in: Inorganic and Nuclear Chemistry Letters, 1972, 8 (2), S. 153–156 (doi:10.1016/0020-1650(72)80102-8).
- ↑ Die von der Radioaktivität ausgehenden Gefahren gehören nicht zu den einzustufenden Eigenschaften nach der GHS-Kennzeichnung. In Bezug auf weitere Gefahren wurde dieser Stoff entweder noch nicht eingestuft oder eine verlässliche und zitierfähige Quelle hierzu wurde noch nicht gefunden.
- ↑ Gregg J. Lumetta, Major C. Thompson, Robert A. Penneman, P. Gary Eller: Curium ( vom 17. Juli 2010 im Internet Archive), in: Lester R. Morss, Norman M. Edelstein, Jean Fuger (Hrsg.): The Chemistry of the Actinide and Transactinide Elements, Springer, Dordrecht 2006; ISBN 1-4020-3555-1, S. 1397–1443 (doi:10.1007/1-4020-3598-5_9).
- ↑ a b V. Scherer, M. Fochler: The thermal decomposition of curium(III) oxalate IO-hydrate, in: Journal of Inorganic and Nuclear Chemistry, 1968, 30 (6), S. 1433–1437 (doi:10.1016/0022-1902(68)80282-9).
- ↑ Hirokazu Hayashi, Hiromichi Hagiya, Seong-Yun Kim, Yasuji Morita, Mitsuo Akabori, Kazuo Minato: Separation and recovery of Cm from Cm–Pu mixed oxide samples containing Am impurity, in: Journal of Radioanalytical and Nuclear Chemistry, 2013, 296 (3), S. 1275–1286 (doi:10.1007/s10967-012-2304-y).