Desulfuromonadales
Die Desulfuromonadales bilden eine Ordnung innerhalb der Deltaproteobacteria. Wie alle Pseudomonadota (Proteobakterien) sind sie gramnegativ. Sie nutzen durch anaerobe Atmung elementaren Schwefel, Mangan oder Eisen zur Energiegewinnung im Stoffwechsel. Man spricht von der Fe(III)-, Schwefel- oder Mn(IV)-Reduktion. Auch Nitrat und Trichloressigsäure sowie auch andere Metalle wie Technetium oder Cobalt können von einigen dieser Bakterien reduziert und somit im Energiestoffwechsel eingesetzt werden. Die Fähigkeit, Technetium zu verstoffwechseln ist insofern bemerkenswert, als dieses Element radioaktiv und nur in verschwindend kleinen Mengen (als Resultat der Spontanspaltung von [[Uran238U]]) auf der Erde vorhanden ist.
| Desulfuromonadales | ||||||||||
|---|---|---|---|---|---|---|---|---|---|---|
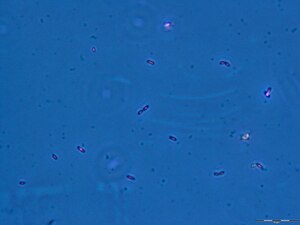
Geobacter sulfurreducens | ||||||||||
| Systematik | ||||||||||
| ||||||||||
| Wissenschaftlicher Name | ||||||||||
| Desulfuromonadales | ||||||||||
| corrig. Kuever et al. 2006 |
Die Arten dieser Ordnung sind meist stäbchenförmig. Meist sind sie durch eine Geißel beweglich, Pelobacter und Malonomonas allerdings nur in frühen Wachstumsstadien der Kolonien, andere sind unbeweglich.
Eigenschaften
BearbeitenDie Mitglieder dieser Ordnung sind meist obligat anaerob, das heißt, sie können nur unter völligem Ausschluss von Sauerstoff leben, es gibt jedoch einige mikroaerobe Arten. Beispielsweise toleriert Malonomonas geringe Sauerstoffkonzentrationen. Desulfuromusa kysingii toleriert ebenfalls geringfügig Sauerstoffeinfluss (2 %), wächst hierbei aber nicht. Die meisten Desulfuromonadales sind mesophil, ihr Wachstumsoptimum liegt also bei mittleren Temperaturen. Geopsychrobacter ist psychrophil (kälteliebend), es wächst bei Temperaturen zwischen 4 und 30 °C, das Optimum liegt bei 22 °C.[1] Geothermobacter ehrlichii ist thermophil und wurde gefunden in einer Hydrothermalquelle des Juan-de-Fuca-Rückens. Es wächst bei Temperaturen zwischen 35 and 65 °C.[2]
Desulfuromonadales wurden von anoxischen Habiten im Süßwasser, Meerwasser und Brackwasser isoliert. Malonomonas kommt in anoxischen Meeressedimenten vor, im Süßwasser wurde diese Gattung noch nicht gefunden. Geobacter scheint in Böden die vorherrschende Rolle innerhalb der Fe(III)-reduzierenden Bakterien zu spielen.[3]
Ökologie
BearbeitenEinige Arten von Desulfuromonas können in Gegenwart von Acetat in einer mutualistischen Assoziation mit Arten von phototrophen, schwefelbildenden Bakterien, den grünen Schwefelbakterien (Chlorobiaceae), leben. Bei diesem Syntrophismus wird der Energiestoffwechsel und damit das Wachstum beider Partner durch Austausch von bestimmten Stoffwechselprodukten gegenseitig gefördert. Beispielsweise bildet das grüne Schwefelbakterium Prosthecochloris aestuarii aus Schwefelwasserstoff elementaren Schwefel (S0) woraus Desulfuromonas wiederum, solange Acetat vorhanden ist, durch die Schwefelreduktion Schwefelwasserstoff (H2S) bildet.[4] Somit bildet sich ein verkürzter Schwefelkreislauf.
Durch die Reduktion von dreiwertigen Eisen-Ionen (Fe3+) zu zweiwertigen (Fe2+) oder von elementarem Schwefel zu Schwefelwasserstoff spielen Desulfuromonadales eine wichtige Rolle im Schwefelkreislauf und Eisenkreislauf der Erde. Weiterhin sind Eisen-reduzierende Bakterien interessant in Bezug auf die Evolution. Es wird vermutet, dass die Fe(III)-Reduktion neben der Schwefelreduktion eine der ersten Formen der anaeroben Atmung von Bakterien ist.[5] Man findet diese Form des Stoffwechsels vor allem in den früh abzweigenden Entwicklungslinien der Bakterien und Archaeen.
Einige Geobacter-Stämme sind durch ihre Fähigkeit, aromatische Verbindungen wie Toluol abzubauen, für die Reinigung von schadstoffbelasteten Böden und Grundwässern bedeutend.
Geobacter metallireducens kann als Elektronenakzeptor auch Uran verwenden: Das in Form von Uranyl-Ionen (UO22+) wasserlösliche sechswertige Uran U(VI) wird hierbei durch die bakterielle Übertragung von 2 Elektronen zu vierwertigem Uran U(IV) reduziert, welches wiederum als das wasserunlösliche Urandioxid (UO2, das Mineral Uraninit) ausfällt. Dadurch ist dieses Bakterium für die Säuberung von mit Uran belastetem Wasser anwendbar. Denkbar wäre auch eine Art Biomining von Uran aus Meerwasser (Urangehalt 3,3 μg/l) oder stärker uranhaltigen Wässern.
Stoffwechsel
BearbeitenEnergiequellen dieser Bakterienordnung sind anaerobe Atmung sowie Gärung. Bei der anaeroben Atmung werden von Desulfuromonadales elementarer Schwefel (S0), Polysulfide oder dreiwertiges Eisen (Fe3+) statt Sauerstoff (wie bei der aeroben Atmung) in der Atmungskette als Elektronenakzeptoren genutzt und somit reduziert. Als Elektronendonatoren dienen einfache organische Verbindungen wie z. B. Acetat. Die freigesetzte Energie wird zur ATP-Bildung eingesetzt. Die organischen Elektronendonatoren werden meist vollständig über den Citronensäurezyklus zu CO2 oxidiert. Bei der Schwefelreduktion (Schwefelatmung) wird Schwefel zu Schwefelwasserstoff (H2S) reduziert, bei der Eisenreduktion (Eisenatmung) dreiwertige Eisen-Ionen (Fe3+) zu zweiwertigen (Fe2+). Auch andere Stoffe können reduziert werden, z. B. Mangan(IV), Cobalt, Technetium, Nitrat und Trichloressigsäure.
Die stammesgeschichtliche Verwandtschaft der Eisen(III)- und Mangan(IV)-reduzierenden Bakterien ist vielfältig. Viele dieser Bakterien, welche hierbei Acetat vollständig oxidieren, findet man bei den Geobacteraceae. Andere mit dieser Eigenschaft sind z. B. Arten von Shewanella (Gammaproteobacteria), Acidithiobacillus ferrooxidans (Betaproteobacteria) und Deferribacter themophilus (Deferribacteres).
Mangan(IV)-, Eisen(III)- und Schwefelreduktion dienen ausschließlich der Energiegewinnung, nicht dem Baustoffwechsel, z. B. für den Aufbau von Aminosäuren, sind also nicht assimilatorisch, die Endprodukte, Mn(II), Fe(II) bzw. Schwefelwasserstoff werden sofort ausgeschieden.
Schwefelreduktion
BearbeitenAlle Arten der Desulfuromonadaceae sowie Geobacter sulfurreducens, Geobacter humireducens und Syntrophotalea carbinolica (auch Pelobacter carbinolicus genannt[6]) zählen zu den Schwefelatmern. Bei Syntrophotalea carbinolica wurde die Schwefel- wie auch die Eisenreduktion nachgewiesen[7]. Einfache organische Verbindungen wie Acetat dienen als Elektronendonatoren im Energiestoffwechsel und als Baustoffquellen. Weitere für verschiedene Arten verwertbare Stoffe sind u. a.: Glutamat, Fumarat, Alanin, Oxalacetat und Pyruvat. Desulfuromonas palmitatis oxidiert u. a. auch langkettige Fettsäuren. Außerdem kann es auch elementaren, molekularen Wasserstoff H2 im Energiestoffwechsel als Elektronendonator verwenden.
Desulfuromonas acetoxidans reduziert elementaren Schwefel zu Schwefelwasserstoff und nutzt Acetat als Elektronendonator, das dabei über den Citronensäurezyklus vollständig zu Kohlenstoffdioxid (CO2) oxidiert wird:
- CH3COOH + 2 H2O + 4 S0 → 2 CO2 + 4 H2S
Im Englischen spricht man auch von den „sulfur reducing bacteria“. Das Präfix desulfur- in der Systematik steht für die Schwefel-Reduktion. Bei der Schwefelatmung dieser Bakterien werden Sulfat, Thiosulfat und Sulfit nicht als Elektronenakzeptoren genutzt. Dies unterscheidet sie von den Sulfatatmern (sulfatreduzierenden Bakterien). Einige Sulfatreduzierer (Sulfatatmer) sind allerdings auch in der Lage, elementaren Schwefel als Elektronenakzeptor einzusetzen.
Einige weitere bekannte Bakterien, die elementaren Schwefel reduzieren, sind: Desulfovibrio gigas, Arten von Desulfomicrobium, Desulfurella acetivorans und Wolinella succinogenes. Schwefel-reduzierende Archaeen sind: Sulfolobus ambivalens, Pyrobaculum islandicum, Stygiolobus azoricus und Thermodiscus maritimus.
Eisenreduktion und andere Elektronenakzeptoren
BearbeitenEisen ist weitverbreitet in der Natur und ist ein wichtiges Stoffwechselelement, welches schon früh im Laufe der Evolution für den Energiestoffwechsel genutzt wurde. Viele Arten der Ordnung Desulfuromonadales reduzieren Fe3+ zu Fe2+. Die Eisen(III)-Ionen können aus verschiedenen Eisenverbindungen abgespalten werden, einige Beispiele sind: Eisen(III)-chlorid, Eisen(III)-oxid und Eisen(III)-citrat. Geobacter metallireducens reduziert Fe(III) zu Fe(II) beispielsweise mit Acetat als Elektronendonator:
- CH3COO− + 8 Fe3+ + 4 H2O → 2HCO3− + 8 Fe2+ +9 H+
Alle Arten von Geobacter, Geothermobacter und Geopsychrobacter sowie Syntrophotalea carbinolica, S. acetylenica und S. venetiana nutzen dreiwertiges Eisen (Fe3+) als Elektronenakzeptor. Viele Arten von Desulfuromonadaceae nutzen außer Schwefel auch Eisen als Elektronenakzeptor.
Bei Desulfuromusa kysingii und bei einigen Arten von Geobacter (z. B. Geobacter metallireducens und Geobacter humireducens) kann auch Nitrat als Elektronenakzeptor dienen. Nitrat wird zu Ammoniak reduziert und nicht zu elementarem, molekularem Stickstoff N2, wie es bei der Denitrifikation der Fall ist.
Mangan wird ebenfalls von einigen Arten, z. B: Desulfuromonas palmitatise, Geobacter metallireducens und Desulfuromonas acetexigens, reduziert und als Elektronenakzeptor genutzt. Mn(IV) wird hierbei zu Mn(II) reduziert. Trichlorobacter (Geobacteraceae) nutzt Trichloressigsäure als Elektronenakzeptor und reduziert es zu Dichloressigsäure und Chlorwasserstoff (HCl). Es besteht eine relativ große Vielfalt von Metallen, die von einigen Arten im Energiestoffwechsel reduziert werden, beispielsweise Cobalt Co(III) und Technetium Tc(VII) von Geobacter sulfurreducens. Tc(VII) wird auch von Geobacter metallireducens als Elektronenakzeptor genutzt. Ob die Tc(VII)-Reduktion hierbei auch das Wachstum dieser Arten ermöglicht, ist allerdings unklar. Auch Uran U(VI) kann von Geobacter metallireducens als einzigem Elektronenakzeptor eingesetzt werden und wird zu U(IV) reduziert. Dieses Bakterium wächst, wenn U(VI) als einziger Elektronenakzeptor vorhanden ist[8]. Auch Shewanella putrefaciens, eine Bakterienart der Gammaproteobacteria, zeigt diese Fähigkeit. Bei anderen Fe(III)- und Mangan(IV)-Atmern sowie bei vielen Sulfat-reduzierenden Bakterien (z. B. Desulfovibrio) wurde ebenfalls die Fähigkeit nachgewiesen, U(VI) zu reduzieren, doch Wachstum wurde hierbei nicht beobachtet[9].
Gärung
BearbeitenEinige Mitglieder der Desulfuromonadales sind auch zur Gärung befähigt (zur Abgrenzung zum Begriff Fermentation siehe dort). In der Regel ist dabei Acetat das Endprodukt. Alle Arten von Desulfuromusa können diesen Energiestoffwechsel zusätzlich zur anaeroben Atmung nutzen. Auch alle Mitglieder der Pelobacteraceae sind zur Gärung befähigt. Auch Arten von Syntrophotalea, wie Syntrophotalea acetylenica, S. carbinolica und S. venetiana können die Gärung durchführen. Hier kann zusätzlich zu Acetat auch Ethanol entstehen, bei der Art Pelobacter propionicus auch Propionat. P. acidigallici bildet Acetat und CO2. Malonomonas kann auf einem Agarmedium mit Malonat als einziger Energie- und Kohlenstoffquelle kultiviert werden, aus Malonat entsteht dabei Acetat als Endprodukt, Malat und Fumarat können ebenfalls von dieser Art verwendet werden, Endprodukte sind dann Succinat und CO2.
Geschichte
BearbeitenDie Schwefelreduktion, bei der Acetat als Elektronendonator fungiert, wurde erst 1976 im Bakterium Desulfuromonas acetoxidans entdeckt.[10] Geobacter metallireducens wurde 1987 von Lovley und Mitarbeitern aus Sedimenten des Potomac Rivers isoliert und als Bakterienstamm GS-15 bezeichnet.[11] 1988 wurde sein Energiestoffwechsel mit vollständiger Oxidation von Acetat (und anderen Kohlenstoffverbindungen), verbundenen mit Fe(III)-Reduktion, nachgewiesen[12] und 1993 wurde das Bakterium als Geobacter metallireducens benannt.
Geobacter metallireducens ist ein intensiv untersuchter Eisenreduzierer und ist u. a. von besonderen Interesse der Geomikrobiologie und vor allem der Erforschung des Stoffwechselwegs der Eisenreduktion.
Systematik
BearbeitenDie Ordnung Desulfuromonadales besteht aus folgenden Familien und Gattungen[13]:
- Desulfuromonadaceae corrig. Kuever et al. 2006
- Desulfuromonas Pfennig & Biebl 1977
- Desulfuromusa Liesack & Finster 1994
- Malonomonas Dehning & Schink 1990
- Pelobacter Schink & Pfennig 1983
- Geobacteraceae Holmes et al. 2004
- Geoalkalibacter Zavarzina et al. 2007
- Geobacter Lovley et al. 1995
- Geobacter sulfurreducens Caccavo et al. 1994
- Geopsychrobacter Holmes et al. 2005
- Geothermobacter Kashefi et al. 2005
- Syntrophotaleaceae Waite et al. 2020
- Syntrophotalea Waite et al. 2020
Ein weiteres, älteres, aber noch genutztes System besteht nur aus zwei Familien[14]:
- Desulfuromonadaceae
- Desulfuromonas
- Desulfuromusa
- Malonomonas
- Pelobacter
- Geobacteraceae
- Geoalkalibacter Zavarzina et al. 2007
- Geobacter
- Geopsychrobacter
- Geothermobacter
- Trichlorobacter
Literatur
Bearbeiten- Oliver Klimmek, Achim Kröger: Oxidative Phosphorylierung mit Schwefel statt Sauerstoff. In Biospektrum (Zeitschrift), Jg. 8, 2002, Nr. 2 ISSN 0947-0867 S. 153–157 online
- Michael T. Madigan, John M. Martinko, Jack Parker: Brock – Mikrobiologie. 11. Auflage. Pearson Studium, München 2006, ISBN 3-8274-0566-1
- George M. Garrity: Bergey's manual of systematic bacteriology. 2. Auflage. Springer, New York 2005, Vol. 2: The Proteobacteria Part C: The Alpha-, Beta-, Delta-, and Epsilonproteabacteria ISBN 0-387-24145-0
- Martin Dworkin, Stanley Falkow, Eugene Rosenberg, Karl-Heinz Schleifer, Erko Stackebrandt (Hrsg.) The Prokaryotes, A Handbook of the Biology of Bacteria. 7 Bände, 3. Auflage, Springer, New York u. a. O., 2006, ISBN 0-387-30740-0. Vol. 2: Ecophysiology and Biochemistry ISBN 0-387-25492-7
Weblinks
Bearbeiten- Geobacter Project
- Wissenschaft Online: Bakterieller Elektroschocker (PDF-Datei; 83 kB)
Einzelnachweise
Bearbeiten- ↑ Holmes DE, Nicoll JS, Bond DR, Lovley DR.: Potential role of a novel psychrotolerant member of the family Geobacteraceae, Geopsychrobacter electrodiphilus gen. nov., sp. nov., in electricity production by a marine sediment fuel cell. In: Applied and Environmental Microbiology. Band 70, Nr. 10, 2004, S. 6023–6030 doi:10.1128/AEM.70.10.6023-6030.2004 (englisch).
- ↑ Kashefi K, Holmes DE, Baross JA, Lovley DR.: Thermophily in the Geobacteraceae: Geothermobacter ehrlichii gen. nov., sp. nov., a novel thermophilic member of the Geobacteraceae from the "Bag City" hydrothermal vent. In: Applied and Environmental Microbiology. Band 69, Nr. 5, 2003 S. 2985–2993; PMID 12732575, doi:10.1128/AEM.69.5.2985-2993.2003 (englisch).
- ↑ Bo B. Jørgensen, Niels P. Revsbech, T. Henry Blackburn, and Yehuda Cohen: Enrichment of Geobacter Species in Response to Stimulation of Fe(III) Reduction in Sandy Aquifer Sediments. In: Applied and Environmental Microbiology Bd. 38, Nr. 1, 1979, S. 46–58, PMID 10833228
- ↑ Biebl, H. and N. Pfennig: Growth yields of green sulfur bacteria in mixed cultures with sulfur and sulfate reducing bacteria. In: Archives of Microbiology. Band 117, 1978, S. 9–16; doi:10.1007/BF00689344
- ↑ Vargas, M., K. Kashefi, E. L. Blunt-Harris, and D. R. Lovley.: Microbiological evidence for Fe(III) reduction on early Earth. In: Nature, Band 395, 1998, S. 65–67; PMID 9738498, doi:10.1038/25720 (englisch).
- ↑ Gabriela Feix Pereira, Harry Luiz Pilz-Junior & Gertrudes Corção: The impact of bacterial diversity on resistance to biocides in oilfields In: Scientific Reports. Band 11, Artikel Nummer: 23027 (2021) doi:10.1038/s41598-021-02494-7
- ↑ Lovley, D.R., E.J.P. Phillips, D.J. Lonergan and P.K. Widman: Fe(III) and S0 reduction by Pelobacter carbinolicus. In: Applied and Environmental Microbiology Bd. 61, 1995, S. 2132–2138 PMID 7793935
- ↑ Lovley, D. R., E. J. P. Phillips, Y. A. Gorby, and E. R. Landa: Microbial reduction of uranium. In: Nature. Bd. 350, 1991, S. 413–416 Nature Online.
- ↑ Lovley, D. R., E. E. Roden, E. J. P. Phillips, and J. C. Woodward: Enzymatic iron and uranium reduction by sulfate-reducing bacteria. In: Marine Geology. Bd. 113, 1993, S. 41–53.
- ↑ Pfennig, N. and Biebl, H.: Desulfuromonas acetoxidans gen. nov. and sp. nov., a new anaerobic, sulfur-reducing, acetate oxidizing bacterium. In: Archives of Microbiology. Bd. 110, 1976. S. 3–12. doi:10.1007/BF00303588
- ↑ Lovley D.R, Stolz J.F, Nord G.L, Phillips E.J.P: Anaerobic production of magnetite by a dissimilatory iron-reducing microorganism. In: Nature. Bd. 330, 1987, S. 252–254. Nature Online
- ↑ Lovley, D.R. and E.J.P. Phillips: Novel mode of microbial energy metabolism: organic carbon oxidation coupled to dissimilatory reduction of iron or manganese. In: Applied and Environmental Microbiology. Bd. 54, 1988, S. 1472–1480. Online
- ↑ Systematik nach National Center for Biotechnology Information (NCBI) (Stand: 23. Dezember 2012)
- ↑ bacterio.cict.fr: List of Prokaryotic names with Standing in Nomenclature – Order Desulfuromonadales ( vom 8. August 2007 im Internet Archive) (englisch)