Humane Rotaviren
Humane Rotaviren sind beim Menschen vorkommende Viren der Gattung Rotavirus (Familie Reoviridae, Unterfamilie Sedoreovirinae). Ihr Name rührt von der radähnlichen Struktur (lateinisch rota ‚das Rad‘) der Viren, die sich unter dem Elektronenmikroskop zeigt.[3] Sie wurden 1973 von Ruth Bishop durch Dünndarmbiopsien erkrankter Kinder entdeckt.[4]
| Rotaviren | ||||||||
|---|---|---|---|---|---|---|---|---|
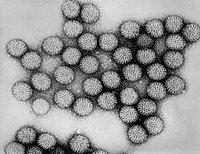
Humanes Rotavirus | ||||||||
| Systematik | ||||||||
| Taxonomische Merkmale | ||||||||
| ||||||||
| Wissenschaftlicher Name | ||||||||
| Rotavirus | ||||||||
| Kurzbezeichnung | ||||||||
| RVA bis RVJ | ||||||||
| Links | ||||||||
|

Rotaviren sind die häufigste Ursache für schwere Durchfallerkrankungen, sie tragen jährlich zu etwa 140 Millionen Fällen weltweit bei. Von allen klinisch relevanten Durchfallerkrankungen gehen 35 bis 52 % auf Rotaviren zurück. Zur Prävention stehen Impfstoffe zur Verfügung.
Rotaviren sind auch im Tierreich weitverbreitet. Rotavirusinfektionen von Kälbern haben große wirtschaftliche Auswirkungen.
Aufbau der Rotaviren
BearbeitenHumane Rotaviren sind 76 nm große RNA-Viren mit einem doppelschaligen ikosaedrischen Kapsid. Eine Virushülle ist nicht vorhanden. Das Genom besteht aus elf doppelsträngigen RNA-Segmenten von 0,6 bis 3,3 kb Länge. Jedes dieser Segmente codiert ein virales Protein. Durch die Segmentierung des Genoms besteht die Möglichkeit der Reassortantenbildung.[5]
Klassifikation
BearbeitenHumane Rotaviren gehören zur Familie der Reoviridae, Unterfamilie Sedoreovirinae. Insgesamt sind neun Spezies innerhalb der Gattung Rotavirus bekannt, bezeichnet mit Rotavirus A bis Rotavirus J * (International Committee on Taxonomy of Viruses (ICTV), Stand 2020).[6] Menschen infizieren sich hauptsächlich mit den Spezies A, B und C, am häufigsten mit Spezies A. Letztere ist mithin die klinisch wichtigste.[3] Die Spezies A bis E * verursachen auch bei Tieren Krankheiten,[7] so etwa Spezies E und H bei Schweinen, Spezies D, F und G bei Vögeln, Spezies I bei Katzen und Spezies J bei Langflügelfledermäusen.[8][9][10][11]
Bei der Klassifizierung der Serotypen innerhalb der Spezies Rotavirus A[12] wurde ursprünglich, ähnlich wie im Fall des Grippevirus Influenzavirus A,[13] ein duales System angewandt, das auf der Reaktivität der Epitope zweier Proteine auf der Oberfläche des Virions basierte, wobei das Glycoprotein VP7 die G-Serotypen und das protease-sensitive Protein VP4 die P-Serotypen definierte.[14] Es wurde durch ein G-/P-Genotyp-System abgelöst.[14] Hierbei werden die Gene von VP4 und VP7 klassifiziert.
Da die beiden Gene, welche G- und P-Genotypen bestimmen, getrennt an die Tochterviren weitergegeben werden können, finden sich – wie bei Influenza – unterschiedliche Kombinationen.[14] Für Rotaviren der Gruppe A wurde ein Typisierungssystem für das gesamte Genom aufgestellt, das zur Bestimmung der Herkunft atypischer Linien verwendet werden kann.[15] Die Verbreitung von Rotaviren der einzelnen G- und P-Typen variiert wie bei den H/N-Typen der Grippeviren von Land zu Land und von Jahr zu Jahr.[16] Die G- und P-Antigentypen sind variabel kombinierbar.[3] Ist der G-Genotyp bekannt, wird dieser durch eine arabische Zahl dargestellt (z. B. G1), ein bekannter P-Genotyp wird mit einer arabischen Zahl in eckigen Klammern angegeben (z. B. P[8]).[14][7] Es sind 32 G- und 51 P-Typen bekannt,[17] humanpathogen sind nur wenige Kombinationen (G1P[8], G2P[4], G3P[8], G4P[8], G9P[8] und G12P[8]).[18]
Übertragung
BearbeitenDie Infektion mit Rotaviren erfolgt meist auf gewöhnlichem fäkal-oralem Weg, wobei kontaminierte Lebensmittel und kontaminiertes Trinkwasser eine Rolle spielen können. Die Möglichkeit einer Übertragung durch Aerosole lässt sich experimentell nachweisen.[19] Im Anschluss an eine schwere Erkrankung wird der Erreger üblicherweise für ca. eine bis drei Wochen ausgeschieden. Die Ausscheidung kann jedoch bis zu acht Wochen,[20] bei Patienten mit Immundefizienz noch länger dauern.[21] Der Erreger kann tagelang auf Oberflächen und wochenlang in Wasser aktiv bleiben (hohe Tenazität). Auch auf Händen kann der Erreger überdauern.[22] Die hohe Durchseuchung bereits im Kindesalter resultiert aus der geringen Infektionsdosis von nur zehn Viruspartikeln, der hohen Konzentrationsdichte im diarrhöischen Kot (etwa 1011 infektiöse Partikeln pro Milliliter) und der hohen Umwelttoleranz des Erregers.[3]
Epidemiologie
BearbeitenRotaviren sind weltweit verbreitet. Vor der Einführung der Rotavirus-Impfungen haben bis zum Ende des dritten Lebensjahres die meisten Kinder (> 90 %) bereits eine Infektion durchgemacht. In Deutschland werden im Schnitt pro Jahr etwa 50.000 Erkrankungsfälle gemeldet.[23] In den gemäßigten Zonen treten die meisten davon zwischen Februar und April auf, in den Tropen hingegen unterliegt die Inzidenz keinen signifikanten Schwankungen im Jahresverlauf.[3] Innerhalb der ersten Lebensjahre werden infolge von Kontakten mit Rotaviren zunehmend Antikörper gebildet. Frühere Erkrankungen können bei einer späteren Reinfektion mit denselben bzw. anderen Rotaviren-Typen vor einer neuerlichen Erkrankung schützen. Zwar erkrankt man, wenn überhaupt, nur leicht, doch scheiden Infizierte infektiöse Viren aus und sind damit Überträger.[3] Im Erwachsenenalter äußern sich Erkrankungen vor allem als Reisediarrhoe, wobei nur ca. 20 % der Reisediarrhoen durch Rotaviren entstehen. Die schwersten Krankheitsverläufe sind in der Altersgruppe zwischen sechs Monaten und zwei Jahren zu beobachten. In den gemäßigten Klimazonen ereignen sich Rotavirusinfektionen vorwiegend während der Wintermonate. Außer Kindern erkranken vor allem Ältere oder Immunsupprimierte schwer.
Nach Schätzungen der Weltgesundheitsorganisation starben 2004 etwa 527.000 Kinder unter fünf Jahren an einer Rotavirus-induzierten Dehydratation bzw. Gastroenteritis, hauptsächlich in Entwicklungsländern.[24] Nach der Einführung der Impfstoffe 2006 verringerte sich die Zahl der Todesfälle: So starben 2008 etwa 453.000 Kinder unter fünf Jahren, 2013 etwa 215.000 Kinder unter fünf Jahren.[25] In Deutschland sind durch eine viral bedingte Einstülpung des Darmes[26] verursachte Todesfälle äußerst selten.[27]
Krankheitsbilder und Physiologie
BearbeitenNach einer Inkubationszeit von ein bis drei Tagen treten die klinischen Symptome auf.[3] Die Infektion kann aber auch klinisch inapparent, d. h. ohne Symptome verlaufen. Häufig beginnen die Symptome mit Erbrechen, gefolgt von mäßigem Fieber und nichtblutigem Durchfall; Bauchschmerzen sind dagegen selten.[3] Bei schweren Krankheitsverläufen kann der Durchfall vier bis fünf Tage andauern und durch damit verbundenen Wasser- und Elektrolytverlust zur Exsikkose führen, die potentiell lebensbedrohlich ist. Diese und die auftretende metabolische Azidose können zu Herzrhythmusstörungen bis zum Herzstillstand führen.[3] Die übliche Erkrankungsdauer beträgt sechs bis acht Tage. Bei Kleinkindern kann die Infektion mit Rotaviren auch zu einer Intussuszeption des Darmes als besonderer Komplikation führen, die operativ behandelt werden muss. Zudem können die Viren ins Blut gelangen (Virämie) und Nieren und Leber befallen.[3]
Die Vermehrung der Erreger findet in den apikalen Enterozyten der Dünndarmzotten statt. Vermutlich wird durch das virale Protein (NSP4), das Eigenschaften eines Enterotoxins aufweist, die pathogene Wirkung verstärkt.
Nach etwa 10 bis 14 Tagen endet die Ausscheidung von Viren, Immunkompromittierte leiden dagegen monatelang an Durchfällen und damit einhergehender Virusausscheidung.[3]
Diagnose
BearbeitenDie diagnostische Untersuchung auf Rotaviren erfolgt aus dem Stuhl meist mit einem Immunassay, der spezifisch ein Kapsidprotein als Antigen nachweist. Antigentests haben oft nur geringe analytische Sensitivität. Doch in der akuten Erkrankungsphase ist viel virales Antigen im flüssigen Stuhl vorhanden, sodass die Testempfindlichkeit reicht, um Rotaviren als Ursache zu bestätigen. Das Virus ist bei längerfristiger Ausscheidung ohne akute Infektionszeichen wegen geringer Antigenmenge mittels Antigentest nicht zu bestätigen.
Einfach ist der Nachweis im Stuhl mittels Elektronenmikroskopie, da die Rotaviren an ihrer typischen Morphologie gut zu erkennen sind. Für spezielle Fragestellungen zum Ausscheiderstatus oder zur Bestimmung der Subtypen für epidemiologische Untersuchungen ist eine RT-PCR zu empfehlen. Nur noch selten wird eine klassische Virusisolierung, RNA-Elektrophorese oder Nukleinsäurehybridisierungsreaktion verwendet.
Schnelltestverfahren zum Nachweis von Antigen sind zwar möglich, aber aufgrund geringer Sensibilität und nicht ausreichender Spezifität (falsch positive Ergebnisse) nur eingeschränkt verwertbar. Serologische Methoden zum Nachweis spezifischer Antikörper gegen Rotaviren haben diagnostisch keine Bedeutung.
Prophylaxe
BearbeitenAls Prophylaxemaßnahme dient die Einhaltung allgemeiner Hygienestandards sowie die Isolierung von Patienten bei einer stationären Aufnahme, eventuell in einer Kohortenisolierung. Aufgrund der hohen Tenazität des Erregers ist eine hohe Compliance essentiell, zur Oberflächendesinfektion sollten viruzide Mittel verwendet werden.[3]
Impfung
BearbeitenIn Europa stehen zwei verschiedene Rotavirusimpfstoffe zur Verfügung: ein monovalenter Impfstoff RV1 (Rotarix von GlaxoSmithKline) sowie ein pentavalenter Impfstoff RV5 (RotaTeq von Sanofi Pasteur MSD).[28] Das Impfschema besteht aus zwei bzw. drei Teilimpfungen. Es handelt sich um Schluckimpfungen. Die Immunisierung muss mit der vollendeten 24. (Rotarix) bzw. 32. (RotaTeq) Lebenswoche abgeschlossen sein. Im August 2013 wurde die Rotavirusimpfung in den Impfkalender der STIKO aufgenommen und wird in Deutschland für Säuglinge ab einem Alter von sechs Wochen empfohlen.[29][30] Ohne Impfung erkrankt bis zum fünften Lebensjahr nahezu jedes Kind an Rotaviren.[31] Neben dem Schutz vor der Rotavirusinfektion gibt es in den USA auch Hinweise auf einen Rückgang von Krampfanfällen nach Rotavirusimpfung.[32]
In Indien ist seit 2014 ein dritter, monovalenter Impfstoff zugelassen: Rotavac.[33] RV1, RV5 sowie Rotavac sind von der WHO vorqualifiziert und gelten als sicher und wirksam.[33] Ferner sind in einzelnen Länder weitere Impfstoffe lokal zugelassen.
Eine Schluckimpfung gegen Rotaviren (RotaShield von Wyeth Lederle) wurde 1998 in den USA in den normalen Impfplan aufgenommen, am 15. Oktober 1999 jedoch wieder zurückgezogen, nachdem landesweit 76 Fälle einer Intussuszeption (Darmeinstülpung) aufgetreten waren und ein möglicher Zusammenhang mit der Impfung angegeben wurde. Nach intensiven klinischen Studien sind seit dem 2. Quartal 2006 wieder Rotavirus-Impfungen für Kinder im Alter bis zu sechs Monaten in Europa und den USA zugelassen. Eine klinische Studie zu Rotarix – mit 615 untersuchten Intussuszeptionen aus Brasilien und Mexiko – wurde im Juni 2011 im New England Journal of Medicine publiziert.[34] In der Fallkontrollstudie wurde ein leicht erhöhtes Risiko konstatiert, aber für beide Länder eine positive Nutzen-Risiko-Bilanz.
Laut einer Studie der australischen Therapeutic Goods Administration zeigte sich (ohne Differenzierung des Impfzeitpunkts) ein um den Faktor 3,5 (0,7–10,1) gesteigertes Risiko der Intussuszeption, während für RotaTeq ein um den Faktor 5,3 erhöhtes Risiko (1,1–15,4) gefunden wurde.[35]
Harry Greenberg von der Stanford University deutete im NEJM die Resultate dahingehend, dass „Intussuszeptionen ein prinzipielles Risiko aller Rotavirus-Infektionen sind“, da beide Impfstoffe aus Lebendviren bestehen. Weil eine Impfung zu inapparenten Infektionen führt, könnte es aber sein, dass die Gefahr einer Erkrankung durch die Impfung geringer ist als bei einer Infektion mit dem Wildtyp. Das Risiko gilt aber als sehr gering, auf 100.000 geimpfte Säuglinge dürfte es zu einem bis fünf Zwischenfällen kommen.[36]
Therapie
BearbeitenEine spezielle Therapie existiert nicht, eine Therapie erfolgt rein symptomatisch. Es ist in jedem Fall auf eine ausreichende Flüssigkeitszufuhr (ggf. Elektrolytlösung) – oral oder parenteral – zu achten.[37] Von der Einnahme von Antidiarrhoika ist abzuraten, da diese die Ausscheidung des Erregers erschweren und somit den Krankheitsverlauf verlängern können.
Meldepflicht
BearbeitenDer Nachweis von Rotaviren ist in Deutschland nach § 7 Infektionsschutzgesetz (IfSG) namentlich meldepflichtig, darüber hinaus nach § 6 IfSG Verdacht auf und die Erkrankung […] an einer akuten infektiösen Gastroenteritis, wenn der oder die Betroffene Umgang mit Lebensmittel hat, in einer Gemeinschaftseinrichtung arbeitet oder wenn nach dem epidemischen Zusammenhang ein Ausbruch zu vermuten ist (wenn zwei oder mehr gleichartige Erkrankungen auftreten, bei denen ein epidemischer Zusammenhang wahrscheinlich ist oder vermutet wird).[38] Zudem haben Leitungen von Gemeinschaftseinrichtungen gemäß § 34 Abs. 6 und Abs. 1 IfSG das zuständige Gesundheitsamt unverzüglich zu benachrichtigen, wenn es in ihrer Einrichtung betreute Kinder [gibt], die das 6. Lebensjahr noch nicht vollendet haben und an infektiöser Gastroenteritis erkrankt oder dessen verdächtig sind.
Fußnote
BearbeitenWeblinks
Bearbeiten- Rotavirus-Infektionen – Informationen des Robert Koch-Instituts
- Rotavirus vaccines: WHO position paper – July 2021, WHO, englisch, PDF
Einzelnachweise
Bearbeiten- ↑ a b c d e ICTV: Bluetongue virus, EC 51, Berlin, Germany, July 2019; Email ratification March 2020 (MSL #35)
- ↑ ICTV Master Species List 2018b v1. MSL #34, Feb. 2019.
- ↑ a b c d e f g h i j k l Cornelia Henke-Gendo: Virale Gastroenteritiserreger. In: Sebastian Suerbaum, Gerd-Dieter Burchard, Stefan H. E.Kaufmann, Thomas F. Schulz (Hrsg.): Medizinische Mikrobiologie und Infektiologie. Springer-Verlag, 2016, ISBN 978-3-662-48678-8, S. 513 ff., doi:10.1007/978-3-662-48678-8_65.
- ↑ R. F. Bishop u. a.: Virus particles in epithelial cells of duodenal mucosa from children with acute non-bacterial gastroenteritis. In: Lancet (London). Band 2, Nr. 7841, 8. Dezember 1973, S. 1281–1283, doi:10.1016/s0140-6736(73)92867-5, PMID 4127639.
- ↑ Ulrich Desselberger: Rotaviruses. In: Virus Research. Band 190, 22. September 2014, S. 75–96, doi:10.1016/j.virusres.2014.06.016.
- ↑ International Committee on Taxonomy of Viruses (ICTV). Abgerufen am 13. April 2020 (englisch).
- ↑ a b Carl D. Kirkwood: Genetic and antigenic diversity of human rotaviruses: potential impact on vaccination programs. In: The Journal of Infectious Diseases. 202 Suppl, 1. September 2010, S. S43–48, doi:10.1086/653548, PMID 20684716.
- ↑ Mitsutaka Wakuda u. a.: Porcine rotavirus closely related to novel group of human rotaviruses. In: Emerging Infectious Diseases. Band 17, Nr. 8, August 2011, S. 1491–1493, doi:10.3201/eid1708.101466, PMID 21801631, PMC 3381553 (freier Volltext).
- ↑ Douglas Marthaler u. a.: Widespread rotavirus H in commercially raised pigs, United States. In: Emerging Infectious Diseases. Band 20, Nr. 7, Juli 2014, S. 1195–1198, doi:10.3201/eid2007.140034, PMID 24960190, PMC 4073875 (freier Volltext).
- ↑ Tung G. Phan u. a.: Rotavirus I in feces of a cat with diarrhea. In: Virus Genes. Band 53, Nr. 3, Juni 2017, S. 487–490, doi:10.1007/s11262-017-1440-4, PMID 28255929, PMC 7089198 (freier Volltext).
- ↑ Krisztián Bányai u. a.: Candidate new rotavirus species in Schreiber’s bats, Serbia. In: Infection, Genetics and Evolution. Band 48, 1. März 2017, S. 19–26, doi:10.1016/j.meegid.2016.12.002.
- ↑ Miguel O’Ryan: The ever-changing landscape of rotavirus serotypes. In: The Pediatric Infectious Disease Journal. Band 28, 3 Suppl, März 2009, S. S60–62, doi:10.1097/INF.0b013e3181967c29, PMID 19252426.
- ↑ dort mit H und N klassifiziert
- ↑ a b c d John T. Patton: Rotavirus diversity and evolution in the post-vaccine world. In: Discovery Medicine. Band 13, Nr. 68, Januar 2012, S. 85–97, PMID 22284787, PMC 3738915 (freier Volltext).
- ↑ My V. T. Phan u. a.: Unbiased whole-genome deep sequencing of human and porcine stool samples reveals circulation of multiple groups of rotaviruses and a putative zoonotic infection. In: Virus Evolution. Band 2, Nr. 2, Juli 2016, S. vew027, doi:10.1093/ve/vew027, PMID 28748110, PMC 5522372 (freier Volltext).
- ↑ G. M. Beards, U. Desselberger, T. H. Flewett: Temporal and geographical distributions of human rotavirus serotypes, 1983 to 1988. In: Journal of Clinical Microbiology. Vol. 27, Nr. 12, Dezember 1989, S. 2827–2833, PMID 2556435, PMC 267135 (freier Volltext).
- ↑ Susan Afua Damanka u. a.: Genetic analysis of Ghanaian G1P[8] and G9P[8] rotavirus A strains reveals the impact of P[8] VP4 gene polymorphism on P-genotyping. In: PLOS ONE. Band 14, Nr. 6, 26. Juni 2019, S. e0218790, doi:10.1371/journal.pone.0218790, PMID 31242245, PMC 6594640 (freier Volltext).
- ↑ Hiroshi Suzuki: Rotavirus Replication: Gaps of Knowledge on Virus Entry and Morphogenesis. In: The Tohoku Journal of Experimental Medicine. Band 248, Nr. 4, August 2019, S. 285–296, doi:10.1620/tjem.248.285, PMID 31447474.
- ↑ D. S. Prince u. a.: Aerosol transmission of experimental rotavirus infection. In: Pediatric Infectious Disease. Band 5, Nr. 2, März 1986, S. 218–222, doi:10.1097/00006454-198603000-00012, PMID 3005999.
- ↑ Simone Richardson, Keith Grimwood, Rebecca Gorrell, Enzo Palombo, Graeme Barnes: Extended excretion of rotavirus after severe diarrhoea in young children. In: The Lancet. Band 351, Nr. 9119, 20. Juni 1998, S. 1844–1848, doi:10.1016/s0140-6736(97)11257-0.
- ↑ Shou-Chien Chen, Lia-Beng Tan, Li-Min Huang, Kow-Tong Chen: Rotavirus infection and the current status of rotavirus vaccines. In: Journal of the Formosan Medical Association. Band 111, Nr. 4, 1. April 2012, S. 183–193, doi:10.1016/j.jfma.2011.09.024.
- ↑ S. A. Ansari, V. S. Springthorpe, S. A. Sattar: Survival and vehicular spread of human rotaviruses: possible relation to seasonality of outbreaks. In: Reviews of Infectious Diseases. Band 13, Nr. 3, 1. Juni 1991, S. 448–461, PMID 1866549.
- ↑ Robert Koch-Institut: SurvStat@RKI 2.0. Abgerufen am 31. Mai 2016.
- ↑ Rotavirus. In: WHO. Abgerufen am 16. August 2022 (englisch).
- ↑ Jacqueline E. Tate et al.: Global, Regional, and National Estimates of Rotavirus Mortality in Children. In: Clinical Infectious Diseases: An Official Publication of the Infectious Diseases Society of America. 62 Suppl 2, 1. Mai 2016, S. S96–S105, doi:10.1093/cid/civ1013, PMID 27059362 (englisch).
- ↑ Sandra Niendorf: Noro- und Rotavirusinfektionen – die aktuelle Situation in Deutschland. (PDF) In: RKI. 4. November 2015, S. 26, abgerufen am 16. September 2022.
- ↑ Rotaviren-Impfung bei Kindern. In: impfen-info.de; umfassende Informationen der Bundeszentrale für gesundheitliche Aufklärung (BZgA) zum Thema Impfungen. Abgerufen am 16. September 2022.
- ↑ Rotavirus-Impfstoffe. Paul-Ehrlich-Institut, 23. März 2020, abgerufen am 13. April 2020.
- ↑ Neuer Impfkalender: Experten raten zur Impfung gegen Rotaviren. In: Spiegel Online. 26. August 2013, abgerufen am 21. Januar 2015.
- ↑ Epidemiologisches Bulletin 35/2013 (PDF) Robert Koch-Institut.
- ↑ Matthias Thalhammer, Lisa Demel: Rotavirus - Impfung. In: Netdoktor.at. 1. April 2011, abgerufen am 9. Dezember 2018.
- ↑ D. C. Payne, J. Baggs u. a.: Protective association between rotavirus vaccination and childhood seizures in the year following vaccination in US children. In: Clinical infectious diseases. Band 58, Nummer 2, Januar 2014, S. 173–177, ISSN 1537-6591. doi:10.1093/cid/cit671. PMID 24265355.
- ↑ a b Karla Soares-Weiser u. a.: Vaccines for preventing rotavirus diarrhoea: vaccines in use. In: The Cochrane Database of Systematic Reviews. Band 2019, Nr. 10, 28. Oktober 2019, doi:10.1002/14651858.CD008521.pub5, PMID 31684685, PMC 6816010 (freier Volltext).
- ↑ M. M. Patel, V. R. López-Collada u. a.: Intussusception risk and health benefits of rotavirus vaccination in Mexico and Brazil. In: The New England Journal of Medicine. Band 364, Nummer 24, Juni 2011, S. 2283–2292, doi:10.1056/NEJMoa1012952. PMID 21675888.
- ↑ J. P. Buttery, M. H. Danchin u. a.: Intussusception following rotavirus vaccine administration: post-marketing surveillance in the National Immunization Program in Australia. In: Vaccine. Band 29, Nummer 16, April 2011, S. 3061–3066, doi:10.1016/j.vaccine.2011.01.088. PMID 21316503.
- ↑ Rotavirus-Impfung: Studien bestätigen minimales Risiko von Intussuszeptionen. In: Deutsches Ärzteblatt. 10. Februar 2014, abgerufen am 13. April 2020.
- ↑ Wolfgang Jilg: Rotavirus. In: Heinz Spiess, Ulrich Heininger, Wolfgang Jilg (Hrsg.): Impfkompendium. 8. Auflage. Georg Thieme Verlag, 2015, ISBN 978-3-13-498908-3, S. 267 ff.
- ↑ Rotaviren-Gastroenteritis. In: RKI-Ratgeber für Ärzte. Robert Koch-Institut, 1. Mai 2010, abgerufen am 18. März 2020.