Wasserstoff
Wasserstoff ist ein chemisches Element mit dem Symbol H (für lateinisch Hydrogenium „Wasserbildner“) und der Ordnungszahl 1. Im Periodensystem steht das Element Wasserstoff in der 1. Periode und in der 1. IUPAC-Gruppe.
| Eigenschaften | |||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Allgemein | |||||||||||||||||||||||||
| Name, Symbol, Ordnungszahl | Wasserstoff, H, 1 | ||||||||||||||||||||||||
| Elementkategorie | Nichtmetalle | ||||||||||||||||||||||||
| Gruppe, Periode, Block | 1, 1, s | ||||||||||||||||||||||||
| Aussehen | farbloses Gas (H2) | ||||||||||||||||||||||||
| CAS-Nummer |
| ||||||||||||||||||||||||
| EG-Nummer | 215-605-7 | ||||||||||||||||||||||||
| ECHA-InfoCard | 100.014.187 | ||||||||||||||||||||||||
| Massenanteil an der Erdhülle | 0,9 % (9. Rang)[1] | ||||||||||||||||||||||||
| Atomar[2] | |||||||||||||||||||||||||
| Atommasse | 1,008 (1,00784–1,00811)[3][4] u | ||||||||||||||||||||||||
| Atomradius (berechnet) | 25 (53) pm | ||||||||||||||||||||||||
| Kovalenter Radius | 31 pm | ||||||||||||||||||||||||
| Van-der-Waals-Radius | 120 pm | ||||||||||||||||||||||||
| Elektronenkonfiguration | 1s1 | ||||||||||||||||||||||||
| 1. Ionisierungsenergie | 13.59843449(8) eV[5] ≈ 1312.05 kJ/mol[6] | ||||||||||||||||||||||||
| Physikalisch[2] | |||||||||||||||||||||||||
| Aggregatzustand | gasförmig (H2) | ||||||||||||||||||||||||
| Dichte | gasförmig: 0,0899 kg/m3 bei 273 K[7] flüssig: 0,0709 g/cm3 bei 20,324 K | ||||||||||||||||||||||||
| Magnetismus | diamagnetisch (χm = −2,2 · 10−9)[8] | ||||||||||||||||||||||||
| Schmelzpunkt | 14,01 K (−259,14 °C) | ||||||||||||||||||||||||
| Siedepunkt | 21,15 K[9] (−252 °C) | ||||||||||||||||||||||||
| Molares Volumen | fest: 11,42 · 10−6 m3·mol−1 | ||||||||||||||||||||||||
| Verdampfungsenthalpie | 0,90 kJ·mol−1[9] | ||||||||||||||||||||||||
| Schmelzenthalpie | 0,558 kJ·mol−1 | ||||||||||||||||||||||||
| Schallgeschwindigkeit | 1270 m·s−1 bei 298,15 K | ||||||||||||||||||||||||
| Spezifische Wärmekapazität | 14304 J·kg−1·K−1 | ||||||||||||||||||||||||
| Wärmeleitfähigkeit | 0,1805 W·m−1·K−1 | ||||||||||||||||||||||||
| Chemisch[2] | |||||||||||||||||||||||||
| Oxidationszustände | −1, ±0, +1 | ||||||||||||||||||||||||
| Normalpotential | 0 V (Referenz: 2 H+ + 2 e− ⇌ H2) | ||||||||||||||||||||||||
| Elektronegativität | 2,2 (Pauling-Skala) | ||||||||||||||||||||||||
| Isotope | |||||||||||||||||||||||||
| |||||||||||||||||||||||||
| Weitere Isotope siehe Liste der Isotope | |||||||||||||||||||||||||
| NMR-Eigenschaften | |||||||||||||||||||||||||
| |||||||||||||||||||||||||
| Sicherheitshinweise | |||||||||||||||||||||||||
| |||||||||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | |||||||||||||||||||||||||
Wasserstoff ist mit einem Massenanteil von etwa 70 % das häufigste chemische Element im Universum, jedoch nicht auf der Erde, wo sein Massenanteil an der Erdhülle nur 0,87 % beträgt.[11]
Der Großteil des Wasserstoffs auf der Erde ist im Wasser gebunden, der Verbindung mit Sauerstoff, deren Masse zu 11 % aus Wasserstoff besteht. Wasserstoff kommt gebunden an andere Elemente in sämtlichen Pflanzen und lebenden Organismen vor. Wasserstoff ist ein fester Bestandteil fast aller organischen chemischen Substanzen.
Wasserstoff ist das chemische Element mit der geringsten Atommasse. Sein häufigstes Isotop, Protium, ist das einzige stabile Isotop ohne ein Neutron. Es besteht nur aus einem Proton und einem Elektron. Es existieren zwei weitere natürlich vorkommende Wasserstoffisotope, von denen das nicht-radioaktive Deuterium 0,0156 % des natürlichen Wasserstoffs ausmacht, während das in den oberen Schichten der Atmosphäre gebildete radioaktive Tritium nur in kleinsten Mengen vorkommt.[11][12]
Unter Bedingungen, die normalerweise auf der Erde herrschen (siehe Normalbedingungen), liegt das gasförmige Element Wasserstoff nicht als atomarer Wasserstoff mit dem Symbol H vor, sondern als molekularer Wasserstoff mit dem Symbol H2, als ein farb- und geruchloses Gas. Wenn z. B bei Redoxreaktionen Wasserstoff neu gebildet wird, tritt das Element vorübergehend atomar als H auf und wird als naszierender Wasserstoff bezeichnet. In dieser reaktiven Form reagiert Wasserstoff besonders gut mit anderen Verbindungen oder Elementen.
Geschichte
Entdeckt wurde Wasserstoff vom englischen Chemiker und Physiker Henry Cavendish im Jahre 1766, als er mit Metallen (Eisen, Zink und Zinn) und Säuren experimentierte. Cavendish nannte das dabei entstandene Gas wegen seiner Brennbarkeit „inflammable air“ („brennbare Luft“). Er untersuchte das Gas eingehend und veröffentlichte seine Erkenntnisse.[13] Auf ähnliche Weise (Einwirkung von Säuren auf Metalle) hatten allerdings schon im 17. Jahrhundert Théodore Turquet de Mayerne (um 1620) und Robert Boyle (um 1670) ein Gas erzeugt, das sie Knallgas genannt hatten. Eine genauere Analyse erfolgte aber erst durch Antoine Laurent de Lavoisier, der erkannte, dass bei der Verbrennung des Gases Wasser entstand und deshalb das brennbare Gas als „hydrogène“ bezeichnete (lateinisch hydrogenium: „Wasser erzeugender Stoff“, davon kurz „Hydrogen“; von altgriechisch ὕδωρ hydōr „Wasser“ und -gen) und ihm damit seinen heutigen Namen gab. Cavendish hatte inzwischen – eine Beobachtung von Joseph Priestley aufgreifend – erkannt, dass bei der Verbrennung von Wasserstoff Wasser entsteht (veröffentlicht erst 1784).[14] Lavoisier erfuhr von den Experimenten von Cavendish beim Besuch von dessen Assistenten Charles Blagden 1783. Cavendish war Anhänger der Phlogistonlehre und sein Wasserstoff war für ihn ein Kandidat für diese hypothetische Substanz. Lavoisier aber zeigte in aufsehenerregenden Experimenten, dass das Gas ein eigenständiges Element war und ein Bestandteil des Wassers, das man damals vielfach noch selbst für elementar hielt, gemäß der alten Vier-Elemente-Lehre. Lavoisier führte seine Experimente quantitativ aus unter Verwendung der von ihm postulierten Massenerhaltung. Er leitete Wasserdampf in einer abgeschlossenen Apparatur über glühende Eisenspäne und ließ die entstandenen Gase an anderer Stelle kondensieren. Dabei stellte er fest, dass die Masse des kondensierten Wassers etwas geringer war als die der ursprünglich eingesetzten Masse. Dafür war ein Gas entstanden, dessen Masse zusammen mit dem Gewichtszuwachs des oxidierten Eisens genau der „verloren gegangenen“ Wassermenge entsprach. Sein eigentliches Experiment war also erfolgreich.
Lavoisier untersuchte das entstandene Gas weiter und führte die als Knallgasprobe bekannte Untersuchung durch, wobei das Gas verbrannte. Er nannte es daher zunächst wie Cavendish brennbare Luft (im Französischen in umgekehrter Wortstellung „air inflammable“). Als er in weiteren Experimenten zeigte, dass sich aus dem Gas umgekehrt Wasser erzeugen lässt, taufte er es hydro-gène (griechisch: hydro = Wasser; genes = erzeugend). Das Wort bedeutet demnach: „Wassererzeuger“. Die deutsche Bezeichnung lässt auf die gleiche Begriffsherkunft schließen.
Nachdem man gemäß der Schule von Lavoisier lange Sauerstoff für den Säurecharakter verantwortlich gemacht hatte, änderte sich dies, als Humphry Davy 1808 Chlorwasserstoff darstellte und nachwies, dass darin kein Sauerstoff enthalten war. Danach erkannte man, dass statt Sauerstoff Wasserstoff für den Säurecharakter verantwortlich war.
Vorkommen
Wasserstoff ist das häufigste chemische Element in der Sonne und den großen Gasplaneten Jupiter, Saturn, Uranus und Neptun, die über 99,99 % der Masse des Sonnensystems in sich vereinen. Wasserstoff stellt 75 % der gesamten Masse beziehungsweise 93 % aller Atome des Sonnensystems. Im gesamten Weltall wird (unter Nichtbeachtung dunkler Materie) ein noch höherer Anteil an Wasserstoff vermutet.
Vorkommen im Universum
Kurz nach der Entstehung des Universums waren nach der mutmaßlichen Vernichtung der Antimaterie durch ein geringes Übermaß der Materie und der Kondensation eines Quark-Gluon-Plasmas zu Baryonen nur mehr Protonen und Neutronen (nebst Elektronen) vorhanden. Bei den vorherrschenden hohen Temperaturen vereinigten sich diese zu leichten Atomkernen, wie 2H und 4He. Die meisten Protonen blieben unverändert und stellten die zukünftigen 1H-Kerne dar. Nach ungefähr 380.000 Jahren war die Strahlungsdichte des Universums so gering geworden, dass sich Wasserstoff-Atome einfach durch Zusammenschluss der Kerne mit den Elektronen bilden konnten, ohne gleich wieder durch ein Photon auseinandergerissen zu werden.
Mit der weitergehenden Abkühlung des Universums formten sich unter dem Einfluss der Gravitation und ausgehend von räumlichen Dichteschwankungen allmählich Wolken aus Wasserstoffgas, die sich zunächst großräumig zu Galaxien und darin zu Protosternen zusammenballten. Unter dem wachsenden Druck der Schwerkraft setzte schließlich die Kernfusion ein, bei der Wasserstoff zu Helium verschmilzt. So entstanden erste Sterne und später die Sonne.
Sterne bestehen weit überwiegend aus Wasserstoff-Plasma. Die Kernfusion von Wasserstoff 1H zu Helium 4He erfolgt hauptsächlich über die Zwischenstufen Deuterium 2H und Helium 3He oder über den Bethe-Weizsäcker-Zyklus. Die dabei frei werdende Energie ist die Energiequelle der Sterne. Der in unserer Sonne enthaltene Wasserstoff macht den größten Teil der gesamten Masse unseres Sonnensystems aus.
Die Gasplaneten bestehen zu großen Teilen aus Wasserstoff. Unter den extremen Drücken, die in großen Tiefen in den großen Gasplaneten Jupiter und Saturn herrschen, kann er in metallischer Form existieren. Dieser „metallische“ Kern ist elektrisch leitfähig und erzeugt vermutlich das Magnetfeld der Gasplaneten.
Außerhalb von Sternensystemen kommt Wasserstoff in Gaswolken vor. In den so genannten H-I-Gebieten liegt das Element atomar und nichtionisiert vor. Diese Gebiete emittieren Strahlung von etwa 1420 MHz, die sogenannte 21-cm-Linie, auch HI- oder Wasserstofflinie genannt, die von Übergängen des Gesamtdrehimpulses herrührt. Sie spielt eine wichtige Rolle in der Astronomie und dient dazu, Wasserstoffvorkommen im All zu lokalisieren und zu untersuchen.
Ionisierte Gaswolken mit atomarem Wasserstoff nennt man dagegen H-II-Gebiete. In diesen Gebieten senden Sterne hohe Mengen ionisierender Strahlung aus. Mit Hilfe der H-II-Gebiete lassen sich Rückschlüsse auf die Zusammensetzung der interstellaren Materie ziehen. Wegen ständiger Ionisation und Rekombination der Atome senden sie mitunter sichtbare Strahlung aus, die oft so stark ist, dass man diese Gaswolken mit einem kleinen Fernrohr sehen kann.
Irdische Vorkommen
Auf der Erde ist der Massenanteil wesentlich geringer. Bezogen auf die Erd-Gesamtmasse ist der Anteil etwa 0,03 %.[15] Außerdem liegt der irdische Wasserstoff im Gegensatz zu den Vorkommen im All überwiegend gebunden und nur selten in reiner Form als unvermischtes Gas vor. Die bekannteste Verbindung ist das Wasser. Neben diesem sind Erdgase wie Methan sowie Erdöl wichtige wasserstoffhaltige Verbindungen auf der Erde. In mehr als der Hälfte aller bisher bekannten Minerale ist Wasserstoff (meist als Kristallwasser) enthalten.[16]
Der größte Anteil des Wasserstoffs an der Erdoberfläche kommt in der Verbindung Wasser vor. In dieser Form bedeckt er über zwei Drittel der Erdoberfläche. Die gesamten Wasservorkommen der Erde belaufen sich auf circa 1,386 Milliarden km³. Davon entfallen 1,338 Milliarden km³ (96,5 %) auf Salzwasser in den Ozeanen. Die verbliebenen 3,5 % liegen als Süßwasser vor. Davon befindet sich wiederum der größte Teil im festen Aggregatzustand: in Form von Eis in der Arktis und Antarktis sowie in den Permafrostböden vor allem in Sibirien. Der geringe restliche Anteil ist flüssiges Süßwasser und findet sich meist in Seen und Flüssen, aber auch als Grundwasser.
In der Erdatmosphäre liegt Wasserstoff hauptsächlich als gasförmiges Wasser (Wasserdampf) vor. Wie viel Wasserdampf eine Volumeneinheit Luft enthält, hängt neben dem Vorhandensein von Wasser von der Lufttemperatur ab. Beispielsweise kann Luft von 30 °C Temperatur bis zu einem Volumenanteil von 4,2 % Wasserdampf aufnehmen. Die relative Luftfeuchtigkeit beträgt dann 100 %, da der Sättigungsdampfdruck des Wassers erreicht ist.
Die Häufigkeit von molekularem Wasserstoff in der Atmosphäre beträgt nur 0,55 ppm. Dieser niedrige Anteil kann mit der hohen thermischen Geschwindigkeit der Moleküle und dem hohen Anteil an Sauerstoff in der Atmosphäre erklärt werden. Bei der mittleren Temperatur der Atmosphäre bewegen sich die H2-Teilchen im Durchschnitt mit fast 2 km/s. Das ist rund ein Sechstel der Fluchtgeschwindigkeit auf der Erde. Aufgrund der Maxwell-Boltzmann-Verteilung der Geschwindigkeiten der H2-Moleküle gibt es aber dennoch eine beträchtliche Zahl von Molekülen, welche die Fluchtgeschwindigkeit erreichen. Die Moleküle haben jedoch nur eine extrem geringe freie Weglänge, sodass nur Moleküle in den oberen Schichten der Atmosphäre tatsächlich entweichen. Weitere H2-Moleküle kommen aus darunter liegenden Schichten nach, und es entweicht wieder ein bestimmter Anteil, bis letztlich nur noch Spuren des Elements in der Atmosphäre vorhanden sind. Zudem wird der Wasserstoff in den unteren Schichten der Atmosphäre durch eine photoaktivierte Reaktion mit Sauerstoff zu Wasser verbrannt. Bei einem geringen Anteil stellt sich ein Gleichgewicht zwischen Verbrauch und Neuproduktion (durch Bakterien und photonische Spaltung des Wassers) ein.
Gewinnung
Molekularer Wasserstoff
Kleinere Mengen Wasserstoff können bei Schauversuchen durch Reaktionen von verdünnten Säuren mit unedlen Metallen wie Zink gewonnen werden. Für die Reaktion gilt schematisch:
Bei dieser Reaktion handelt es sich um eine Redoxreaktion, in der das Zink als Reduktionsmittel wirkt und die Protonen der Säure durch Abgabe von Elektronen zum elementaren Wasserstoff reduziert, während das Zink nach Abgabe der Elektronen als kationisches Zink mit dem Anion der Säure ein Zinksalz bildet. Wenn bei dieser Reaktion die Temperatur erhöht wird oder wenn gar an Stelle von Zink Alkalimetalle als sehr starke Reduktionsmittel verwendet werden, dann bildet sich Wasserstoff bereits mit schwachen Säuren, wie z. B. Wasser. Das ist der Grund dafür, dass Metallbrände niemals mit Wasser gelöscht werden dürfen, denn gebildeter Wasserstoff würde dann als Brandverstärker wirken.[11]
Das wichtigste großtechnische Verfahren zur industriellen Gewinnung von molekularem Wasserstoff ist die um 1920 entwickelte Dampfreformierung. Bei dieser Reaktion werden unter hoher Temperatur und hohem Druck Kohlenwasserstoffe wie Methan und andere als Reduktionsmittel für die Protonen des Wassers eingesetzt. Dabei entsteht zunächst ein sogenanntes Synthesegas, ein Gemisch aus Kohlenstoffmonoxid und Wasserstoff. Das Mengenverhältnis der Reaktionsprodukte kann anschließend mit der sogenannten Wassergas-Shift-Reaktion zu Gunsten von Wasserstoff zwar noch verbessert werden, jedoch entsteht dabei unerwünschtes Kohlendioxid und der Wirkungsgrad (Erdgas zu Wasserstoff) erreicht nur etwa 60 bis 70 %.[11]
Derzeit gewinnt im Rahmen der Debatte um die Vermeidung von Kohlendioxid und um die Power-to-Gas-Strategie die Wasserelektrolyse als Methode zur Herstellung von Wasserstoff immer mehr an Bedeutung. Bei der Wasserelektrolyse wird Wasser in einer elektrochemischen Redoxreaktion durch Zufuhr von elektrischer Energie in die Bestandteile Wasserstoff und Sauerstoff zerlegt.
- Wasser wird durch elektrischen Strom in Wasserstoff und Sauerstoff gespalten.
Atomarer Wasserstoff
Atomarer Wasserstoff kann durch Zufuhr der Dissoziationsenergie aus dem molekularen Element erzeugt werden. Methodisch wird dieses bewerkstelligt durch Erhitzung auf mehrere tausend Grad, elektrische Entladung bei hoher Stromdichte und niedrigem Druck, Bestrahlung mit Ultraviolettlicht, Beschuss mit Elektronen bei 10 bis 20 Elektronenvolt oder Mikrowellenstrahlung. Allerdings reagiert atomarer Wasserstoff (z. B. an Behälterwänden) sehr schnell wieder zu molekularem Wasserstoff. Es stellt sich somit ein Fließgleichgewicht ein, das in der Regel weit auf der Seite des molekularen Wasserstoffs liegt.
- [17]
- Durch Energiezufuhr dissoziiert molekularer Wasserstoff in die atomare Form. Diese Reaktion beginnt ab 1500 K und ist vollständig bei 3000 K.
Zur Darstellung von größeren Mengen atomaren Wasserstoffs sind das Woodsche Darstellungsverfahren (Robert Williams Wood, 1898) und dasjenige von Irving Langmuir, die Langmuir-Fackel besonders geeignet.
Physikalische Eigenschaften
Wasserstoff ist das Element mit der geringsten Dichte. Molekularer Wasserstoff (H2) ist etwa 14,4-mal weniger dicht als Luft. Flüssiger Wasserstoff wiegt je nach Temperatur zwischen 77,00 und 31,26 Gramm pro Liter.[18] Sein Schmelzpunkt liegt bei 14,02 K (−259 °C), der Siedepunkt bei 21,15 K (−252 °C). Wasserstoff ist in Wasser und anderen Lösungsmitteln schlecht löslich. Für Wasser beträgt die Löslichkeit 19,4 ml/l (1,6 mg/l)[7] bei 20 °C und Normaldruck. Dagegen ist die Löslichkeit (genauer: maximale Volumenkonzentration) in Metallen deutlich höher.
Einige thermodynamische Eigenschaften (Transportphänomene) sind aufgrund der geringen Molekülmasse und der daraus resultierenden hohen mittleren Geschwindigkeit der Wasserstoffmoleküle (1770 m/s bei 25 °C) von besonderer Bedeutung, wie z. B. beim Oberth-Effekt-Raketentreibstoff. Der Joule-Thomson-Koeffizient von Wasserstoff ist bei Raumtemperatur negativ (Joule-Thomson-Effekt). Das bedeutet, dass bei einer Isenthalpen Entspannung des Drucks das Gas bei dieser Temperatur im Gegensatz zu den meisten anderen Gasen nicht abkühlt, sondern erwärmt. Wasserstoff besitzt bei Raumtemperatur das höchste Diffusionsvermögen, die höchste Wärmeleitfähigkeit und die höchste Effusionsgeschwindigkeit aller Gase. Eine geringere Viskosität weisen nur drei- oder mehratomige reale Gase wie Butan auf.
Die Mobilität des Wasserstoffs in einer festen Matrix ist, bedingt durch den geringen Molekülquerschnitt, ebenfalls sehr hoch. So diffundiert Wasserstoff durch Materialien wie Polyethylen und glühendes Quarzglas. Ein sehr wichtiges Phänomen ist die außerordentlich hohe Diffusionsgeschwindigkeit in Eisen, Platin und einigen anderen Übergangsmetallen, da es dort dann zur Wasserstoffversprödung kommt. In Kombination mit einer hohen Löslichkeit treten bei einigen Werkstoffen extrem hohe Permeationsraten auf. Hieraus ergeben sich technische Nutzungen zur Wasserstoffanreicherung, aber auch technische Probleme beim Transportieren, Lagern und Verarbeiten von Wasserstoff und Wasserstoffgemischen, da nur Wasserstoff diese räumlichen Begrenzungen durchwandert (siehe Sicherheitshinweise).
389 nm (kaum erkennbar), 397 nm (schwach violett), 410 nm (violett), 434 nm (indigo), 486 nm (türkis) und 656 nm (rot)
Wasserstoff hat ein Linienspektrum und je nach Temperatur des Gases im sichtbaren Bereich ein mehr oder weniger ausgeprägtes kontinuierliches Spektrum. Letzteres ist beim Sonnenspektrum besonders ausgeprägt. Die ersten Spektrallinien im sichtbaren Bereich, zusammengefasst in der so genannten Balmer-Serie, liegen bei 656 nm, 486 nm, 434 nm und 410 nm. Daneben gibt es weitere Serien von Spektrallinien im Infrarot- (Paschen-Serie, Brackett-Serie und Pfund-Serie) und eine im Ultraviolettbereich (Lyman-Serie) des elektromagnetischen Spektrums. Eine besondere Bedeutung in der Radioastronomie hat die 21-Zentimeter-Linie (HI-Linie) in der Hyperfeinstruktur.
In einem magnetischen Feld verhält sich H2 sehr schwach diamagnetisch. Das bedeutet, die Dichte der Feldlinien eines extern angelegten Magnetfeldes nimmt in der Probe ab. Die magnetische Suszeptibilität ist bei Normdruck = -2.2e-9 und typischerweise einige Größenordnungen unter der von diamagnetischen Festkörpern.
Gegenüber elektrischem Strom ist H2 ein Isolator. In einem elektrischen Feld hat er eine Durchschlagsfestigkeit von mehreren Millionen Volt pro Meter.
Der empirische Atomradius von (atomarem) Wasserstoff beträgt 25 pm, der kovalente Radius 31 pm und der Van-der-Waals-Radius 120 pm.[6] In höchstangeregten Wasserstoffatomen (Rydberg-Zuständen), wie sie unter den Vakuumbedingungen interstellarer Nebel vorkommen, befinden sich deren Elektronen auf Bahnen mit Atomradien von bis zu 0,339 Millimetern.[19]
Aggregatzustände
Bei Temperaturen unterhalb von 21,15 K (−252 °C) kondensiert Wasserstoff zu einer klaren, farblosen Flüssigkeit. Dieser Zustand wird als LH2 abgekürzt (engl. liquid, „flüssig“). Unterhalb von 14,02 K (−259,2 °C) bildet Wasserstoff einen kristallinen Festkörper mit hexagonal dichtester Kugelpackung (hcp), dort ist jedes Molekül von zwölf weiteren umgeben. Am Gefrierpunkt bildet sich beim Abkühlen ein schlammartiges Zweiphasengemisch, ein sogenannter Slush.
Anders als bei Helium tritt beim Verflüssigen von einfachem Wasserstoff ( 1H) keine Suprafluidität auf; prinzipiell kann aber das Isotop Deuterium ( 2H) suprafluid werden.
Der Tripelpunkt des Wasserstoffs, bei dem seine drei Aggregatzustände gleichzeitig vorkommen, ist einer der Fixpunkte der Internationalen Temperaturskala. Er liegt bei einer Temperatur von 13,8033 K[20] und einem Druck von 7,042 kPa.[20] Der kritische Punkt liegt bei 33,18 K[20] und 13,0 bar,[20] die kritische Dichte beträgt 0,03012 g/cm³[17] (die niedrigste kritische Dichte aller Elemente).
Unter extremen Drücken, wie sie innerhalb von Gasplaneten herrschen, wird wahrscheinlich metallischer Wasserstoff, d. h. in metallischer Form, ausgebildet. Dabei wird er elektrisch leitend (vgl. Leitungsband).
Atom- und kernphysikalische Eigenschaften
Ein einzelnes Wasserstoffatom besteht aus einem positiv geladenen Kern und einem negativ geladenen Elektron, das über die Coulomb-Wechselwirkung an den Kern gebunden ist. Dieser besteht stets aus einem einzelnen Proton (Hauptisotop 1H) und seltener je nach Isotop einem oder zwei zusätzlichen Neutronen (2H bzw. 3H-Isotop). Das Wasserstoffatom 1H spielte aufgrund seines einfachen Aufbaus in der Entwicklung der Atomphysik als „Modellatom“ eine herausragende Rolle.
So entstand 1913 aus Untersuchungsergebnissen am Wasserstoff das bohrsche Atommodell, mit dessen Hilfe eine vergleichsweise einfache Beschreibung vieler Eigenschaften des Wasserstoffatoms möglich ist. Man stellt sich dazu vor, dass das Elektron den Kern auf einer bestimmten Kreisbahn umläuft. Nach Bohr kann das Elektron auch auf andere, im Abstand zum Kern genau definierte Bahnen springen, so auf weiter außen liegende, wenn ihm die dazu nötige Energie zugeführt wird (z. B. durch Stöße im erhitzten Gas oder in der elektrischen Gasentladung). Beim Rücksprung von einer äußeren auf eine innere Bahn wird jeweils eine elektromagnetische Strahlung oder Welle einer bestimmten, der frei werdenden Energie entsprechende Wellenlänge abgegeben. Mit diesem Modell lassen sich die Spektrallinien des H-Atoms erklären, die im sichtbaren Licht bei Wellenlängen von 656 nm, 486 nm, 434 nm und 410 nm liegen (Balmer-Serie); im ultravioletten Bereich liegt die Lyman-Serie mit Wellenlängen von 122 nm, 103 nm, 97 nm und 95 nm. Wichtige Serien im Infraroten sind die Paschen-Serie (1,9 μm; 1,3 μm; 1,1 μm und 1 μm) und die Brackett-Serie (4,1 μm; 2,6 μm; 2,2 μm und 1,9 μm) (in allen Serien sind hier nur die ersten vier Linien angegeben). Das Bohrsche Modell reicht aber bei der Betrachtung von Details und für andere Atome zur Erklärung der dabei beobachteten bzw. gemessenen Phänomene nicht aus.
Physikalisch korrekter ist die quantenmechanische Beschreibung, die dem Elektron anstelle der flachen bohrschen Bahnen räumlich ausgedehnte Atomorbitale zuschreibt. Das H-Atom ist das einzige, für das sich das Eigenwertproblem sowohl der nichtrelativistischen Schrödingergleichung als auch der relativistischen Diracgleichung analytisch, das heißt ohne den Einsatz numerischer Verfahren, lösen lässt. Das ist sonst nur für die ebenfalls ausgiebig untersuchten wasserstoffähnlichen Ionen möglich, denen lediglich ein Elektron verblieben ist (He+, Li2+ usw. bis U91+).
Andere quantenmechanische Phänomene bewirken weitere Effekte. Die Feinstruktur der Spektrallinien kommt u. a. daher, dass Bahndrehimpuls und Spin des Elektrons miteinander koppeln. Berücksichtigt man darüber hinaus den Kernspin, kommt man zur Hyperfeinstruktur. Eine sehr kleine, aber physikalisch besonders interessante Korrektur ist die Lambverschiebung durch elektromagnetische Vakuumfluktuationen. Durch all diese Korrekturen wird bereits das Spektrum des Wasserstoffs zu einem komplexen Phänomen, dessen Verständnis viel theoretisches Wissen in Quantenmechanik und Quantenelektrodynamik erfordert.
Isotope
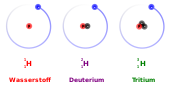
Es existieren drei natürlich vorkommende Isotope des Wasserstoffs. Von allen Elementen unterscheiden sich beim Wasserstoff die Isotope in ihren chemischen Reaktionsfähigkeiten am deutlichsten voneinander. Das liegt an dem vergleichsweise großen Unterschied der Atommasse (Deuterium 2H doppelt, Tritium 3H dreimal so schwer wie Wasserstoff 1H).
- Das einfachste Wasserstoff-Isotop 1H besitzt lediglich ein Proton im Kern und wird daher gelegentlich Protium genannt. Es hat mit einer relativen Häufigkeit von 99,98 % den weitaus größten Anteil am irdisch vorkommenden Wasserstoff. Es ist nicht radioaktiv, also stabil.
- Das Isotop 2H hat neben dem Proton ein Neutron im Kern. Man bezeichnet es als Deuterium. Für Deuterium gibt es das D als ein eigenes Elementsymbol.[21] Verwendung findet es z. B. als Bestandteil von Lösungsmitteln für die 1H-NMR Spektroskopie, da es dabei kein störendes Nebensignal liefert. Es macht 0,015 % aller Wasserstoffatome aus. Deuterium ist ebenfalls stabil.
- Das Isotop 3H hat neben dem Proton zwei Neutronen im Kern. Man bezeichnet es als Tritium mit dem Elementsymbol T. Es hat nur einen verschwindenden Anteil am gesamten in der Natur vorkommenden Wasserstoff. Es ist radioaktiv und zerfällt durch Betazerfall (β−) mit einer Halbwertszeit von 12,32 Jahren in 3He. Tritium wird durch Kernreaktionen in der oberen Erdatmosphäre ständig als kosmogenes Radionuklid gebildet.[22] Im Gleichgewicht von natürlicher Produktion und Zerfall befinden sich ca. 3,5 kg Tritium in der Biosphäre. Tritium kann in Oberflächenwassern und in Lebewesen nachgewiesen werden.
- Die schwereren Isotope 4H, 5H, 6H und 7H haben sehr kurze Lebensdauern in der Größenordnung von 10−22 s bis 10−21 s.
Kernspinzustände im H2-Molekül
Unter normalen Bedingungen ist Wasserstoffgas H2 ein Gemisch von Molekülen, die sich durch die Symmetrie ihrer Kernspins voneinander unterscheiden: ortho- und para-Wasserstoff (kurz o- und p-Wasserstoff). Bei o-Wasserstoff haben die Kernspins symmetrische Konfiguration, daher Gesamtspin S = 1 und für die Molekülrotation nur ungerade Quantenzahlen J = 1, 3 … Beim p-Wasserstoff nehmen die Kernspins einen antisymmetrischen Zustand ein, bilden also den Gesamtspin S = 0 und haben für die Molekülrotation nur gerade Quantenzahlen J = 0, 2 … Mit J = 0 ist p-Wasserstoff die energieärmste Form, also der Grundzustand. Der erste angeregte Zustand ist bei 15,1 meV Energie o-Wasserstoff mit J = 1.
Nahe dem absoluten Nullpunkt T = 0 K findet man im thermodynamischen Gleichgewicht ausschließlich p-Wasserstoff, für nicht zu kaltes Wasserstoffgas ein Gemisch aus der p- und der o-Form. Da es für Gesamtspin S = 0 nur einen Spinzustand gibt, bei symmetrischen Kernspins (S = 1) aber drei Zustände verschiedener Orientierung im Raum, überwiegen diese ab etwa T > 200 K im Gleichgewicht im Verhältnis ortho/para-Wasserstoff von bis zu 3:1. Weiter kann der Anteil der o-Form im thermodynamischen Gleichgewicht nicht gesteigert werden.
Im reinen Gas dauert bei tiefen Temperaturen die Einstellung des Gleichgewichts Monate, da die Wechselwirkungen zwischen den Kernen und der Hülle extrem schwach sind. Für diese Zeiten liegt damit praktisch eine Mischung von zwei unterschiedlichen Gasen vor. Trotz gleicher chemischer Zusammensetzung H2 unterscheiden sie sich sogar makroskopisch durch deutlich verschiedenen Temperaturverlauf der spezifischen Wärme. Abgesehen hiervon sind die physikalischen Eigenschaften von o- und p-Wasserstoff aber nur geringfügig verschieden. Beispielsweise liegen der Schmelz- und Siedepunkt der p-Form etwa 0,1 K unter denen der o-Form.
Bei der industriellen Herstellung von flüssigem Wasserstoff spielt der Übergang zwischen o- und p-Wasserstoff eine wichtige Rolle, weil bei der Temperatur der Verflüssigung das Gleichgewicht schon stark zur p-Form hin tendiert und sich spätestens im flüssigen Zustand dann schnell einstellt. Damit die dabei frei werdende Wärme nicht gleich einen Teil der gewonnenen Flüssigkeit wieder verdampfen lässt, beschleunigt man die Einstellung des neuen Gleichgewichts schon im gasförmigen Zustand durch den Einsatz von Katalysatoren.
Chemische Eigenschaften
Besonderheiten
Im Periodensystem steht Wasserstoff in der I. Hauptgruppe, weil er 1 Valenzelektron besitzt. Ähnlich wie die ebenfalls dort stehenden Alkalimetalle hat er in vielen Verbindungen die Oxidationszahl +1. Allerdings ist sein Valenzelektron auf der K-Schale, die nur maximal 2 Elektronen haben kann und somit die Edelgaskonfiguration bereits mit 2 Elektronen und nicht mit 8, wie bei den anderen Schalen, erreicht.
Durch Aufnahme eines Elektrons von sehr unedlen Metallen kann Wasserstoff die Edelgaskonfiguration des Heliums erreichen und hat dann die Oxidationszahl −1. Diese Verbindungen haben einen Halogenidcharakter und werden als Hydride bezeichnet.
Diese Stellung quasi „in der Mitte“ zwischen zwei Edelgaskonfigurationen, in der er die gleiche Anzahl Elektronen aufnehmen oder abgeben kann, ist eine Eigenschaft, die der IV. Hauptgruppe ähnelt, was seine Elektronegativität erklärt, die eher der des ebenfalls „in der Mitte“ stehenden Kohlenstoffs als der des Lithiums gleicht.
Aufgrund dieser „gemäßigten“ Elektronegativität sind die für die I. Hauptgruppe typischen Bindungen des Wasserstoffs in der Oxidationszahl +1 keine Ionenbindungen wie bei den Alkalimetallen, sondern kovalente Molekülbindungen.
Zusammenfassend sind die Eigenschaften des Wasserstoffs für die I. Hauptgruppe atypisch, da aufgrund der Tatsache, dass die K-Schale nur 2 Elektronen aufnehmen kann, Eigenschaften anderer Gruppen hinzukommen.
Molekularer Wasserstoff
Bei Zündung reagiert Wasserstoff mit Sauerstoff und Chlor heftig, ist sonst aber vergleichsweise beständig und wenig reaktiv. Bei hohen Temperaturen wird das Gas reaktionsfreudig und geht mit Metallen und Nichtmetallen gleichermaßen Verbindungen ein.
Mit Chlor reagiert Wasserstoff exotherm unter Bildung von gasförmigem Chlorwasserstoff, der in Wasser gelöst Salzsäure ergibt. Beide Gase reagieren dabei mit gleichen Stoffmengenanteilen:
- je ein Chlor- und Wasserstoffmolekül reagieren zu zwei Chlorwasserstoffmolekülen
Diese Reaktion ist unter dem Namen Chlorknallgasreaktion bekannt, die sich schon durch die Bestrahlung mit Licht zünden lässt. Für die Knallgasreaktion (Wasserstoff und Sauerstoff) bedarf es einer Zündung.
- je ein Sauerstoff- und zwei Wasserstoffmoleküle reagieren zu zwei Wassermolekülen
Die aggressivste Reaktion bei niedrigen Temperaturen geht jedoch Wasserstoff mit Fluor ein. Wird Wasserstoffgas bei −200 °C auf gefrorenes Fluor geleitet, reagieren die beiden Stoffe sofort explosiv miteinander.
- je ein Fluor- und Wasserstoffmolekül reagieren zu zwei Fluorwasserstoffmolekülen
Wird der molekulare Wasserstoff ionisiert, so spricht man vom Diwasserstoff-Kation. Dieses Teilchen tritt z. B. in Niedertemperatur-Plasmaentladungen in Wasserstoff als häufiges Ion auf.
- Ionisation durch ein schnelles Elektron im Plasma
Nascierender Wasserstoff
Wasserstoff in statu nascendi, d. h. im Zustand des Entstehens unmittelbar nach einer Wasserstoff erzeugenden Reaktion, existiert für Sekundenbruchteile in Form der einzelnen, sehr reaktiven H-Atome. Je zwei der Atome reagieren dann zum Molekül, das sich aber nach dem Zusammenschluss für kurze Zeit noch in einem angeregten Zustand befindet. Nascierender Wasserstoff kann – abweichend vom „normalen“ chemischen Verhalten – verschiedene Reaktionen bewirken, die mit molekularem Wasserstoff nicht möglich sind.
So gelingt es zum Beispiel nicht, mit Hilfe von im Kippschen Apparat erzeugtem Wasserstoffgas in einer angesäuerten, violetten Kaliumpermanganatlösung (KMnO4) oder gelben Kaliumdichromatlösung (K2Cr2O7) den die Reduktion anzeigenden Farbwechsel hervorzurufen. Mit direkt in diesen Lösungen durch Zugabe von Zinkpulver erzeugtem Wasserstoff in statu nascendi gelingt diese reduktive Farbänderung.
- Nascierender Wasserstoff vermag unter sauren Bedingungen violette Permanganatlösung zu entfärben.
- Unter sauren Bedingungen wird gelbe Dichromatlösung grün durch die reduzierende Wirkung des nascierenden Wasserstoffs.
Atomarer Wasserstoff
Um molekularen Wasserstoff in die Atome zu zerlegen, muss Energie von 436,22 kJ/mol (4,52 eV pro Molekül) aufgewendet werden (der Chemiker spricht von Enthalpie); beim Zusammenschluss zu Wasserstoffmolekülen wird diese Energie wieder freigesetzt:
Diese Energie ist unter Standardbedingungen weit höher als die thermische Energie , daher liegt das Gleichgewicht vollkommen auf der rechten Seite der dargestellten Gleichung.
Eine Anwendung findet diese Reaktion beim Arcatom-Schweißen.
Im Weltraum liegt bei niedrigen Temperaturen in der Regel molekularer Wasserstoff vor. In der Nähe heißer Sterne wird molekularer Wasserstoff jedoch von deren Strahlung aufgespalten, so dass dort die atomare Form überwiegt oder auch die Atome ionisiert werden (H-II-Gebiet).
Innerhalb von Sternen liegt Wasserstoff infolge der dort herrschenden hohen Temperaturen nicht atomar vor, sondern als Plasma. Die Oberfläche der Sonne hat jedoch „nur“ eine Temperatur von ca. 5500 °C, was einer thermischen Energie von 0,5 eV entspricht, weit unter der Energie von 4,5 eV, die zur Auflösung der molekularen Bindung erforderlich ist. Bei dieser Temperatur ist daher der größte Teil des Wasserstoffes nicht ionisiert und sogar molekular. Im Außenbereich der Sonne, der Korona, herrschen hingegen Temperaturen um eine Million Kelvin. Daher sind im Sonnenlicht die Übergänge der Elektronen im atomaren Wasserstoff erkennbar.
Wasserstoffbrückenbindung
Eine wichtige Eigenschaft des Wasserstoffs ist die so genannte Wasserstoffbrückenbindung, eine anziehende elektrostatische Kraft zwischen zwei Molekülen. Ist Wasserstoff an ein stark elektronegatives Atom, wie Fluor oder Sauerstoff, gebunden, so befindet sich sein Elektron eher in der Nähe des Bindungspartners. Es tritt also eine Ladungsverschiebung auf und das H-Atom wirkt nun positiv polarisiert. Der Bindungspartner wirkt entsprechend negativ. Kommen sich zwei solche Moleküle nahe genug, tritt eine anziehende elektrische Kraft zwischen dem positiven H-Atom des einen Moleküls und des negativen Teils des jeweiligen Partners auf. Das ist eine Wasserstoffbrückenbindung.
Da die Wasserstoffbrückenbindung mit nur 17 kJ/mol bis 167 kJ/mol[23] schwächer ist als die Bindungskraft innerhalb eines Moleküls, verbinden sich die Moleküle nicht dauerhaft. Vielmehr bleibt die Wasserstoffbrücke wegen ständiger Bewegung nur Bruchteile einer Sekunde bestehen. Dann lösen sich die Moleküle voneinander, um erneut eine Wasserstoffbrückenbindung mit einem anderen Molekül einzugehen. Dieser Vorgang wiederholt sich ständig.
Die Wasserstoffbrückenbindung ist für viele Eigenschaften verschiedener Verbindungen verantwortlich, wie DNA oder Wasser. Bei Letzterem führen diese Bindungen zu den Anomalien des Wassers, insbesondere der Dichteanomalie.
Verwendung
Jedes Jahr werden weltweit mehr als 600 Milliarden Kubikmeter Wasserstoff (rd. 30 Mio. t) für zahllose Anwendungen in Industrie und Technik gewonnen. Wichtige Einsatzgebiete sind:
- Energieträger: Beim Schweißen, als Raketentreibstoff. Von seiner Verwendung als Kraftstoff für Strahltriebwerke, in Wasserstoffverbrennungsmotoren oder über Brennstoffzellen verspricht man sich, in absehbarer Zeit die Nutzung von Erdölprodukten ablösen zu können (siehe Wasserstoffantrieb), weil bei der Verbrennung vor allem Wasser entsteht, doch kein Ruß und kein Kohlenstoffdioxid. Wasserstoff ist jedoch im Gegensatz zu Erdöl keine Primärenergie.
- Kohlehydrierung: Durch verschiedene chemische Reaktionen wird Kohle mit H2 in flüssige Kohlenwasserstoffe überführt. So lassen sich Benzin, Diesel und Heizöl künstlich herstellen.
- Reduktionsmittel: H2 kann mit Metalloxiden reagieren und ihnen dabei den Sauerstoff entziehen. Es entsteht Wasser und das reduzierte Metall. Dieses Verfahren der Verhüttung von Erzen und Zwischenprodukten wird genützt um Metalle möglichst rein zu gewinnen, etwa Wolfram. Denn Kohle und Koks bringen Begleitstoffe wie Phosphor und Schwefel ein.
- Ammoniakherstellung: Mit dem Haber-Bosch-Verfahren wird aus Stickstoff und Wasserstoff Ammoniak hergestellt und daraus wichtige Düngemittel und Sprengstoffe.
- Fetthärtung: Gehärtete Fette werden aus Pflanzenöl mittels Hydrierung gewonnen. Dabei werden die Doppelbindungen in ungesättigten Fettsäure-Resten der Glyceride mit Wasserstoff abgesättigt. Die entstehenden Fette haben einen höheren Schmelzpunkt, wodurch das Produkt fest wird. Auf diese Weise stellt man Margarine her. Dabei können als Nebenprodukt gesundheitlich bedenkliche trans-Fette entstehen.
- Lebensmittelzusatzstoff: Wasserstoff ist als E 949 zugelassen und wird (selten) als Treibgas, Packgas u. ä. verwendet.[24]
- Kühlmittel: Aufgrund seiner hohen Wärmekapazität benutzt man (gasförmigen) Wasserstoff in Kraftwerken und den dort eingesetzten Turbogeneratoren als Kühlmittel. Insbesondere setzt man H2 dort ein, wo eine Flüssigkeitskühlung problematisch werden kann. Die Wärmekapazität kommt dort zum Tragen, wo das Gas nicht oder nur langsam zirkulieren kann. Weil die Wärmeleitfähigkeit ebenfalls hoch ist, verwendet man strömendes H2 zum Abtransport von thermischer Energie in große Reservoire (z. B. Flüsse). In diesen Anwendungen schützt Wasserstoff die Anlagen vor Überhitzung und erhöht die Effizienz. Von Vorteil ist dabei, dass Wasserstoff durch seine geringe Dichte, die in die Reynoldszahl eingeht, bis zu höheren Geschwindigkeiten widerstandsarm laminar strömt als andere Gase.
- Kryogen: Wegen der hohen Wärmekapazität und des niedrigen Siedepunkts eignet sich flüssiger Wasserstoff als Kryogen, also als Kühlmittel für extrem tiefe Temperaturen. Auch größere Wärmemengen können von flüssigem Wasserstoff gut absorbiert werden, bevor eine merkliche Erhöhung in seiner Temperatur auftritt. So wird die tiefe Temperatur bei äußeren Schwankungen aufrechterhalten.
- Traggas: In Ballons und Luftschiffen fand Wasserstoff eine seiner ersten Verwendungen. Wegen der leichten Entzündlichkeit von H2-Luft-Gemischen führte dies jedoch wiederholt zu Unfällen. Die größte Katastrophe in diesem Zusammenhang ist wohl das Unglück der „Dixmude“ 1923, am bekanntesten wurde sicherlich die „Hindenburg-Katastrophe“ im Jahr 1937. In bemannten Zeppelinen wurde daraufhin der Wasserstoff durch Helium ersetzt. Spielt der Sicherheitsaspekt keine Rolle, beispielsweise bei Wetterballons, wird weiterhin der vielfach kostengünstigere und leichtere Wasserstoff bevorzugt.
- In der instrumentellen Analytik: so beim Betrieb des Flammenionisationsdetektors (FID) in Gaschromatographen.
Die beiden natürlichen Isotope haben spezielle Einsatzgebiete.
Deuterium (D = 2H)[21] findet (in Form von schwerem Wasser) in Schwerwasserreaktoren als Moderator Verwendung, d. h. zum Abbremsen der bei der Kernspaltung entstehenden schnellen Neutronen auf thermische Geschwindigkeit.
Deuterierte Lösungsmittel werden in der magnetischen Kernresonanzspektroskopie benutzt, da Deuterium einen Kernspin von Eins besitzt und im NMR-Spektrum des normalen Wasserstoff-Isotops nicht sichtbar ist.
In der Chemie und Biologie helfen Deuteriumverbindungen bei der Untersuchung von Reaktionsabläufen und Stoffwechselwegen (Isotopenmarkierung), da sich Verbindungen mit Deuterium chemisch und biochemisch meist nahezu identisch verhalten wie die entsprechenden Verbindungen mit Wasserstoff. Die Reaktionen werden von der Markierung nicht gestört, der Verbleib des Deuteriums ist in den Endprodukten dennoch feststellbar.
Ferner sorgt der erhebliche Massenunterschied zwischen Wasserstoff und Deuterium für einen deutlichen Isotopeneffekt bei den massenabhängigen Eigenschaften. So hat das schwere Wasser einen messbar höheren Siedepunkt als Wasser.
Das radioaktive Isotop Tritium (T = 3H) wird in Kernreaktoren in industriell verwertbaren Mengen hergestellt. Außerdem ist es neben Deuterium ein Ausgangsstoff bei der Kernfusion zu Helium. In der zivilen Nutzung dient es in Biologie und Medizin als radioaktiver Marker. So lassen sich beispielsweise Tumorzellen aufspüren. In der Physik ist es einerseits selbst Forschungsgegenstand, andererseits untersucht man mit hochbeschleunigten Tritiumkernen schwere Kerne oder stellt künstliche Isotope her.
Mit Hilfe der Tritiummethode lassen sich Wasserproben sehr genau datieren. Mit einer Halbwertszeit von etwa zwölf Jahren eignet es sich besonders für die Messung relativ kurzer Zeiträume (bis zu einigen hundert Jahren). Unter anderem lässt sich so das Alter eines Weines feststellen.
Es findet Verwendung als langlebige, zuverlässige Energiequelle für Leuchtfarben (im Gemisch mit einem Fluoreszenzfarbstoff), vor allem in militärischen Anwendungen, auch in Armbanduhren. Weitere militärische Verwendung findet das Isotop in der Wasserstoffbombe und gewissen Ausführungen von Kernwaffen, deren Wirkung auf Spaltung beruht.
Wasserstoff als Energiespeicher
Wasserstoff gilt als ein Energieträger der Zukunft.[25]
Herstellung von Wasserstoff
Als Energieträger ist Wasserstoff – wie elektrische Energie – keine Primärenergie, sondern muss wie Strom aus Primärenergie hergestellt werden.
Wasserstoff als Energieträger verursacht kein Kohlenstoffdioxid, wenn er mit erneuerbaren Energien wie Windenergie oder Sonnenenergie gewonnen wird (sogenannter grüner Wasserstoff). Biowasserstoff verursacht in der Nettobilanz kein Kohlendioxid, wenn Anbau und Verarbeitung der genutzten Biomasse CO2-neutral erfolgen. Derzeit (2019) erfolgt die Wasserstoff-Herstellung jedoch fast ausschließlich aus fossiler Primärenergie, überwiegend durch Erdgas-Reformierung.
Die unter dem Schlagwort „Power-to-Gas“ oft favorisierte Gewinnung durch Wasserelektrolyse mit überschüssigem erneuerbaren Strom gilt bei praktisch realisierten Wirkungsgraden von kaum über 60 %[26] als relativ ineffizient und wirtschaftlich nicht konkurrenzfähig gegenüber Reformierung von Erdgas, weil ausreichend billiger Strom-Überschuss tatsächlich nur für einige Stunden im Jahr genutzt werden kann und sich bei so meist geringer Auslastung die erforderliche Anlagen-Technik nur mit hohen Subventionen in Forschungs- und Pilot-Anlagen finanzieren lässt. Das kann sich erst ändern, falls eine künftig überwiegend regenerativ umgestellte Strom-Versorgung noch wesentlich mehr und nicht anderweitig verwertbare Überschüsse abwirft oder aber Erdgas als Rohstoff teurer als regenerative Stromerzeugung werden sollte bzw. mit einer entsprechend hohen CO2-Abgabe belegt wird.[27]
Speicherung von Wasserstoff
Energiedichten im Vergleich
| Brennstoff | Brennwert / Masse | Dichte | Brennwert / Vol | Heizwert / Vol |
|---|---|---|---|---|
| Wasserstoff[28] | 39,39 kWh/kg = 141,8 MJ/kg | 0,090 kg/m³ | 3,54 kWh/m³ = 12,7 MJ/m³ | 3,0 kWh/m³ = 10,8 MJ/m³ |
| Methan CH4[29] | 13,9 kWh/kg = 50 MJ/kg | 0,72 kg/m³ | 10 kWh/m³ = 36 MJ/m³ | 9,0 kWh/m³ = 32,4 MJ/m³ |
| Erdgas „H“[30] | 13,9 kWh/kg = 50 MJ/kg | 0,80 kg/m³ | 11,1 kWh/m³ = 40 MJ/m³ | 10 kWh/m³ = 36,0 MJ/m³ |
| Diesel[31] | 12,5 kWh/kg = 45 MJ/kg | 0,83 kg/L | 10,5 kWh/L = 37,8 MJ/L | 9,8 kWh/L = 35,3 MJ/L |
| Benzin[32] | 12,0 kWh/kg = 43 MJ/kg | 0,75 kg/L | 9,0 kWh/L = 32,4 MJ/L | 8,3 kWh/L = 30,0 MJ/L |
Auf das Volumen bezogen:[33]
- Wasserstoff (flüssig, also tiefkalt): 2360 kWh/m³
- Benzin: 8760 kWh/m³
- Erdgas (20 MPa = 200 bar): 2580 kWh/m³
- Wasserstoffgas (20 MPa): 530 kWh/m³
- Wasserstoffgas (Normaldruck): 3 kWh/m³
Kernfusion
Kernfusion in der Sonne und in Sternen
Mit Wasserstoffbrennen wird die Kernfusion von Wasserstoff zu Helium im Inneren von Sternen bezeichnet. Diese Reaktion stellt in normalen Sternen während des Großteils ihres Lebenszyklus die wesentliche Energiequelle dar. Sie hat trotz ihres historisch bedingten Namens nichts mit einer chemischen Verbrennung zu tun.
Der Prozess der Kernfusion kann beim Wasserstoffbrennen auf zwei Arten ablaufen, bei denen auf verschiedenen Wegen jeweils vier Protonen, die Atomkerne des Wasserstoffs, in einen Heliumkern 4He umgewandelt werden:
- die relativ direkte Proton-Proton-Reaktion
- der schwere Elemente (Kohlenstoff, Stickstoff, Sauerstoff) nutzende Bethe-Weizsäcker-Zyklus (CNO-Zyklus)
Insgesamt wird beim Wasserstoffbrennen etwa 0,73 % der Masse in Energie umgewandelt, was man als Massendefekt bezeichnet. Die aus der Massendifferenz erzeugte Energie ergibt sich aus der einsteinschen Beziehung E = mc². Sie resultiert aus der Kernbindungsenergie der Nukleonen, der Kernbausteine.
Fusionswaffen
1952 testeten die Vereinigten Staaten die erste Wasserstoffbombe. Brennstoff war das Isotop Deuterium. In der Bombe liefen vor allem folgende Kernreaktionen ab:
Das entstandene Tritium und Helium-3 können noch weiter reagieren:
In Summe entstehen aus drei Deuteronen ein Heliumkern sowie ein Neutron und ein Proton.
Da Deuterium wie Wasserstoff schwer zu speichern ist, wird bei den meisten Fusionswaffen inzwischen auf Lithium-Deuterid (LiD) als Brennstoff zurückgegriffen. Durch die bei der Primärreaktion von Deuterium entstehenden Neutronen wird aus dem Lithium Tritium erbrütet:
Fusionsreaktoren
Physiker forschen an einer friedlichen Nutzung der Kernverschmelzung zur Energiegewinnung in Kernfusionsreaktoren. Am weitesten fortgeschritten sind Versuche, die Reaktion in einem Plasma kontrolliert ablaufen zu lassen. Die dazu nötigen sehr hohen Temperaturen sind schwierig zu realisieren. Anders als Wasserstoffbomben werden Reaktoren voraussichtlich nur die Deuterium-Tritium-Reaktion zur Energiegewinnung nutzen können.
Biologische Bedeutung
Wasserstoff ist in Form verschiedenster Verbindungen essentiell für alle bekannten Lebewesen. An vorderster Stelle zu nennen ist hier Wasser, welches als Medium für alle zellulären Prozesse und für alle Stofftransporte dient. Zusammen mit Kohlenstoff, Sauerstoff, Stickstoff (und seltener auch anderen Elementen) ist er Bestandteil derjenigen Moleküle aus der organischen Chemie, ohne die jegliche uns bekannte Form von Leben schlicht unmöglich ist.
Wasserstoff spielt im Organismus aktive Rollen, so bei einigen Koenzymen wie Nicotinamid-Adenin-Dinucleotid (NAD/NADH), die als Reduktionsäquivalente (oder „Protonentransporter“) im Körper dienen und bei Redoxreaktionen mitwirken. In den Mitochondrien, den Kraftwerken der Zelle, dient die Übertragung von Wasserstoffkationen (Protonen) zwischen verschiedenen Molekülen der so genannten Atmungskette dazu, einen Protonengradienten durch chemiosmotisches Membranpotenzial zur Generierung von energiereichen Verbindungen wie Adenosintriphosphat (ATP) bereitzustellen. Bei der Photosynthese in Pflanzen und Bakterien wird der Wasserstoff aus dem Wasser dazu benötigt, das fixierte Kohlendioxid in Kohlenhydrate umzuwandeln.
Bezogen auf die Masse ist Wasserstoff im menschlichen Körper das drittwichtigste Element: Bei einer Person mit einem Körpergewicht von 70 kg, sind rund 7 kg (= 10 Gew.-%) auf den enthaltenen Wasserstoff zurückzuführen. Nur Kohlenstoff (ca. 20 Gew.-%) und Sauerstoff (ca. 63 Gew.-%) machen einen noch größeren Gewichtsanteil aus. Bezogen auf die Anzahl der Atome ist der sehr leichte Wasserstoff sogar das mit Abstand häufigste Atom im Körper eines jeden Lebewesens (die 7 kg beim Menschen entsprechen 3,5·103 Mol Wasserstoff mit je 2·6·1023 Atomen, das sind rund 4,2·1027 Wasserstoffatome).
Medizinische Bedeutung
In biologischen Systemen reagiert molekularer Wasserstoff mit reaktiven Sauerstoffspezies und wirkt so als Antioxidans. Im Tierversuch führt die Anreicherung von Trinkwasser mit molekularem Wasserstoff nach Nierentransplantation zu einem besseren Überleben des Transplantates, zu einem verminderten Auftreten einer chronischen Schädigung des Transplantates, zu einer Verminderung der Konzentration an reaktiven Sauerstoffspezies und zu einer Hemmung von Signalwegen, welche die entzündliche Aktivität verstärken (proinflammatorische Signalwege).[34]
Ökologische Bedeutung
Das Treibhauspotential von Wasserstoff ist bisher nur wenig untersucht. Die Schätzungen reichen vom 1,9 bis zum 16fachen der Wirkung von Kohlenstoffdioxid, bei einem Zeithorizont von 100 Jahren.[35] Eine 2023 publizierte Studie ermittelte über den Zeithorizont von 100 Jahren ein Treibhauspotential von 11,6 ±2,8, womit es 11,6 mal stärker wirkt als Kohlenstoffdioxid.[36]
Dabei ist Wasserstoff allerdings kein direktes Treibhausgas, denn es absorbiert keine Infrarotstrahlung. Stattdessen beeinflusst es das Vorkommen anderer Treibhausgase, sodass es indirekt Einfluss auf den Treibhauseffekt nimmt. Wenn H2 in die Atmosphäre gelangt, reagiert es mit dem dort vorkommenden Hydroxylradikal und bildet Wasser. Dadurch steht zum einen zunächst weniger Hydroxylradikal zur Verfügung, welches eine wichtige Reinigungsfunktion hat, um Methan und andere Treibhausgase mit noch höherer Klimawirkung als Wasserstoff abzubauen. Zum anderen entsteht dabei Wasserdampf, welcher in der Stratosphäre ebenfalls eine hohe Klimawirkung hat. Laut einer von der britischen Regierung in Auftrag gegebenen Studie aus dem Jahr 2022 soll eine Tonne Wasserstoff über einen Zeitraum von 100 Jahren die Atmosphäre der Erde etwa elf Mal so stark erwärmen wie eine Tonne CO2. Allerdings kommen die Autoren ebenfalls zu dem Schluss, dass auch in den pessimistischsten Szenarien die schädlichen Effekte weit weniger gravierend sind als diejenigen, die das durch die Nutzung von klimaneutral hergestelltem Wasserstoff eingesparte CO2 haben würde.[37] Trotz der klimaschädlichen Wirkung wird H2 nicht in der Liste der Treibhausgase des Pariser Klimaschutzabkommens und den Inventaren der Klimarahmenkonventionen §12 aufgeführt. Es kann deshalb nicht in nationalen Klimabilanzen verrechnet werden.[35]
Bedeutung im Leistungssport
Aufgrund der Wirkung als Antioxidans hat Wasserstoff eine leistungssteigernde Wirkung bei anaeroben Belastungen. Er kann sowohl niedrig dosiert im Training über einen längeren Zeitraum verwendet werden als auch hochdosiert unmittelbar vor bzw. während des Wettkampfes, z. B. in Halbzeitpausen.[38] Er kann sowohl zum unmittelbaren Gebrauch Getränken beigefügt werden als auch in Gasform ähnlich wie bei Sauerstoff z. B. über eine Maske eingeatmet werden.[39] Nur die intravenöse Verabreichung ist durch die Anti-Doping-Bestimmungen verboten.[40]
Sicherheitshinweise
Wasserstoff ist extrem entzündbar (alte Bezeichnung: hochentzündlich). Er brennt mit reinem Sauerstoff oder Luft sowie mit anderen gasförmigen Oxidationsmitteln wie Chlor oder Fluor mit heißer Flamme. Da die Flamme kaum sichtbar ist, kann man unabsichtlich hinein geraten.[41] Gemische mit Chlor oder Fluor sind schon durch Ultraviolettstrahlung entzündbar (siehe Chlorknallgas). Außer der nach GHS vorgeschriebenen Kennzeichnung (siehe Info-Box) müssen H2-Druckgasflaschen nach DIN EN 1089-3 mit roter Flaschenschulter und rotem Flaschenkörper versehen sein.
Wasserstoff ist nicht als gesundheitsschädlich oder umweltgefährdend eingestuft. Daher ist kein AGW-Wert festgelegt. Atem- oder Hautschutz sind nicht erforderlich. Erst wenn hohe Konzentrationen eingeatmet werden, können durch den Mangel an Sauerstoff ab etwa 30 Vol.-% Bewegungsstörungen, Bewusstlosigkeit und Ersticken auftreten.[42] Durch rasch austretendes Gas können bei Kontakt mit der Haut Kälteverbrennungen auftreten.
Gemische aus Luft mit einem Volumenanteil von 4 % bis 76 % Wasserstoff sind entzündbar. Ab einem Volumenanteil von 18 % in Luft ist das Gemisch explosiv (Knallgas). Aufgrund der hohen Diffusionsneigung und der geringen Dichte verflüchtigt sich Wasserstoff in offener Umgebung häufig, bevor es zur Bildung eines explosiven Gemischs kommt, oder brennt in heißen Umgebungen beim Erreichen der Konzentrationsgrenze von 4 % ab. Die Zündtemperatur in Luft beträgt 560 °C. Bei der Handhabung ist der Wasserstoff von Zündquellen, dazu gehören elektrostatische Entladungen, fernzuhalten. Die Lagerung der Behälter sollte fern von oxidierenden Gasen (Sauerstoff, Chlor) und anderen oxidierenden (brandfördernden) Stoffen erfolgen.
Wasserstoff kann wegen seiner geringen Größe durch viele Feststoffe hindurchdiffundieren, das heißt, Gas kann langsam durch ungeeignete Materialien austreten. Die für Gastanks und Leitungen verwendeten Materialien und ‑stärken berücksichtigen dies, sodass keine größeren Risiken bestehen als z. B. bei der Verwendung von Benzin.[43][44][45] Wasserstofffahrzeuge mit Drucktanks können problemlos in Parkhäusern und Tiefgaragen geparkt werden. Es existiert keine gesetzliche Bestimmung, die das einschränkt (siehe dazu: Wasserstoffspeicherung).
Nachweis
Molekularen Wasserstoff kann man durch die Knallgasprobe nachweisen. Bei dieser Nachweisreaktion wird eine kleine, beispielsweise während einer Reaktion aufgefangene Menge eines Gases in einem Reagenzglas entzündet. Wenn danach ein dumpfer Knall, ein Pfeifen oder ein Bellen zu hören ist, so ist der Nachweis positiv (das heißt, es war Wasserstoff in dem Reagenzglas). Der Knall kommt durch die Reaktion von Wasserstoffgas mit dem Luftsauerstoff zustande:
- (exotherme Reaktion)
- Wasserstoff reagiert mit Sauerstoff zu Wasser
Mit der gleichen Reaktion verbrennt Wasserstoff mit einer schwach bläulichen Flamme, wenn man ihn gleich an der Austrittsstelle entzündet (Pfeifgas).
Die Knallgasprobe ist die „klassische“ Methode zum Nachweis und ist besonders in Schulversuchen beliebt.
Verbindungen
Wasserstoff geht mit den meisten chemischen Elementen Verbindungen mit der allgemeinen Summenformel EHn (n = 1, 2, 3, 4) ein. Einige wenige dieser Elementwasserstoffe sind nur in Form so genannter Addukte bekannt, wie Lm · EHn (L steht für einen Liganden). Die Folgende Abbildung bietet eine Übersicht über wichtige Grundreaktionen des Wasserstoffs. Auf genaue Reaktionsbedingungen und Stöchiometrie ist hier nicht geachtet.
Wasserstoff kann in Verbindungen sowohl positive als auch negative Ladungsanteile tragen. Das ist abhängig davon, ob der Bindungspartner eine höhere oder eine niedrigere Elektronegativität als Wasserstoff (2,2) besitzt. Zwischen den beiden Verbindungstypen lässt sich im Periodensystem keine scharfe Grenze ziehen, da zum Beispiel das Säure-Base-Verhalten mit berücksichtigt werden muss. Eine mehr oder weniger willkürliche Betrachtung besagt, dass in den Wasserstoffverbindungen der Elemente Bor, Silicium, Germanium, Zinn und Blei sowie allen links davon der Wasserstoff negativ polarisiert ist, in Verbindungen mit Kohlenstoff, Phosphor, Arsen, Antimon, Bismut und allen Elementen rechts davon positiv. Entsprechend lässt sich bei Monosilan (SiH4) die Oxidationszahl für Silicium auf +4 (Wasserstoff dementsprechend −1), in Methan (CH4) für Kohlenstoff auf −4 (Wasserstoff +1) festlegen.
Zur Darstellung von Wasserstoffverbindungen EHn werden hauptsächlich drei verschiedene Verfahren genutzt:
- Die Umsetzung des entsprechenden Elements E mit Wasserstoff (H2; Hydrogenolyse)
- Ein Element reagiert mit Wasserstoff bei Energiezufuhr zum entsprechenden Elementwasserstoff.
- Die Reaktion von Metallverbindungen des Typs MnE mit Wasserstoffsäuren (H+; Protolyse)
- Eine Metallverbindung des Elements E reagiert mit einer Säure HA zum Elementwasserstoff und einem Metallsalz.
- Die Umsetzung von Halogenverbindungen (EHaln) mit Hydriden (H−; Hydridolyse)
- Hydridionen setzen aus einer Halogenverbindung des Elements E den entsprechenden Elementwasserstoff frei.
Salzartige Verbindungen
In Verbindung mit Metallen kann Wasserstoff jeweils ein Elektron aufnehmen, so dass negativ geladene Wasserstoffionen (Hydridionen, H−) entstehen, die mit Metallkationen Salze bilden. Diese Verbindungen werden Hydride genannt. Salzartige Elementwasserstoffe sind von den Alkali- und, mit Ausnahme von Beryllium, den Erdalkalimetallen bekannt. Außerdem zählt man die Dihydride des Europiums und Ytterbiums (EuH2 und YbH2) dazu.
Metallhydride reagieren sehr heftig mit Wasser unter Freisetzung von molekularem Wasserstoff (H2) und können sich an der Luft selbst entzünden, wobei sich Wasser und das Metalloxid bilden. In der Mehrzahl sind sie aber nicht explosiv. Minerale, die (an Sauerstoff gebundenen) Wasserstoff enthalten, sind Hydrate oder Hydroxide.
Metallartige Verbindungen
In metallartigen Wasserstoffverbindungen – mit wenigen Ausnahmen sind das die Übergangsmetallhydride – ist atomarer Wasserstoff in der entsprechenden Metallstruktur eingelagert. Man spricht in diesem Fall auch von Wasserstoff-Einlagerungsverbindungen, obwohl sich bei der Aufnahme des Wasserstoffs die Struktur des Metalls ändert (was eigentlich nicht der Definition für Einlagerungsverbindungen entspricht). Das Element besetzt die oktaedrischen und tetraedrischen Lücken in den kubisch- bzw. hexagonal-dichtesten Metallatompackungen.
Die Löslichkeit von Wasserstoff steigt mit zunehmender Temperatur. Man findet jedoch selbst bei Temperaturen über 500 °C selten mehr als einen Stoffmengenanteil von 10 % Wasserstoff im betreffenden Metall. Am meisten Wasserstoff können die Elemente Vanadium, Niob und Tantal aufnehmen. Bei Raumtemperatur sind folgende Stöchiometrien zu beobachten: VH0,05, NbH0,11 und TaH0,22. Ab 200 °C findet man bei diesen Metallen eine 1:1-Stöchiometrie (MH) vor. Das kubisch-raumzentrierte Kristallgitter bleibt dabei unangetastet.
Kovalente Verbindungen
Verbindungen, bei denen Wasserstoff der elektropositivere Partner ist, haben einen hohen kovalenten Anteil. Als Beispiele seien Fluorwasserstoff (HF) oder Chlorwasserstoff (HCl) genannt. In Wasser reagieren diese Stoffe als Säuren, da der Wasserstoff sofort als Proton (H+-Ion) von umgebenden Wassermolekülen abgespalten werden kann. Isolierte H+-Ionen verbinden sich in wässriger Lösung sofort mit Wassermolekülen zu H3O+-Ionen; dieses Ion ist verantwortlich für die saure Eigenschaft von wässrigen Chlorwasserstofflösungen.
Säure-Base-Verhalten
Die kovalenten Wasserstoffverbindungen der Elemente der IV. bis VII. Hauptgruppe des Periodensystems sowie Borwasserstoffe sind Säuren nach der Definition von Johannes Nicolaus Brønsted, geben also Protonen an andere Verbindungen ab.
Die Säurestärke der Verbindungen nimmt dabei in den Hauptgruppen von oben nach unten und in den Perioden von links nach rechts zu. Ebenso steigt sie mit der Zahl der Element-Element-Bindungen bei Wasserstoffverbindungen eines bestimmten Elements. So ist zum Beispiel Wasser (H2O) eine schwächere Säure als Wasserstoffperoxid (H2O2), Ethan (C2H6) in der Säurestärke schwächer als Ethen (C2H4) und Ethin (C2H2).
Umgekehrt können kovalente Elementwasserstoffe als Basen fungieren. Wasserstoffverbindungen der Elemente aus Hauptgruppe V bis VII können Protonen aufnehmen, da sie über freie Elektronenpaare verfügen.
Ursache für die Acidität oder Basizität einer wässrigen Lösung ist die Stoffmengenkonzentration an Protonen (H+-Ionen). Den negativen dekadischen Logarithmus dieser Konzentration nennt man pH-Wert. Zum Beispiel bedeutet eine Konzentration von 0,001 mol H+-Ionen pro Liter Wasser „pH 3,0“. Dieses Beispiel trifft auf eine Säure zu. Wasser ohne jeden Zusatz hat bei Normalbedingungen den pH 7, Basen haben pH-Werte bis 14.
Oxide
Wasserstoffoxide (auch Hydrogeniumoxide) sind Verbindungen, die nur aus Wasserstoff und Sauerstoff bestehen. Von größter Wichtigkeit ist das Wasser (Wasserstoffoxid); von technischer Bedeutung ist daneben Wasserstoffperoxid, früher Wasserstoffsuperoxid genannt. Ein weiteres, aber selteneres Oxid ist das Dihydrogentrioxid.
Von außerordentlicher Bedeutung für alles Leben auf der Erde sind auch Alkohole und Saccharide sowie Carbonsäuren, die (nur) Wasserstoff, Sauerstoff und Kohlenstoff enthalten.
Kohlenwasserstoffe
Wasserstoff bildet mit Kohlenstoff die kovalenten Kohlenwasserstoffe, deren Studium sich die Kohlenwasserstoffchemie verschrieben hat.
Siehe auch
Literatur
Chemie
- Erwin Riedel: Anorganische Chemie. de Gruyter, Berlin 2002, ISBN 3-11-017439-1.
- A. F. Holleman, E. Wiberg, N. Wiberg: Lehrbuch der Anorganischen Chemie. 102. Auflage. Walter de Gruyter, Berlin 2007, ISBN 978-3-11-017770-1, S. 259–296.
- Harry H. Binder: Lexikon der chemischen Elemente – das Periodensystem in Fakten, Zahlen und Daten. S. Hirzel Verlag, Stuttgart 1999, ISBN 3-7776-0736-3.
Technik
- Peter Kurzweil: Brennstoffzellentechnik. 1. Auflage. Vieweg Verlag, Wiesbaden 2003, ISBN 3-528-03965-5.
- Udo Schelling: Brennstoffzellen. In: Richard Zahoransky (Hrsg.): Energietechnik. 5., überarb. u. erw. Auflage. Vieweg+Teubner Verlag, Wiesbaden 2010, ISBN 978-3-8348-1207-0, S. 203ff.
- Helmut Eichlseder, Manfred Klell: Wasserstoff in der Fahrzeugtechnik. 1. Auflage. Vieweg+Teubner Verlag, Wiesbaden 2008, ISBN 978-3-8348-0478-5.
- Rex A. Ewing: Hydrogen – A Journey Into a World of Hydrogen Energy and Fuel Cells. Pixyjack Press, Masonville CO 2004, ISBN 0-9658098-6-2.
Bedeutung
- Hoimar von Ditfurth: Im Anfang war der Wasserstoff. dtv, München 2002, ISBN 3-423-33015-5.
Weblinks
- Literatur von und über Wasserstoff im Katalog der Deutschen Nationalbibliothek
- Linkkatalog zum Thema Wasserstoff bei curlie.org (ehemals DMOZ)
- Eine Wasserstoff- und Deuterium-Spektralröhre Betrieb mit 1,8 kV, 18 mA und einer Frequenz von 35 kHz.
Einzelnachweise
- ↑ Harry H. Binder: Lexikon der chemischen Elemente – das Periodensystem in Fakten, Zahlen und Daten. S. Hirzel Verlag, Stuttgart 1999, ISBN 3-7776-0736-3.
- ↑ Die Werte für die Eigenschaften (Infobox) sind, wenn nicht anders angegeben, aus www.webelements.com (Wasserstoff) entnommen.
- ↑ Angegeben ist der von der IUPAC empfohlene Standardwert, da die Isotopenzusammensetzung dieses Elements örtlich schwanken kann, ergibt sich für das mittlere Atomgewicht der in Klammern angegebene Massenbereich. Siehe: Michael E. Wieser, Tyler B. Coplen: Atomic weights of the elements 2009 (IUPAC Technical Report). In: Pure and Applied Chemistry. 2010, S. 1, doi:10.1351/PAC-REP-10-09-14.
- ↑ IUPAC, Standard Atomic Weights Revised 2013.
- ↑ Eintrag zu hydrogen in Kramida, A., Ralchenko, Yu., Reader, J. und NIST ASD Team (2019): NIST Atomic Spectra Database (ver. 5.7.1). Hrsg.: NIST, Gaithersburg, MD. doi:10.18434/T4W30F (physics.nist.gov/asd). Abgerufen am 11. Juni 2020.
- ↑ a b Eintrag zu hydrogen bei WebElements, www.webelements.com, abgerufen am 11. Juni 2020.
- ↑ a b c d Eintrag zu Wasserstoff in der GESTIS-Stoffdatenbank des IFA, abgerufen am 23. Oktober 2021. (JavaScript erforderlich)
- ↑ Robert C. Weast (Hrsg.): CRC Handbook of Chemistry and Physics. CRC (Chemical Rubber Publishing Company), Boca Raton 1990, ISBN 0-8493-0470-9, S. E-129 bis E-145. Die Werte dort sind auf g/mol bezogen und in cgs-Einheiten angegeben. Der hier angegebene Wert ist der daraus berechnete maßeinheitslose SI-Wert.
- ↑ a b Yiming Zhang, Julian R. G. Evans, Shoufeng Yang: Corrected Values for Boiling Points and Enthalpies of Vaporization of Elements in Handbooks. In: Journal of Chemical & Engineering Data. 56, 2011, S. 328–337, doi:10.1021/je1011086.
- ↑ Eintrag zu Hydrogen im Classification and Labelling Inventory der Europäischen Chemikalienagentur (ECHA), abgerufen am 1. August 2016. Hersteller bzw. Inverkehrbringer können die harmonisierte Einstufung und Kennzeichnung erweitern.
- ↑ a b c d Theodore L. Brown, H. Eugene LeMay, Bruce E. Bursten: Chemie. Die zentrale Wissenschaft. Pearson Studium, 2007, ISBN 978-3-8273-7191-1, S. 1087–1090.
- ↑ Jürgen Sültenfuß: Das Radionuklid Tritium im Ozean: Messverfahren und Verteilung von Tritium im Südatlantik und im Weddellmeer. Dissertation. In: Berichte zur Polarforschung. Nr. 256, 1998, 1.1 Das Isotop Tritium, S. 2–4, doi:10.2312/BzP_0256_1998 (awi.de [PDF]).
- ↑ Ernst F. Schwenk: Sternstunden der frühen Chemie. Verlag C. H. Beck, 1998, ISBN 3-406-45601-4.
- ↑ Martin Carrier, Cavendishs Version der Phlogistonchemie oder: Über den empirischen Erfolg unzutreffender theoretischer Ansätze, in: J. Mittelstraß, Chemie und Geisteswissenschaften, Akademie Verlag, Berlin 1992, S. 35–52, (online)
- ↑ The composition of the Earth. (PDF) Archiviert vom am 28. September 2011; abgerufen am 16. Dezember 2019.
- ↑ H (Hydrogen). Webmineral – Mineral Species sorted by the element (englisch).
- ↑ a b Eintrag zu Wasserstoff. In: Römpp Online. Georg Thieme Verlag, abgerufen am 2. Januar 2015.
- ↑ Nist Datenbank: Saturation Properties for Hydrogen — Temperature Increments. National Institute of Standards and Technology, abgerufen am 6. Juli 2020.
- ↑ GIT Labor-Fachzeitschrift. Heft 9/2013, S. 596, nach Jürgen Quadbeck-Seeger (Hrsg.): Chemie Rekorde. Wiley-VCH.
- ↑ a b c d Eintrag zu Wasserstoff. In: P. J. Linstrom, W. G. Mallard (Hrsg.): NIST Chemistry WebBook, NIST Standard Reference Database Number 69. National Institute of Standards and Technology, Gaithersburg MD.
- ↑ a b Anm. Nur für die 2 schwereren Isotope des Wasserstoffs werden eigene chemische Zeichen benutzt.
- ↑ D. Lal, B. Peters: Cosmic ray produced radioactivity on the earth. In: Handbuch der Physik. Band 46/2, Springer, Berlin 1967, S. 551–612.
- ↑ George A. Jeffrey: An Introduction to Hydrogen Bonding. Oxford University Press, 1997, ISBN 0-19-509549-9.
- ↑ Verordnung (EG) Nr. 1333/2008 in der konsolidierten Fassung vom 31. Oktober 2022
- ↑ Wasserstoff als Energieträger der Zukunft ( vom 26. Oktober 2012 im Internet Archive) VDE; abgerufen am 11. April 2012.
- ↑ energieagentur.nrw Information der Energieagentur Nordrhein-Westfalen zu Brennstoffzelle und Wasserstoff: alkalische Elektrolyse/Lurgi-Verfahren, abgerufen am 11. August 2020
- ↑ [Rüdiger Paschotta]: Power to Gas – ein Hype? In: energie-lexikon.info. Abgerufen am 19. Dezember 2022.
- ↑ Rüdiger Paschotta: Wasserstoff. In: energie-lexikon.info. Abgerufen am 19. Dezember 2022.
- ↑ Rüdiger Paschotta: Methan. In: energie-lexikon.info. Abgerufen am 19. Dezember 2022.
- ↑ Rüdiger Paschotta: Erdgas. In: energie-lexikon.info. Abgerufen am 19. Dezember 2022.
- ↑ Rüdiger Paschotta: Dieselkraftstoff. In: energie-lexikon.info. Abgerufen am 19. Dezember 2022.
- ↑ Rüdiger Paschotta: Benzin. In: energie-lexikon.info. Abgerufen am 19. Dezember 2022.
- ↑ Stephan Glante: Untersuchungen zur Synthese von ZIF-8 und Wasserstoffspeicherung in ausgewählten metall-organischen Gerüstverbindungen opus4.kobv.de, 6. Juni 2019, abgerufen am 5. November 2022.
- ↑ Jon S Cardinal, Jianghua Zhan, Yinna Wang, Ryujiro Sugimoto, Allan Tsung, Kenneth R McCurry, Timothy R Billiar, Atsunori Nakao: Oral hydrogen water prevents chronic allograft nephropathy in rats. In: Kidney International. Band 77, Nr. 2, Januar 2010, S. 101–109, doi:10.1038/ki.2009.421, PMID 19907413.
- ↑ a b Umweltbundesamt; Ist Wasserstoff treibhausgasneutral? Tabelle 1: Treibhauspotentialwerte von Wasserstoff
- ↑ Maria Sand et al.: A multi-model assessment of the Global Warming Potential of hydrogen. In: communications earth & environment. Band 4, 2023, doi:10.1038/s43247-023-00857-8.
- ↑ Atmospheric implications of increased Hydrogen use
- ↑ Botek, M., Krejčí, J., McKune, A.J. et al. (2019), Hydrogen Rich Water Improved Ventilatory, Perceptual and Lactate Responses to Exercise. Int J Sports Med 40(14), 879-885.
- ↑ Aoki, K., Nakao, A., Adachi, Tusdm et al. (2012): Pilot study: Effects of drinking hydrogen-rich water on muscle fatigue caused by acute exercise in elite athletes. In: Med Gas Res. 2 (12). doi:10.1186/2045-9912-2-12
- ↑ Arnd Krüger: Wasserstoff. Leistungssport. 50, (2020), 2, S. 29–32.
- ↑ Axel Stepken: Wasserstoff – So sicher wie Benzin ( vom 22. Dezember 2015 im Internet Archive), Medienforum Deutscher Wasserstofftag, 2003. (PDF; 704 kB).
- ↑ Helmut Eichlseder, Manfred Klell: Wasserstoff in der Fahrzeugtechnik. 2010, ISBN 978-3-8348-0478-5.
- ↑ Spektakulärer Test zeigt: Wasserstoff im Auto muss nicht gefährlicher sein als Benzin. In: wissenschaft.de. 3. Februar 2003, abgerufen am 8. September 2019.
- ↑ Sicherheitsaspekte bei der Verwendung von Wasserstoff ( vom 6. März 2012 im Internet Archive) Quelle: Hycar.
- ↑ Crashversuch der University of Miami auf YouTube

