Iodphenole
| Iodphenole | |||||||
| Name | 2-Iodphenol | 3-Iodphenol | 4-Iodphenol | ||||
| Andere Namen | o-Iodphenol | m-Iodphenol | p-Iodphenol | ||||
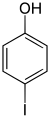
| Strukturformel | 
|

|
| ||||
| CAS-Nummer | 533-58-4 | 626-02-8 | 540-38-5 | ||||
| PubChem | 10784 | 12272 | 10894 | ||||
| Summenformel | C6H5IO | ||||||
| Molare Masse | 220,01 g·mol−1 | ||||||
| Aggregatzustand | fest | ||||||
| Schmelzpunkt | 43 °C[1] | 40 °C[1] | 92–94 °C[1] | ||||
| Siedepunkt | 186–187 °C (160 Torr)[1] |
||||||
| pKs-Wert[1] | 8,46 | 9,17 | 9,20 | ||||
| GHS- Kennzeichnung |
|
|
| ||||
| H- und P-Sätze | 302‐312‐315‐319‐332‐335 | 315‐319‐335 | 302‐312‐314 | ||||
| keine EUH-Sätze | keine EUH-Sätze | keine EUH-Sätze | |||||
| 261‐280‐305+351+338 | 261‐305+351+338 | 280‐305+351+338‐310 | |||||
Die Iodphenole bilden in der Chemie eine Stoffgruppe, die sich sowohl vom Phenol als auch vom Iodbenzol ableitet. Die Struktur besteht aus einem Benzolring mit angefügter Hydroxygruppe (–OH) und Iod (–I) als Substituenten. Durch deren unterschiedliche Anordnung ergeben sich drei Konstitutionsisomere mit der Summenformel C6H5IO.
Eigenschaften
BearbeitenDas 4-Iodphenol, das die höchste Symmetrie aufweist, besitzt den höchsten Schmelzpunkt. Die Iodphenole weisen aufgrund des −I-Effekts des Iodsubstituenten eine höhere Acidität im Vergleich zum Phenol auf. Die pKs-Werte sind daher entsprechend niedriger (Phenol: 9,99[1]).
Darstellung
BearbeitenDie Iodphenole sind aus den Iodanilinen durch Verkochen ihrer Diazoniumsalze darstellbar.
Einzelnachweise
Bearbeiten- ↑ a b c d e f CRC Handbook of Tables for Organic Compound Identification, Third Edition, 1984, ISBN 0-8493-0303-6.
- ↑ Datenblatt 2-Iodophenol bei Sigma-Aldrich, abgerufen am 3. Mai 2011 (PDF).
- ↑ Datenblatt 3-Iodophenol bei Sigma-Aldrich, abgerufen am 3. Mai 2011 (PDF).
- ↑ Datenblatt 4-Iodophenol bei Sigma-Aldrich, abgerufen am 3. Mai 2011 (PDF).

