Lupane (Stoffgruppe)
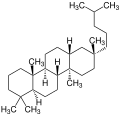
Die Lupane sind eine Stoffgruppe von Triterpenen mit einer pentacyclischen Struktur. Wie alle Triterpene sind die Lupane aus sechs Isopreneinheiten aufgebaut und haben daher in der Regel 30 Kohlenstoffatome. Lupane haben eine Struktur aus vier Sechsringen und einem Fünfring. Der Grundkörper Lupan C30H52 (CAS-Nummer 464-99-3) hat Methylgruppen in den Stellungen 4, 4, 8, 10, 14 und 17 sowie einen Isopropylrest in Stellung 19.
Strukturformeln wichtiger Lupane
-
Betulin C30H50O2
-
Betulinsäure C30H48O3
-
Lupeol C30H50O
Das Lupan-Grundgerüst basiert auf dem des Baccharans; Lupane gehören daher zur Triterpen-Untergruppe des Baccharantyps.
Strukturformeln von Lupan und Baccharan
-
Lupan C30H52
-
Baccharan
Historisches
BearbeitenJohann Tobias Lowitz isolierte Betulin aus Birkenrinde; er veröffentlichte seine Untersuchung 1788.[1] Die Entdeckung des Lupeols wurde 1891 durch Arthur Likiernik bekanntgegeben; er hatte es während seiner Doktorarbeit bei Ernst Schulze aus gelben Lupinen (Lupinus luteus) isoliert und nach diesem Ursprung benannt.[2][3] Später fand Schulze Lupeol auch in weißen Lupinen (Lupinus albus).[4]
1971 wurde eine Totalsynthese von Lupeol publiziert.[5]
Vorkommen und Isolierung
BearbeitenBetulin bildet bis zu 30 % der Trockensubstanz der Rinde der Hänge-Birke Betula verrucosa und kann daraus leicht durch Extraktion mit Chloroform gewonnen werden.[7] Lupeol kommt in Früchten, beispielsweise Mango oder Erdbeeren, und in Gemüse vor.[8]
Verwendung und mögliche Anwendungen
BearbeitenDas Betulin-haltige Medikament Episalvan hat eine europäische Zulassung für die Behandlung von dermalen Wunden bei Erwachsenen. Betulin wird in als emulgierender Zusatz von Haarwaschmitteln genutzt.[9]
Es gibt eine Reihe von Hinweisen, dass Lupane, insbesondere Betulin, Betulinsäure und Lupeol, vorbeugende und heilende Wirkungen gegen Krebserkrankungen haben können.[10]
Verwandte Stoffgruppen
BearbeitenDie Hopanoide haben bei den vier Sechsringen die gleiche Struktur wie die Lupane, unterscheiden sich aber beim Substitutionsmuster am Fünfring. Weitere Untergruppen der Triterpene sind die Oleanane und die Ursane.
Einzelnachweise
Bearbeiten- ↑ Johann Tobias Lowitz: Über eine neue, fast benzoeartige Substanz der Birken. In: Lorenz Crell (Hrsg.): Chemische Annalen. für die Freunde der Naturlehre, Arzneygelahrtheit, Haushaltungskunst und Manufakturen. Band 1788, Nr. 1. Fleckeisen/Müllersche Buchhandlung, Helmstädt und Leipzig 1788, OCLC 609930568, S. 312–316 (online bei der Bayerischen Staatsbibliothek digital): „mehrere Scheite von jungen Birken mit weißer Rinde, aufgerichtet, so nahe an ein sehr ruhiges Feuer“
- ↑ Arthur Likiernik: Ueber das Lupeol. In: Berichte der deutschen chemischen Gesellschaft. Band 24, Nr. 1. Berlin Januar 1891, S. 183–186, doi:10.1002/cber.18910240135 (online bei Gallica Bibliothèque nationale de France).
- ↑ Arthur Likiernik: Ueber das pflanzliche Lecithin und über einige Bestandtheile der Leguminosenschalen. Inaugural-Dissertation. Zürich 1891 (web.archive.org [PDF; 393 kB; abgerufen am 9. Oktober 2021] E. Roth im Botanischen Centralblatt 1892 online).
- ↑ https://archive.org/details/botanischeszentr2597bota/page/208
- ↑ Gilbert Stork, Shoichiro Uyeo, T. Wakamatsu, P. Grieco, J. Labovitz: Total synthesis of lupeol. In: Journal of the American Chemical Society. Band 93, Nr. 19, September 1971, S. 4945–4947, doi:10.1021/ja00748a068.
- ↑ Robert A. Hill, Joseph D. Connolly: Triterpenoids. In: Natural Product Reports. Band 35, Nr. 12, 2018, S. 1294–1329, doi:10.1039/C8NP00029H.
- ↑ Brian Green, Michael D. Bentley, Bong Y. Chung, Nicholas G. Lynch, Bruce L. Jensen: Isolation of Betulin and Rearrangement to Allobetulin. A Biomimetic Natural Product Synthesis. In: Journal of Chemical Education. Band 84, Nr. 12, Dezember 2007, S. 1985, doi:10.1021/ed084p1985.
- ↑ Niege J. C. Furtado, Laetitia Pirson, Hélène Edelberg, Lisa M. Miranda, Cristina Loira-Pastoriza: Pentacyclic Triterpene Bioavailability: An Overview of In Vitro and In Vivo Studies. In: Molecules. Band 22, Nr. 3, 4. März 2017, S. 400, doi:10.3390/molecules22030400, PMID 28273859, PMC 6155290 (freier Volltext).
- ↑ Charles Gauthier, Jean Legault, Marianne Piochon-Gauthier, André Pichette: Advances in the synthesis and pharmacological activity of lupane-type triterpenoid saponins. In: Phytochemistry Reviews. Band 10, Nr. 4, Dezember 2011, S. 521–544, doi:10.1007/s11101-010-9176-y.
- ↑ M. H. Cháirez-Ramírez, M. R. Moreno-Jiménez, R. F. González-Laredo, J. A. Gallegos-Infante, Nuria Elizabeth Rocha-Guzmán: Lupane-type triterpenes and their anti-cancer activities against most common malignant tumors: A review. In: EXCLI Journal 2. 30. November 2016, S. 758–771, doi:10.17179/excli2016-642, PMID 28337107, PMC 5318673 (freier Volltext) – (excli.de [PDF]).