Strontiumhydrogenphosphat
Strontiumhydrogenphosphat, Sr(HPO4), ist das Strontiumsalz der Phosphorsäure in Form eines Hydrogenphosphats.
| Kristallstruktur | ||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
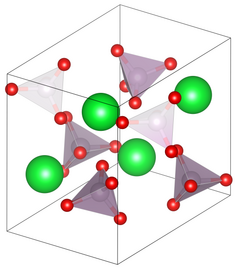
| ||||||||||||||||
| _ Sr2+ _ P5+ _ O2− | ||||||||||||||||
| Kristallsystem |
triklin | |||||||||||||||
| Raumgruppe |
P1 (Nr. 2) | |||||||||||||||
| Gitterparameter |
a =7,184 Å, b = 6,790 Å, c = 7,256 Å, α = 94,68°, β =104,97°, γ =88,77° | |||||||||||||||
| Allgemeines | ||||||||||||||||
| Name | Strontiumhydrogenphosphat | |||||||||||||||
| Verhältnisformel | Sr(HPO4) | |||||||||||||||
| Kurzbeschreibung |
weißes Pulver[1] | |||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||
| ||||||||||||||||
| Eigenschaften | ||||||||||||||||
| Molare Masse | 183,60 g·mol−1 | |||||||||||||||
| Dichte |
3,55 g·cm−3[1] | |||||||||||||||
| Schmelzpunkt |
Zersetzung bei >350 °C[1] | |||||||||||||||
| Löslichkeit |
praktisch unlöslich in Wasser (62,1 mg·l−1 bei 20 °C)[1] | |||||||||||||||
| Sicherheitshinweise | ||||||||||||||||
| ||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). | ||||||||||||||||
Darstellung
BearbeitenDie Darstellung von SrHPO4 kann durch Reaktion von Strontiumchlorid mit Diammoniumhydrogenphosphat erfolgen.
Eigenschaften
BearbeitenStrontiumhydrogenphosphat ist ein weißer, kristalliner Feststoff, welcher weder brennbar ist noch explosive Stäube bildet. Allerdings zersetzt sich der Stoff bei Erhitzen oberhalb von 350 °C.
Die Verbindung liegt in drei verschiedenen Modifikationen vor. Die α-Modifikation wird nach obiger Synthese bei unter 25 °C erhalten, die β-Modifikation bei über 40 °C, während dazwischen eine Mischung mit beiden Modifikationen entsteht. Weiterhin existiert noch eine γ-Modifikation.
α-SrHPO4 kristallisiert in der Raumgruppe P1 (Raumgruppen-Nr. 2) mit den Gitterkonstanten a =7,184 Å, b = 6,790 Å, c = 7,256 Å, α = 94,68°, β = 104,97° und γ = 88,77°[2] Die γ-Modifikation bildet dagegen orthorhombische Kristalle in der Raumgruppe Pbca (Raumgruppen-Nr. 61) aus. Die Gitterkonstanten für diese Modifikation lauten a = 8,313 Å, b = 9,259 Å, c = 18,085 Å.[3]
Verwendung
BearbeitenDie Verbindung dient meist als Ausgangsstoff zur Synthese von Leuchtstoffen wie zweiwertigem Zinn dotiertes Sr2P2O7.[4]
Die Nutzung von mit Seltenen Erden dotiertem SrHPO4 als Diode wird untersucht.[5]
Die Verbindung ist auch Gegenstand der medizinischen Forschung, insbesondere in der Therapie von Osteoporose. Dies ist auf die ähnliche Ionengröße und das ähnliche chemische Verhalten von Strontium verglichen mit Calcium zurückzuführen. Eine Studie kam zu dem Ergebnis, dass Cluster von β-SrHPO4 ein geeigneter Carrier für Calciumphosphat in der Osteoporose-Therapie sind.[6] Auch wird die Nutzung von Strontiumhydrogenphosphat zum Binden von Pb2+-Ionen untersucht.[7]
Einzelnachweise
Bearbeiten- ↑ a b c d e Eintrag zu Strontiumhydrogenphosphat in der GESTIS-Stoffdatenbank des IFA, abgerufen am 4. November 2018. (JavaScript erforderlich)
- ↑ A. Boudjada, R. Masse, J. C. Guitel: Structure cristalline de l’orthophosphate monoacide de strontium:SrHPO4α: forme triclinique. In: Acta Crystallographica Section B. Band 34, 1978, S. 2692–2695, doi:10.1107/S0567740878009036 (französisch).
- ↑ Lotfi Ben Taher et al.: Investigation of the Alkaline Earth Phosphates. Synthesis and Crystal Structure of a New Strontium Hydrogen Phosphate Form. In: Journal of Solid State Chemistry. Band 52, 2000, S. 428–434, doi:10.1006/jssc.2000.870.
- ↑ Richard C. Ropp: Encyclopedia of the Alkaline Earth Compounds. Newnes, 2012, ISBN 978-0-444-59553-9, 4.2, S. 255–266 (eingeschränkte Vorschau in der Google-Buchsuche [abgerufen am 4. November 2018]).}
- ↑ Mengan Wang et al.: Crystal structure, morphology and luminescent properties of rare earthion-doped SrHPO4 nanomaterials. In: Journal of Rare Earths. Band 33, Nr. 4, April 2015, S. 355–360, doi:10.1016/S1002-0721(14)60426-9.
- ↑ Haisan Shi et al.: Biocompatible β-SrHPO4 clusters with dandelion-like structure as an alternative drug carrier. In: Materials Science and Engineering C. Band 81, 1. Dezember 2017, S. 8–12, doi:10.1016/j.msec.2017.07.034.
- ↑ Lu Zhenzhen et al.: Facile Synthesis of β-SrHPO4 with Wide Applications in the Effective Removal of Pb2+ and Methyl Blue. In: Journal of Chemical & Engineering data. 7. August 2017.