Uridintriphosphat
Uridintriphosphat (UTP) ist ein Nukleosidtriphosphat mit der Base Uracil. Es ist ein RNA-Baustein, der unter Abspaltung zweier Phosphatgruppen (Pyrophosphat) in die RNA eingebaut wird, und der als Koenzym zur Aktivierung von Zuckern dient, die in Polysaccharide eingebaut werden sollen. Hierfür bindet es Hexosen in Form eines Esters, so dass eine UDP-Hexose entsteht.
| Strukturformel | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
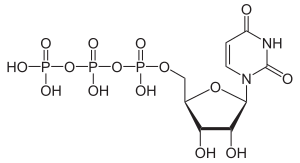
| |||||||||||||||||||
| Allgemeines | |||||||||||||||||||
| Name | Uridintriphosphat | ||||||||||||||||||
| Andere Namen |
| ||||||||||||||||||
| Summenformel | C9H15N2O15P3 | ||||||||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||||||||
| |||||||||||||||||||
| Eigenschaften | |||||||||||||||||||
| Molare Masse | 484,14 g·mol−1 | ||||||||||||||||||
| Sicherheitshinweise | |||||||||||||||||||
| |||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). | |||||||||||||||||||
Die Umesterung von UTP und Glucose-1-phosphat zu UDP-Glucose und Pyrophosphat aktiviert die D-Glucose für den Einbau in Glykogenpolymere (überzähliger Zucker wird in Tieren als Glycogen gespeichert). Dieser Prozess wird durch das Enzym Glucose-1-phosphat-UTP-Transferase katalysiert.[2]
Bei der Isomerisierung von D-Galactose in Glucose wird zunächst UDP-Galactose gebildet, welche dann in UDP-Glucose umgewandelt wird. Diese gibt ihr UDP an die nächste Galactose weiter.
Siehe auch
BearbeitenWeitere Ribonukleosidtriphosphate:
- Adenosintriphosphat (ATP)
- Cytidintriphosphat (CTP)
- Guanosintriphosphat (GTP)
Einzelnachweise
Bearbeiten- ↑ Dieser Stoff wurde in Bezug auf seine Gefährlichkeit entweder noch nicht eingestuft oder eine verlässliche und zitierfähige Quelle hierzu wurde noch nicht gefunden.
- ↑ Georg Löffler, Petro E. Petrides, Peter C. Heinrich (Hrsg.): Biochemie und Pathobiochemie. 8., völlig neu bearb. Auflage. Springer, Berlin, Heidelberg 2007, ISBN 978-3-540-32680-9, S. 369.