Zapnometinib
Zapnometinib ist ein experimenteller Arzneistoff aus der Gruppe der Kinasehemmer, der vom deutschen Pharmaunternehmen Atriva zur Behandlung von COVID-19 entwickelt wird.
| Strukturformel | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
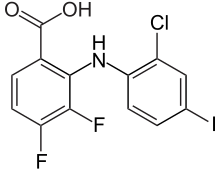
| |||||||||||||||||||
| Allgemeines | |||||||||||||||||||
| Freiname | Zapnometinib (vorgeschlagen[1]) | ||||||||||||||||||
| Andere Namen |
| ||||||||||||||||||
| Summenformel | C13H7ClF2INO2 | ||||||||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||||||||
| |||||||||||||||||||
| Arzneistoffangaben | |||||||||||||||||||
| Wirkstoffklasse | |||||||||||||||||||
| Eigenschaften | |||||||||||||||||||
| Molare Masse | 409,55 g·mol−1 | ||||||||||||||||||
| Aggregatzustand |
Fest[2] | ||||||||||||||||||
| Löslichkeit |
In Wasser: < 1 mg/L[2] | ||||||||||||||||||
| Sicherheitshinweise | |||||||||||||||||||
| |||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). | |||||||||||||||||||
Eigenschaften
BearbeitenDer Wirkstoff ist ein oral bioverfügbarer, niedermolekularer Inhibitor der Mitogen-aktivierten Proteinkinase-Kinase-Kinase (MAP2K; MAPK/ERK-Kinase; MEK), der in vitro antivirale und entzündungshemmende Aktivität zeigt. Er soll sowohl die Virus-Replikation hemmen als auch die körpereigene Immunantwort günstig beeinflussen.
Wirkungsmechanismus
BearbeitenIn einer Studie, in der die Eignung des Raf/MEK/ERK-Signalwegs (MAP-Kinase-Weg) als medikamentöses Ziel für die Behandlung von SARS-CoV-2-Infektionen untersucht wurde, zeigte Zapnometinib (ATR-002) als spezifischer Inhibitor der MEK1/2-Kinasen eine starke Anti-SARS-CoV-2-Aktivität in Zelllinien sowie in einem Luft-Flüssig-Grenzfläche-Zellkulturmodell (Air liquid interface cell culture, ALI). Auch vermochte Zapnometinib in Laborversuchen die SARS-CoV-2-induzierte Expression von pro-inflammatorischen Zytokinen zu beeinträchtigen, was die COVID-19-assoziierte schwere Entzündungsreaktion (Hyperinflammation) verhindern könnte, die eine Schlüsselrolle bei der Progression von COVID-19 spielt.[3]
Klinische Prüfung
BearbeitenNach Angaben von Atriva läuft eine klinische Phase-2-Studie (RESPIRE[4]) an hospitalisierten Patienten mit mittelschwerem bis schwerem COVID-19.[5]
Sonstiges
BearbeitenFür die Behandlung von Infektionen mit Hantaviren hat Zapnometinib in den USA die Einstufung als Orphan-Arzneimittel.[6] Auch die Wirkung gegen Grippeviren wurde untersucht.[7]
Der bereits zur COVID-19-Behandlung zugelassene Kinasehemmer Baricitinib wirkt an anderen Kinasen, nämlich den Januskinasen.
Literatur
Bearbeiten- D. Hüttmann: Neuer Kinasehemmer soll gegen alle Corona-Varianten wirken. Pharmazeutische Zeitung, 29. März 2022.
Einzelnachweise
Bearbeiten- ↑ INN Proposed List 125, World Health Organisation (WHO), 28. Juli 2021.
- ↑ a b c d Zapnometinib Safety Data Sheet, selleckchem.com, abgerufen am 29. März 2022.
- ↑ A. Schreiber, D. Viemann, J. Schöning, S. Schloer, A. Mecate Zambrano, L. Brunotte, A. Faist, M. Schöfbänker, E. Hrincius, H. Hoffmann, M. Hoffmann, S. Pöhlmann, U. Rescher, O. Planz, S. Ludwig: The MEK1/2-inhibitor ATR-002 efficiently blocks SARS-CoV-2 propagation and alleviates pro-inflammatory cytokine/chemokine responses. In: Cellular and Molecular Life Sciences. Band 79, Nr. 1, 2022, doi:10.1007/s00018-021-04085-1.
- ↑ Klinische Studie (Phase 2): Clinical Trial to Evaluate the Safety and Efficacy of ATR-002 in Adult Hospitalized Patients With COVID-19 (RESPIRE) bei Clinicaltrials.gov der NIH
- ↑ Atriva Therapeutics announces efficacy of its lead compound zapnometinib against OmicronAtriva Pressemitteilung, 28. März 2022.
- ↑ Eintrag 853921 in der Datenbank „Orphan Drug Designations and Approvals“, FDA, abgerufen am 29. März 2022.
- ↑ M. Laure, H. Hamza, J. Koch-Heier, M. Quernheim, C. Müller, A. Schreiber, G. Müller, S. Pleschka, S. Ludwig, O. Planz: Antiviral efficacy against influenza virus and pharmacokinetic analysis of a novel MEK-inhibitor, ATR-002, in cell culture and in the mouse model. In: Antiviral Research. 2020, doi:10.1016/j.antiviral.2020.104806.