Zavegepant
Zavegepant ist ein Arzneistoff aus der Wirkstoffklasse der niedermolekularen CGRP-Rezeptor-Antagonisten (Gepante). Unter dem Namen Zavzpret (Pfizer) wurde er im März 2023 in den USA zugelassen zur akuten Behandlung der Migräne mit und ohne Aura bei Erwachsenen.
| Strukturformel | ||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
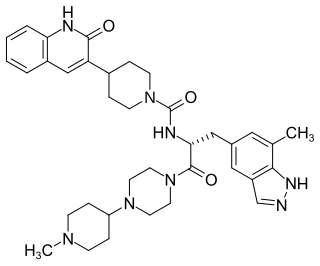
| ||||||||||||||||
| Allgemeines | ||||||||||||||||
| Freiname | Zavegepant[1] | |||||||||||||||
| Andere Namen |
| |||||||||||||||
| Summenformel | C36H46N8O3 | |||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||
| ||||||||||||||||
| Arzneistoffangaben | ||||||||||||||||
| Wirkstoffklasse | ||||||||||||||||
| Wirkmechanismus |
Hemmung des CGRP-Rezeptors | |||||||||||||||
| Eigenschaften | ||||||||||||||||
| Molare Masse | 638,80 g·mol−1 | |||||||||||||||
| pKS-Wert |
4,8 und 8,8[2] | |||||||||||||||
| Sicherheitshinweise | ||||||||||||||||
| ||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). | ||||||||||||||||
Zavegepant wird als Nasenspray verabreicht. Es ist der erste CGRP-Rezeptor-Antagonist zur nasalen Anwendung.[4]
Eigenschaften
BearbeitenZavegepant wird pharmazeutisch in Form seines Salzsäuresalzes (1:1), Zavegepanthydrochlorid,[5] eingesetzt. Zavegepanthydrochlorid ist ein weißes bis fast weißes Pulver und leicht löslich in Wasser.[2] Die pKs-Werte betragen 4,8 und 8,8, die molare Masse ist 675,28 g·mol−1.[2]
Wirkungsmechanismus
BearbeitenGepante sind niedermolekulare CGRP-Rezeptor-Antagonisten. CGRP steht für Calcitonin Gene-Related Peptide, ein Neuropeptid, das an der Auslösung von Migräneanfällen beteiligt ist.
Zavegepant blockiert den CGRP-Rezeptor und hebt dadurch die Effekte von CGRP auf.
Klinische Prüfung
BearbeitenDie Zulassung basiert auf zwei randomisierten, doppelblinden, placebokontrollierten Studien (Studie 1[6][7] und Studie 2[8]) mit insgesamt circa 2000 Teilnehmern, in denen Zavegepant gegen Placebo untersucht wurde.
Ein Endpunkt in beiden Studien war die Schmerzfreiheit nach zwei Stunden, die jeweils in der Verum-Gruppe signifikant häufiger erreicht wurde als in der Placebo-Gruppe (Studie 1: 23,6 vs. 14,9 Prozent, Studie 2: 22,5 vs. 15,5 Prozent). Hinsichtlich der Beseitigung von den am meisten störenden Symptomen (Lichtempfindlichkeit, Übelkeit, Lärmempfindlichkeit) zwei Stunden nach der Einnahme war Zavegepant gegenüber Placebo ebenfalls statistisch überlegen.[2] Auch bei weiteren Endpunkten (Schmerzlinderung nach 2 Stunden, Rückkehr zur normalen Funktion nach 2 Stunden, anhaltende Schmerzfreiheit innerhalb 2 bis 48 Stunden nach Nasenspray-Anwendung) zeigte Zavegepant eine bessere Wirksamkeit im Vergleich zu Placebo.[2]
Die häufigsten unerwünschten Wirkungen, die bei mehr als 2 Prozent der Patienten und häufiger als bei Placebo berichtet wurden, waren Geschmacksstörungen, Übelkeit, nasale Beschwerden und Erbrechen.[2]
Handelsnamen
BearbeitenZavzpret (USA)
Einzelnachweise
Bearbeiten- ↑ INN Recommended List 86, World Health Organisation (WHO), 2. September 2021.
- ↑ a b c d e f Prescribing information Zavzpret, Pfizer, März 2023.
- ↑ Dieser Stoff wurde in Bezug auf seine Gefährlichkeit entweder noch nicht eingestuft oder eine verlässliche und zitierfähige Quelle hierzu wurde noch nicht gefunden.
- ↑ G. Gnegel: Erstes Migräne-Nasenspray mit „Gepant“ in den USA zugelassen. In: deutsche-apotheker-zeitung.de. 15. März 2023, abgerufen am 15. April 2023.
- ↑ Externe Identifikatoren von bzw. Datenbank-Links zu Zavegepanthydrochlorid: CAS-Nr.: 1414976-20-7, PubChem: 134819878, ChemSpider: 81367517, Wikidata: Q99389114.
- ↑ Klinische Studie (Phase 3): Randomized Trial in Adult Participants With Acute Migraines bei Clinicaltrials.gov der NIH
- ↑ Richard B. Lipton, Robert Croop, David A. Stock, Jennifer Madonia, Micaela Forshaw, Meghan Lovegren, Linda Mosher, Vladimir Coric, Peter J Goadsby: Safety, tolerability, and efficacy of zavegepant 10 mg nasal spray for the acute treatment of migraine in the USA: a phase 3, double-blind, randomised, placebo-controlled multicentre trial. In: Lancet Neurology. 2023, Band 22, Nummer 3, S. 209–217 doi:10.1016/S1474-4422(22)00517-8.
- ↑ Klinische Studie (Phase 2, 3): Acute Treatment Trial in Adult Subjects With Migraines bei Clinicaltrials.gov der NIH