2,2,5-Tribromcyclopentanonethylenketal
2,2,5-Tribromcyclopentanonethylenketal ist eine chemische Verbindung aus der Gruppe der substituierten Acetale. Die Verbindung ist eine Zwischenstufe bei der Synthese des Cubans.
| Strukturformel | ||||||||||
|---|---|---|---|---|---|---|---|---|---|---|
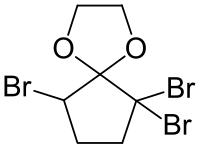
| ||||||||||
| Allgemeines | ||||||||||
| Name | 2,2,5-Tribromcyclopentanonethylenketal | |||||||||
| Andere Namen |
| |||||||||
| Summenformel | C7H9Br3O2 | |||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||
| ||||||||||
| Eigenschaften | ||||||||||
| Molare Masse | 364,86 g·mol−1 | |||||||||
| Aggregatzustand |
fest | |||||||||
| Sicherheitshinweise | ||||||||||
| ||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). | ||||||||||
Synthese
Bearbeiten2,2,5-Tribromcyclopentanonethylenketal kann über eine dreifache Bromierung mit Brom von Cyclopentanonethylenketal in 1,4-Dioxan synthetisiert werden.[2] Um Nebenreaktionen zu vermeiden wird das Reaktionsgemisch auf unter 10 °C gekühlt. Nach der Zugabe wird das Gemisch für etwa 48 Stunden bei Raumtemperatur gerührt, um sicherzustellen, dass die Reaktion fertiggestellt ist. Dies kann unter anderem an einer Farbänderung der Reaktionslösung von orangerot nach gelbgold erkannt werden. Da entstehender Bromwasserstoff den Druck in dem Rundkolben deutlich erhöht, sollte eine Gaswaschflasche angeschlossen werden, um das Bromwasserstoffgas zu neutralisieren und für einen stetigen Druckausgleich zu sorgen. Nach der Reaktionszeit wird das Gemisch neutralisiert und aufgereinigt, in Diethylether gelöst und in einem Eisbad auskristallisiert. Eine Rekristallisation aus Ethanol ist möglich.[2]
Einzelnachweise
Bearbeiten- ↑ Dieser Stoff wurde in Bezug auf seine Gefährlichkeit entweder noch nicht eingestuft oder eine verlässliche und zitierfähige Quelle hierzu wurde noch nicht gefunden.
- ↑ a b Philip E. Eaton: Cubane: Ausgangsverbindungen für die Chemie der neunziger Jahre und des nächsten Jahrhunderts. In: Angewandte Chemie. Band 104, Nr. 11, November 1992, S. 1447–1462, doi:10.1002/ange.19921041105.