2,4-Dibromphenol
2,4-Dibromphenol ist eine chemische Verbindung, die sowohl zu den Phenolen als auch zu den Halogenaromaten zählt.
| Strukturformel | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
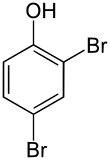
| |||||||||||||||||||
| Allgemeines | |||||||||||||||||||
| Name | 2,4-Dibromphenol | ||||||||||||||||||
| Andere Namen |
2,4-Dibrom-1-hydroxybenzol | ||||||||||||||||||
| Summenformel | C6H4Br2O | ||||||||||||||||||
| Kurzbeschreibung |
weißer bis hellbrauner Feststoff mit phenolartigem Geruch[1] | ||||||||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||||||||
| |||||||||||||||||||
| Eigenschaften | |||||||||||||||||||
| Molare Masse | 251,9 g·mol−1 | ||||||||||||||||||
| Aggregatzustand |
fest | ||||||||||||||||||
| Schmelzpunkt | |||||||||||||||||||
| Siedepunkt | |||||||||||||||||||
| Dampfdruck |
386 mPa (25 °C)[4] | ||||||||||||||||||
| pKS-Wert |
7,79 (25 °C)[2] | ||||||||||||||||||
| Löslichkeit |
2,2 g·l−1[1] | ||||||||||||||||||
| Sicherheitshinweise | |||||||||||||||||||
| |||||||||||||||||||
| Toxikologische Daten |
>2000 mg·kg−1 (LD50, Hase, transdermal)[4] | ||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). | |||||||||||||||||||
Darstellung
Bearbeiten2,4-Dibromphenol kann durch Bromierung von 3-Trimethylsilylphenol mit stöchiometrischen Mengen von elementarem Brom und anschließender Hydrolyse hergestellt werden. Bei Verwendung von überschüssigem Brom entsteht 2,3,4,6-Tetrabromphenol.[5]
Eigenschaften
BearbeitenDer Flammpunkt von 2,4-Dibromphenol liegt bei 113 °C.[3]
Derivate
BearbeitenDer Methylether kann durch Methylierung mit Dimethylsulfat hergestellt werden und ist auch unter dem Trivialnamen 2,4-Dibromanisol bekannt. Sein Schmelzpunkt liegt bei 61,5 °C, sein Siedepunkt bei 272 °C.[2]
Der Ethylether mit dem Trivialnamen 2,4-Dibromphenetol (CAS-Nummer: 38751-57-4) schmilzt bei 53,5 °C.[2]
Veresterung mit Essigsäureanhydrid liefert das Acetat, das bei 36 °C schmilzt (CAS-Nummer: 36914-79-1).[2]
Weitere Bromierung von 2,4-Dibromphenol mit Brom in Kaliumbromid-Lösung liefert 2,4,6-Tribromphenol, das seinerseits mit Brom zum 2,4,4,6-Tetrabrom-2,5-cyclohexadienon weiterreagiert.[6] Diese Reaktion kann durch Iodwasserstoff umgekehrt werden.[7]
Einzelnachweise
Bearbeiten- ↑ a b c Datenblatt 2,4-Dibromphenol bei Alfa Aesar, abgerufen am 2. August 2010 (Seite nicht mehr abrufbar).
- ↑ a b c d e f Dictionary of organic compounds, S. 1971 (eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ a b c d Datenblatt 2,4-Dibromophenol bei Sigma-Aldrich, abgerufen am 26. April 2011 (PDF).
- ↑ a b Paul Howe et al.: "2,4,6-tribromophenol and other simple brominated Phenols" (eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ Tadashi Hashimoto: "Synthesis of Organosilicon Compounds VII. On the Reaction of 3-Trimethylsilylphenol with Electrophilic Reagents", in: Yakugaku Zasshi, 1960, 80, S. 1399–1404; PDF.
- ↑ John A. Price: "The Structure of Tribromophenol bromide", in: J. Am. Chem. Soc., 1955, 77 (20), S. 5436–5437; doi:10.1021/ja01625a081.
- ↑ Hans P. Latscha, Helmut A. Klein, Gerald W. Linti: "Analytische Chemie: Chemie-Basiswissen III", S. 287 (eingeschränkte Vorschau in der Google-Buchsuche).
