Ammoniumcer(IV)-sulfat
chemische Verbindung
Ammoniumcer(IV)-sulfat ist eine anorganische chemische Verbindung aus der Gruppe der Sulfate, die üblicherweise als Dihydrat vorliegt.
| Strukturformel | ||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
 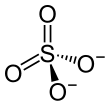
| ||||||||||||||||
| Allgemeines | ||||||||||||||||
| Name | Ammoniumcer(IV)-sulfat | |||||||||||||||
| Andere Namen |
| |||||||||||||||
| Summenformel | (NH4)4Ce(SO4)4 | |||||||||||||||
| Kurzbeschreibung | ||||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||
| ||||||||||||||||
| Eigenschaften | ||||||||||||||||
| Molare Masse | 632,55 g·mol−1 | |||||||||||||||
| Aggregatzustand |
fest[3] | |||||||||||||||
| Dichte |
0,8 g·cm−3 (Schüttdichte)[2] | |||||||||||||||
| Schmelzpunkt | ||||||||||||||||
| Löslichkeit | ||||||||||||||||
| Sicherheitshinweise | ||||||||||||||||
| ||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). | ||||||||||||||||
Gewinnung und Darstellung
BearbeitenAmmoniumcer(IV)-sulfat kann durch Reaktion einer Lösung von Cer(IV)-sulfat mit Ammoniumsulfat gewonnen werden.[5]
Eigenschaften
BearbeitenAmmoniumcer(IV)-sulfat ist ein als gelbe Kristalle oder gelb-oranges Pulver vorliegender Feststoff, der langsam löslich in Wasser ist.[1]
Verwendung
BearbeitenAmmoniumcer(IV)-sulfat-Dihydrat wird in der Dünnschichtchromatographie zum Nachweis von Antidepressiva in menschlichen Blut- und Urinproben verwendet.[3] Es dient auch als Oxidationsmittel und als Maßlösung für Redoxtitrationen (Cerimetrie).[6]
Einzelnachweise
Bearbeiten- ↑ a b c d World Health Organization: The International Pharmacopoeia. World Health Organization, 2006, ISBN 978-92-4156301-7, S. 1310 (eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ a b Datenblatt Ammoniumcer(IV)-sulfat-Dihydrat bei Merck, abgerufen am 13. September 2015.
- ↑ a b c Datenblatt Ammonium cerium(IV) sulfate dihydrate bei Sigma-Aldrich, abgerufen am 21. Mai 2017 (PDF).
- ↑ a b Eintrag zu Ammoniumcer(IV)-sulfatdihydrat in der GESTIS-Stoffdatenbank des IFA, abgerufen am 19. November 2022. (JavaScript erforderlich)
- ↑ Dale L. Perry: Handbook of Inorganic Compounds, Second Edition. CRC Press, 2011, ISBN 978-1-4398-1462-8, S. 19 (eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ Eberhard Nürnberg, Peter Surmann: Hagers Handbuch der pharmazeutischen Praxis Band 2: Methoden. Springer-Verlag, 2013, ISBN 978-3-642-61249-7, S. 356 (eingeschränkte Vorschau in der Google-Buchsuche).