Fluazinam
Fluazinam ist eine chemische Verbindung aus der Gruppe der 2,6-Dinitroaniline und Pyridine. Die Verbindung wurde von Ishihara Sangyō entwickelt und 1990 als Fungizid eingeführt.
| Strukturformel | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
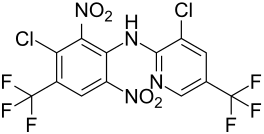
| |||||||||||||||||||
| Allgemeines | |||||||||||||||||||
| Name | Fluazinam | ||||||||||||||||||
| Andere Namen |
| ||||||||||||||||||
| Summenformel | C13H4Cl2F6N4O4 | ||||||||||||||||||
| Kurzbeschreibung |
gelbe, geruchslose Kristalle[1] | ||||||||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||||||||
| |||||||||||||||||||
| Eigenschaften | |||||||||||||||||||
| Molare Masse | 465,09 g·mol−1 | ||||||||||||||||||
| Aggregatzustand |
fest | ||||||||||||||||||
| Dichte |
1,76 g·cm−3[1] | ||||||||||||||||||
| Schmelzpunkt | |||||||||||||||||||
| Dampfdruck | |||||||||||||||||||
| Löslichkeit |
sehr schwer in Wasser (0,135 g·l−1 bei 20 °C)[2] | ||||||||||||||||||
| Sicherheitshinweise | |||||||||||||||||||
| |||||||||||||||||||
| Toxikologische Daten | |||||||||||||||||||
| Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). | |||||||||||||||||||
Gewinnung und Darstellung
BearbeitenFluazinam kann durch Umsetzung von 5,6-Dichlor-3-trifluormethylpyridin mit 2,6-Dinitro-3-chlor-4-trifluormethylanilin gewonnen werden. Alternativ kann 5,6-Dichlor-5-trifluormethylpyridin auch zuerst mit Ammoniak und anschließend mit 2,6-Dinitro-3-chlor-4-trifluormethylchlorbenzol umgesetzt werden. 5,6-Dichlor-5-trifluormethylpyridin entsteht durch Chlorierung und Fluorierung von 3-Methylpyridin.[5]
Verwendung
BearbeitenFluazinam ist ein nicht-systemisches Fungizid, das durch Unterbrechen der oxidativen Phosphorylierung wirkt.[1] Es wird unter dem Handelsnamen Shirlan als Fusariumbeize sowie gegen die Kraut- und Knollenfäule verwendet.
Zulassung
BearbeitenDie EU-Kommission nahm Fluazinam 2008 in die Liste der in der EU zulässigen Wirkstoffe von Pflanzenschutzmitteln auf.[6] In Deutschland, Österreich und der Schweiz sind Pflanzenschutzmittel mit dem Wirkstoff Fluazinam zugelassen.[7]
Toxikologie
BearbeitenFluazinam ist einer der stärksten bekannten Entkoppler der oxidativen Phosphorylierung. Verglichen mit Dinocap und Binapacryl ist Fluazinam jedoch deutlich weniger toxisch.[8]
Einzelnachweise
Bearbeiten- ↑ a b c d e f Müfit Bahadir, Harun Parlar, Michael Spiteller: Springer Umweltlexikon. Springer, 2000, ISBN 3-540-23480-2, S. 445 (eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ a b c Datenblatt Fluazinam bei Ishihara Sangyo Kaisha (PDF; 403 kB)
- ↑ a b Eintrag zu Fluazinam in der GESTIS-Stoffdatenbank des IFA, abgerufen am 10. Januar 2025. (JavaScript erforderlich)
- ↑ Eintrag zu fluazinam (ISO); 3-chloro-N-[3-chloro-2,6-dinitro-4-(trifluoromethyl)phenyl]-5-(trifluoromethyl)pyridin-2-amine im Classification and Labelling Inventory der Europäischen Chemikalienagentur (ECHA), abgerufen am 1. August 2016. Hersteller bzw. Inverkehrbringer können die harmonisierte Einstufung und Kennzeichnung erweitern.
- ↑ Thomas A. Unger: Pesticide Synthesis Handbook. William Andrew, 1996, ISBN 0-8155-1853-6, S. 865 (eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ Richtlinie 2008/108/EG der Kommission vom 26. November 2008 (PDF) zur Änderung der Richtlinie 91/414/EWG des Rates zwecks Aufnahme der Wirkstoffe Flutolanil, Benfluralin, Fluazinam, Fuberidazol und Mepiquat.
- ↑ Generaldirektion Gesundheit und Lebensmittelsicherheit der Europäischen Kommission: Eintrag zu Fluazinam in der EU-Pestiziddatenbank; Eintrag in den nationalen Pflanzenschutzmittelverzeichnissen der Schweiz, Österreichs (Eingabe von „Fluazinam“ im Feld „Wirkstoff“) und Deutschlands, abgerufen am 19. Februar 2016.
- ↑ Ze-jian Guo, Hideto Miyoshi, Terumasa Komyoji, Takahiro Haga, Toshio Fujita: Uncoupling activity of a newly developed fungicide, fluazinam [3-chloro-N-(3-chloro-2,6-dinitro-4-trifluoromethylphenyl)-5-trifluoromethyl-2-pyridinamine]. In: Biochimica et Biophysica Acta (BBA) - Bioenergetics. 1056. Jahrgang, Nr. 1, 1991, S. 89–92, doi:10.1016/S0005-2728(05)80077-5 (englisch).



