Lutetium(III)-oxid
Lutetium(III)-oxid ist eine chemische Verbindung aus der Gruppe der Oxide.
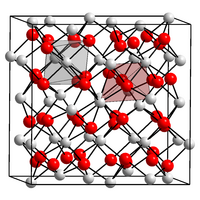
| Kristallstruktur | ||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| ||||||||||||||||
| _ Lu3+ _ O2− | ||||||||||||||||
| Allgemeines | ||||||||||||||||
| Name | Lutetium(III)-oxid | |||||||||||||||
| Andere Namen |
| |||||||||||||||
| Verhältnisformel | Lu2O3 | |||||||||||||||
| Kurzbeschreibung |
weißes Pulver[1] | |||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||
| ||||||||||||||||
| Eigenschaften | ||||||||||||||||
| Molare Masse | 397,93 g·mol−1 | |||||||||||||||
| Aggregatzustand |
fest[1] | |||||||||||||||
| Dichte |
9,42 g·cm−3[1] | |||||||||||||||
| Schmelzpunkt | ||||||||||||||||
| Siedepunkt |
3980 °C[2] | |||||||||||||||
| Löslichkeit | ||||||||||||||||
| Brechungsindex |
1,94743[3] | |||||||||||||||
| Sicherheitshinweise | ||||||||||||||||
| ||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). Brechungsindex: Na-D-Linie, 20 °C | ||||||||||||||||
Vorkommen
BearbeitenLutetium(III)-oxid kommt natürlich in sehr geringem Umfang (0,003 %) im Mineral Monazit vor.[4]
Gewinnung und Darstellung
BearbeitenLutetium(III)-oxid kann durch Verbrennung von Lutetium mit Sauerstoff (Luft)[5] oder am einfachsten durch Thermische Zersetzung von Lutetiumoxalat gewonnen werden.
Die Weltproduktion von Lutetium in Form von Lutetium(III)-oxid beträgt etwa 10 Tonnen pro Jahr.[4]
Lutetium(III)-oxid-Nanokristalle können durch Reaktion von Lutetiumnitrat mit Harnstoff gewonnen werden.[6]
Eigenschaften
BearbeitenLutetium(III)-oxid ist ein weißes Pulver, das unlöslich in Wasser ist.[1] Es ist hygroskopisch und absorbiert auch Kohlendioxid.[7] Es reagiert mit Säuren unter Kationenbildung, welche ihrerseits in Wasser schwach sauer reagieren.[8] Wie die anderen dreiwertigen Oxide der schwereren Lanthanoide kristallisiert es in der kubischen Lanthanoid-C-Struktur[5] mit a = 1039 pm und Z = 16. Es besitzt einen hohen Absorptionskoeffizienten für Röntgenstrahlen, was es als Szintillationsmaterial für medizinische Detektoren interessant macht.[9]
Verwendung
BearbeitenLutetium(III)-oxid wird zur Herstellung von Spezialgläsern und auch als Katalysator beim Cracken, zur Alkylierung, Hydrierung und Polymerisation verwendet. Es dient auch als Ausgangsstoff zur Herstellung von Lasermaterialien. Eine Verbindung aus Lutetium(III)-oxid und Palladium(II)-oxid (erzeugt bei hohem Druck und Temperatur in Gegenwart von Kaliumchlorat) besitzt Eigenschaften die für supraleitende Materialien interessant sind.[2]
Einzelnachweise
Bearbeiten- ↑ a b c d e f Datenblatt Lutetium (III) oxide, 99.99% trace metals basis bei Sigma-Aldrich, abgerufen am 11. März 2012 (PDF).
- ↑ a b c d e Reade: Lutetium Oxide Powder (Lu2O3) ( vom 6. Mai 2012 im Internet Archive)
- ↑ O. Medenbach et al.: Refractive index and optical dispersion of rare earth oxides using a small-prism technique, J. Opt. A: Pure Appl. Opt. 3, S. 174–177, 2001 doi:10.1088/1464-4258/3/3/303.
- ↑ a b John Emsley: Nature's building blocks: an A-Z guide to the elements. Oxford University Press, 2003, ISBN 978-0-19-850340-8, S. 300 (eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ a b A. F. Holleman, E. Wiberg, N. Wiberg: Lehrbuch der Anorganischen Chemie. 102. Auflage. Walter de Gruyter, Berlin 2007, ISBN 978-3-11-017770-1, S. 1941–1943.
- ↑ E. Zych, W. Mielcarek, M. Kojdecki, K. Domagala: X-ray investigation of lutetium oxide nanostructured material. Applied crystallography: proceedings of the XVIII conference, 2001, ISBN 978-981-02-4613-6, S. 302 (eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ Robert E. Krebs: The history and use of our earth's chemical elements: a reference guide. Greenwood Pub Group, 2006, ISBN 978-0-313-33438-2, S. 304 (eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ Periodensystem-online: Lutetium(III)-oxid
- ↑ Oliver T. Chang: Frontal semiconductor research. Nova Science Publishers, 2006, ISBN 978-1-60021-210-9, S. 7 (eingeschränkte Vorschau in der Google-Buchsuche).
