Quercetin-3-O-sambubiosid
Quercetin-3-O-sambubiosid ist ein Glycosid des Flavonols Quercetin. Die Zuckerkomponente ist die Sambubiose.
| Strukturformel | |||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
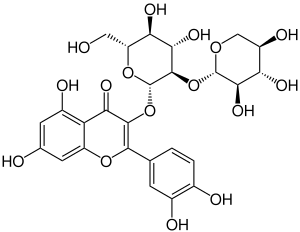
| |||||||||||||
| Allgemeines | |||||||||||||
| Name | Quercetin-3-O-sambubiosid | ||||||||||||
| Andere Namen |
2-(3,4-Dihydroxyphenyl)-5,7-dihydroxy-4-oxo-4H-chromen-3-yl-2-O-β-D-xylopyranosyl-β-D-glucopyranosid | ||||||||||||
| Summenformel | C26H28O16 | ||||||||||||
| Kurzbeschreibung |
weißer Feststoff[1] | ||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||
| |||||||||||||
| Eigenschaften | |||||||||||||
| Molare Masse | 596,5 g·mol−1 | ||||||||||||
| Aggregatzustand |
fest[1] | ||||||||||||
| Sicherheitshinweise | |||||||||||||
| |||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). | |||||||||||||
Vorkommen
BearbeitenQuercetin-3-O-sambubiosid kommt natürlich in verschiedenen Pflanzen vor. So ist es für eine rote Farbe in den Blüten des Mandeleibischs (Hibiscus mutabilis)[2] verantwortlich und kommt auch in Roselle (Hibiscus sabdariffa) vor.[3] Des Weiteren kommt es in der Japanischen Wollmispel[4][5] und der Indischen Lotosblume,[6] sowie in den Beeren von Ribes biebersteinii[7] und den Blüten von Eucommia ulmoides[8] vor.
Eigenschaften
BearbeitenQuercetin-3-O-sambubiosid wirkt als Radikalfänger wie in einer Untersuchung mit Diphenylpikrylhydrazyl festgestellt wurde.[7] Quercetin-3-O-sambubiosid kann außerdem das reaktive Peroxynitrit neutralisieren, beziehungsweise seine Bildung hemmen. Peroxynitrit hat verschiedene schädliche Effekte im Metabolismus, indem es mit Tyrosin-Einheiten in Proteinen reagiert, die Aconitase hemmt und Strangbrüche in DNA verursacht.[4]
Einzelnachweise
Bearbeiten- ↑ a b c d MedChemExpress: Quercetin 3-O-sambubioside, >98%, abgerufen am 8. Februar 2024.
- ↑ Siu Kuin Wong, Eric Wei Chiang Chan: Botany, uses, phytochemistry and pharmacology of Vallaris: A short review. In: Pharmacognosy Journal. Band 5, Nr. 5, September 2013, S. 242–246, doi:10.1016/j.phcgj.2013.10.001.
- ↑ Yassine Oulad El Majdoub, Giovanna Ginestra, Giuseppina Mandalari, Paola Dugo, Luigi Mondello, Francesco Cacciola: The Digestibility of Hibiscus sabdariffa L. Polyphenols Using an In Vitro Human Digestion Model and Evaluation of Their Antimicrobial Activity. In: Nutrients. Band 13, Nr. 7, 10. Juli 2021, S. 2360, doi:10.3390/nu13072360, PMID 34371869, PMC 8308902 (freier Volltext).
- ↑ a b Hyun Ah Jung, Jong Cheol Park, Hae Young Chung, Jong Kim, Jae Sue Choi: Antioxidant flavonoids and chlorogenic acid from the leaves ofEriobotrya japonica. In: Archives of Pharmacal Research. Band 22, Nr. 2, April 1999, S. 213–218, doi:10.1007/bf02976549.
- ↑ Hyun Ah Jung, Jong Cheol Park, Hae Young Chung, Jong Kim, Jae Sue Choi: Antioxidant flavonoids and chlorogenic acid from the leaves ofEriobotrya japonica. In: Archives of Pharmacal Research. Band 22, Nr. 2, April 1999, S. 213–218, doi:10.1007/bf02976549.
- ↑ Shengguo Deng, Zeyuan Deng, Yawei Fan, Jing Li, Rong Liu, Dongmei Xiong: Application of high-speed counter-current chromatography coupled with high performance liquid chromatography for the separation and purification of Quercetin-3-O-sambubioside from the leaves of Nelumbo nucifera. In: Frontiers of Chemical Engineering in China. Band 3, Nr. 4, Dezember 2009, S. 375–382, doi:10.1007/s11705-009-0247-9.
- ↑ a b Abbas Delazar, Laleh Khodaie, Jalil Afshar, Lutfun Nahar, Satyajit Sarker: Isolation and free-radical-scavenging properties of cyanidin 3-O-glycosides from the fruits of Ribes biebersteinii Berl. In: Acta Pharmaceutica. Band 60, Nr. 1, 1. März 2010, S. 1–11, doi:10.2478/v10007-010-0007-x.
- ↑ Xin Li, Lipeng Yang, Shaoyang Liu, Dongqing Fei, Min Zhang, Yuxian Zhang: Effect of Quercetin-3-O-Sambubioside Isolated from Eucommia ulmoides Male Flowers on Spontaneous Activity and Convulsion Rate in Mice. In: Planta Medica. Band 80, Nr. 12, 6. August 2014, S. 974–977, doi:10.1055/s-0034-1382902.