Tafel-Gleichung
Die Tafel-Gleichung beschreibt im Bereich der Elektrochemie näherungsweise den Zusammenhang zwischen der Stromdichte an einer Elektrode und dem Elektrodenpotential. Sie ist nach Julius Tafel benannt, der sie 1905 empirisch fand.[1] Die Tafel-Gleichung ist hilfreich bei Berechnungen der Zellspannung elektrochemischer Zellen, vor allem bei der Elektrolyse.
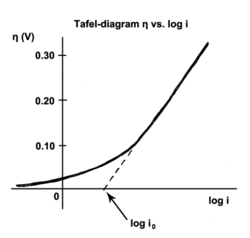
Auch für die Diskussion des Spannungsabfalls in einer Brennstoffzelle bei einem gegebenen Strom ist sie wichtig, hier lautet eine Aussage der Gleichung:
- Bei gegebenem Strom ist der elektrochemisch bedingte Spannungsabfall umso niedriger, je höher der Austauschstrom der Zelle ist.
Der Austauschstrom hängt ab von dem in der Brennstoffzelle verwendeten Katalysator. Daher ist ein Ziel der Weiterentwicklung von Brennstoffzellen, Katalysatoren zu finden, die diesen Strom maximieren.
Formel
Bearbeitenmit
- dem Spannungsabfall
- der allgemeinen Gaskonstante
- der absoluten Temperatur
- dem Durchtritts- oder Symmetriefaktor
- der Zahl der übertragenen Elektronen
- der Faraday-Konstante
- dem natürlichen Logarithmus
- der Austauschstromdichte
- der Stromdichte .
Gültigkeitsbereich
BearbeitenDie Tafel-Gleichung gilt nur näherungsweise in einem mittleren Strombereich. Für kleinere Stromstärken bzw. kleine Überspannungen muss die genauere Butler-Volmer-Gleichung verwendet werden.
Siehe auch
BearbeitenEinzelnachweise
Bearbeiten- ↑ Julius Tafel: Über die Polarisation bei kathodischer Wasserstoffentwicklung. In: Wilhelm Ostwald, J. H. van't Hoff (Hrsg.): Zeitschrift für physikalische Chemie, Stöchiometrie und Verwandtschaftslehre. Band 50. Wilhelm Engelmann, Leipzig 1905, S. 641–712, doi:10.1515/zpch-1905-5043 (PDF).