Withasomnin
Withasomnin ist ein natürliches Alkaloid aus der Gruppe der Pyrazole und zählt somit zu den Heterocyclen. Es wurde 1966 erstmals aus der Wurzel der Schlafbeere isoliert, von deren lateinischem Namen (Withania somnifera) sich auch der Trivialname durch Kontraktion (zusammen mit der Endung -in) ableitet.
| Strukturformel | |||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
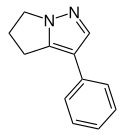
| |||||||||||||
| Allgemeines | |||||||||||||
| Name | Withasomnin | ||||||||||||
| Andere Namen |
3-Phenyl-5,6-dihydro-4H-pyrrolo[1,2-b]pyrazol | ||||||||||||
| Summenformel | C12H12N2 | ||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||
| |||||||||||||
| Eigenschaften | |||||||||||||
| Molare Masse | 184,24 g·mol−1 | ||||||||||||
| Sicherheitshinweise | |||||||||||||
| |||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). | |||||||||||||
Aufbau und Synthese
BearbeitenWithasomnin lässt sich gedanklich in zwei Untereinheiten zerlegen: Δ1-Pyrrolin (gebildet aus L-Ornithin) und Phenethylamin (gebildet aus L-Phenylalanin).[2]
Morimoto et al. beschreiben 1968 ein erstes Verfahren zur Totalsynthese auf der Basis von 4-Phenyl-3-hydroxymethylpyrazol.[3][4] Anschließend wurden zahlreiche weitere Syntheseverfahren entwickelt, beispielhaft erwähnt seien hier ein frühes Ein-Schritt-Verfahren durch Cycloaddition von Phenylacetylen an die mesoionische Verbindung[5] sowie ein aktuelles Verfahren unter Nutzung von Radikalen (radikalischer Ringschluss).[6]
Vorkommen von Withasomnin
BearbeitenWithasomnin gehört – neben weiteren Alkaloiden, Withanoliden, Aminosäuren und Polyphenolen – zu den pharmakologisch wirksamen Bestandteilen der Schlafbeere, die in der ayurvedischen Medizin vielseitige Verwendung findet.
Erstmals isoliert wurde das Withasomnin 1966 in einem alkoholischen Extrakt aus den Wurzeln der Schlafbeere,[7] später konnte es auch in deren Blättern nachgewiesen werden.[8] Daneben findet sich Withasomnin auch in weiteren, auf dem afrikanischen Kontinent heimischen Pflanzen wie Newbouldia laevis,[9] Discopodium penninervium[10] und Elytraria Acaulis.[11]
Eigenschaften
BearbeitenFrühe Studien verweisen auf die Non-Toxizität von Withasomnin sowie dessen schmerzlindernde, lokal betäubende, krampflösende und narkotische Wirkung.[2] Ganz aktuell wurde das antimikrobielle Potenzial von Withasomnin in Docking-Studien mit einem Zielprotein vom Typ Topoisomerase IV nachgewiesen.[12]
Zumeist werden die pharmakologischen Eigenschaften von Withasomnin jedoch nicht isoliert, sondern im Verbund mit den anderen Alkaloiden der jeweiligen Pflanze thematisiert, oft in Überprüfung der traditionellen Verwendung. So ist die antibakterielle, entzündungshemmende, antioxidative, antitumorale, immunmodulatorische und neuroprotektive Wirkung für die Inhaltsstoffe der Schlafbeere gut belegt.[13] Analog dazu wurde auch die Anti-Malaria-Wirkung von Withasomnin nicht isoliert, sondern im Zusammenspiel mit Newbouldine und den weiteren Inhaltsstoffen der Newbouldia-Pflanze untersucht.[14]
Einzelnachweise
Bearbeiten- ↑ a b Datenblatt 3-Phenyl-5,6-dihydro-4H-pyrrolo[1,2-b]pyrazole (PDF) bei BLD Pharmatech, Katalognummer: BD01097699, abgerufen am 25. Januar 2023.
- ↑ a b Eckart Eich: Solanaceae and Convolvulaceae: Secondary Metabolites. Biosynthesis, Chemotaxonomy, Biological and Economic Significance (A Handbook). Springer, Berlin, Heidelberg 2008, ISBN 978-3-540-74540-2, S. 70–71, doi:10.1007/978-3-540-74541-9.
- ↑ Externe Identifikatoren von bzw. Datenbank-Links zu 4-Phenyl-3-hydroxymethylpyrazol: CAS-Nr.: 30159-34-3, PubChem: 22477654, Wikidata: Q116419430.
- ↑ Akira Morimoto, Kosei Noda, Takao Watanabe, Hisashi Takasugi: The total synthesis of withasomnine, a unique pyrazole alkaloid. In: Tetrahedron Letters. Band 9, Nr. 54, 1968, S. 5707–5710, doi:10.1016/S0040-4039(00)70757-X.
- ↑ Darshan Ranganathan, Shakti Bamezai: A Novel and Practical One Step Synthesis of 5,6-Dihydro -3-Phenyl-4H-Pyrrolo (1,2-b) Pyrazole (Withasomnine). In: Synthetic Communications. Band 15, Nr. 3, 1985, S. 259–265, doi:10.1080/00397918508063796.
- ↑ Steven M. Allin, William R. S. Barton, W. Russell Bowman, Tom McInally: Radical cyclisation onto pyrazoles: synthesis of withasomnine. In: Tetrahedron Letters. Band 43, Nr. 23, 2002, S. 4191–4193, doi:10.1016/S0040-4039(02)00763-3.
- ↑ H.-B. Schröter, D. Neumann, A. R. Katritzky, F. J. Swinbourne: Withasomnine. A pyrazole alkaloid from Withania somnifera Dun. In: Tetrahedron. Band 22, Nr. 8, 1966, S. 2895–2897, doi:10.1016/S0040-4020(01)99082-9.
- ↑ Kirson I., Glotter E.: 14 α–hydroxy steroids from Withania somnifera (L) Dunal. In: Journal of Chemical Research, Synopses. Band 10, 1980, S. 338–339.
- ↑ Saburi A. Adesanya, René Nia, Catherine Fontaine, Mary Païs: Pyrazole alkaloids from Newbouldia laevis. In: Phytochemistry. Band 35, Nr. 4, 1994, S. 1053–1055, doi:10.1016/S0031-9422(00)90667-8.
- ↑ Abraham Abebe Wube, Eva-Maria Wenzig, Simon Gibbons, Kaleab Asres, Rudolf Bauer, Franz Bucar: Constituents of the stem bark of Discopodium penninervium and their LTB4 and COX-1 and -2 inhibitory activities. In: Phytochemistry. Band 69, Nr. 4, 2008, S. 982–987, doi:10.1016/j.phytochem.2007.11.001.
- ↑ V Ravikanth, P Ramesh, P. V Diwan, Y Venkateswarlu: Pyrazole alkaloids from Elytraria acaulis. In: Biochemical Systematics and Ecology. Band 29, Nr. 7, 2001, S. 753–754, doi:10.1016/S0305-1978(00)00109-5.
- ↑ Tijith Kuzhiyil George, Anju Tomy, Manakulam Shaikmoideen Jisha: Molecular Docking Study of Bioactive Compounds of Withania somnifera Extract Against Topoisomerase IV Type B. In: Proceedings of the National Academy of Sciences, India Section B: Biological Sciences. Band 90, Nr. 2, 2020, S. 381–390, doi:10.1007/s40011-019-01110-z.
- ↑ Sumaira Saleem, Gulzar Muhammad, Muhammad Ajaz Hussain, Muhammad Altaf, Syed Nasir Abbas Bukhari: Withania somnifera L.: Insights into the phytochemical profile, therapeutic potential, clinical trials, and future prospective. In: Iranian Journal of Basic Medical Sciences. Band 23, Nr. 12, 2020, S. 1501–1526, doi:10.22038/ijbms.2020.44254.10378, PMID 33489024.
- ↑ Liliana Mammino, Mireille K. Bilonda: Computational study of antimalarial pyrazole alkaloids from Newbouldia laevis. In: Journal of Molecular Modeling. Band 20, Nr. 11, 2014, S. 2464, doi:10.1007/s00894-014-2464-5.
