Pyridindicarbonsäuren
Die Pyridindicarbonsäuren bilden in der Chemie eine Stoffgruppe von organischen Verbindungen, die zu den Heterocyclen (genauer: Heteroaromaten) zählt. Sie bestehen aus einem Pyridinring, der mit zwei Carboxygruppen (–COOH) substituiert ist. Durch deren unterschiedliche Anordnung ergeben sich sechs Konstitutionsisomere mit der Summenformel C7H5NO4.
Sie sind zumeist farblose Feststoffe, die sich in Wasser schlecht lösen. Die Schmelzpunkte liegen recht hoch bei rund 230 °C, wobei jedoch die Dinicotinsäure mit 320–325 °C deutlich nach oben abweicht. Chinolinsäure und Cinchomeronsäure zersetzen sich beim Erhitzen durch Decarboxylierung.
Die Pyridindicarbonsäuren sind generell aus den Lutidinen durch Oxidation der beiden Methylgruppen mit Salpetersäure darstellbar.[1]
Lediglich beim 2,4-Isomer wird der Name Lutidin auf das Produkt übernommen: Die Pyridin-2,4-dicarbonsäure trägt den Namen Lutidinsäure. Die Chinolinsäure entsteht durch Oxidation von Chinolin mit Kaliumpermanganat und erhielt dadurch ihren Namen.
Von der Picolinsäure (Pyridin-2-carbonsäure) leitet sich namentlich die Dipicolinsäure (Pyridin-2,6-dicarbonsäure) ab, die am Pyridin achsensymmetrisch in ortho-Stellung zwei Carboxygruppen trägt.
Von der Nicotinsäure (Pyridin-3-carbonsäure) leitet sich namentlich die Dinicotinsäure (Pyridin-3,5-dicarbonsäure) ab, die am Pyridin achsensymmetrisch in meta-Stellung zwei Carboxygruppen trägt.
| Pyridindicarbonsäuren | |||||||
| Name | Pyridin-2,3-dicarbonsäure | Pyridin-2,4-dicarbonsäure | Pyridin-2,5-dicarbonsäure | Pyridin-2,6-dicarbonsäure | Pyridin-3,4-dicarbonsäure | Pyridin-3,5-dicarbonsäure | |
| Andere Namen | Chinolinsäure | Lutidinsäure | Isocinchomeronsäure | Dipicolinsäure | Cinchomeronsäure | Dinicotinsäure | |
| Strukturformel | 
|

|

|

|

|
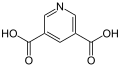
| |
| CAS-Nummer | 89-00-9 | 499-80-9 | 100-26-5 | 499-83-2 | 490-11-9 | 499-81-0 | |
| PubChem | 1066 | 10365 | 7493 | 10367 | 10273 | 10366 | |
| Summenformel | C7H5NO4 | ||||||
| Molare Masse | 167,12 g·mol−1 | ||||||
| Aggregatzustand | fest | ||||||
| Kurzbeschreibung | farblose Feststoffe | ||||||
| Schmelzpunkt | 185–190 °C (Zers.)[2] | 242–243 °C[3] | 236–237 °C[4] | 224–225 °C[5] | 266–270 °C (Zers.)[6] | 320–325 °C[7] | |
| pKs1-Wert (25 °C)[8] | 2,41 | 2,17 | 2,31 | 2,17 | 2,6 | 2,82 | |
| pKs2-Wert (25 °C)[8] | 5,05 | 5,09 | 5,06 | 4,97 | 5,07 | ||
| Löslichkeit in Wasser | 10 g·l−1 (20 °C)[2] | 2,49 g·l−1 (25 °C)[3] | 1,2 g·l−1 (25 °C)[4] | 5 g·l−1 (25 °C)[5] | 2,34 g·l−1 (25 °C)[6] | 1,0 g·l−1 (25 °C)[7] | |
| GHS- Kennzeichnung |
| ||||||
| H- und P-Sätze | 319‐335 | 315‐319‐335 | 315‐319‐335 | 315‐319‐335 | 315‐319‐335 | 315‐319‐335 | |
| keine EUH-Sätze | keine EUH-Sätze | keine EUH-Sätze | keine EUH-Sätze | keine EUH-Sätze | keine EUH-Sätze | ||
| 305+351+338 | 302+352‐304+340 305+351+338 |
302+352‐304+340 305+351+338 |
302+352 305+351+338 |
302+352‐304+340 305+351+338 |
302+352‐304+340 305+351+338 | ||
Literatur
Bearbeiten- Hans Meyer, Hans Tropsch: Über Derivate der Lutidinsäure und das αγ-Diaminopyridin. In: Monatshefte für Chemie, 35, 1914, S. 189–206, doi:10.1007/BF01518123.
- Hans Meyer, Hans Tropsch: Über Dinicotinsäure und deren Abbau zu ββ′-Diaminopyridin und über das αα′-Diaminopyridin. In: Monatshefte für Chemie, 35, 1914, S. 207–217, doi:10.1007/BF01518124.
Siehe auch
BearbeitenEinzelnachweise
Bearbeiten- ↑ Shinkichi Shimizu, Nanao Watanabe, Toshiaki Kataoka, Takayuki Shoji, Nobuyuki Abe, Sinji Morishita, Hisao Ichimura: „Pyridine and Pyridine Derivatives“, in: Ullmann's Encyclopedia of Industrial Chemistry, 2002 (doi:10.1002/14356007.a22_399).
- ↑ a b c Datenblatt Chinolinsäure bei Merck, abgerufen am 25. Dezember 2018.
- ↑ a b c Datenblatt Lutidinsäure bei Merck, abgerufen am 25. Dezember 2018.
- ↑ a b c Datenblatt Isocinchomeronsäure bei Merck, abgerufen am 3. April 2010.
- ↑ a b c Datenblatt Dipicolinsäure bei Merck, abgerufen am 3. April 2010.
- ↑ a b c Datenblatt Cinchomeronsäure bei Merck, abgerufen am 3. April 2010.
- ↑ a b c Datenblatt Dinicotinsäure bei Merck, abgerufen am 3. April 2010.
- ↑ a b D'Ans-Lax: Taschenbuch für Chemiker und Physiker, 3. Auflage, Band 1, Springer-Verlag, Berlin-Göttingen-Heidelberg 1967 (ChemieOnline – pKb- und pKs-Werte).
